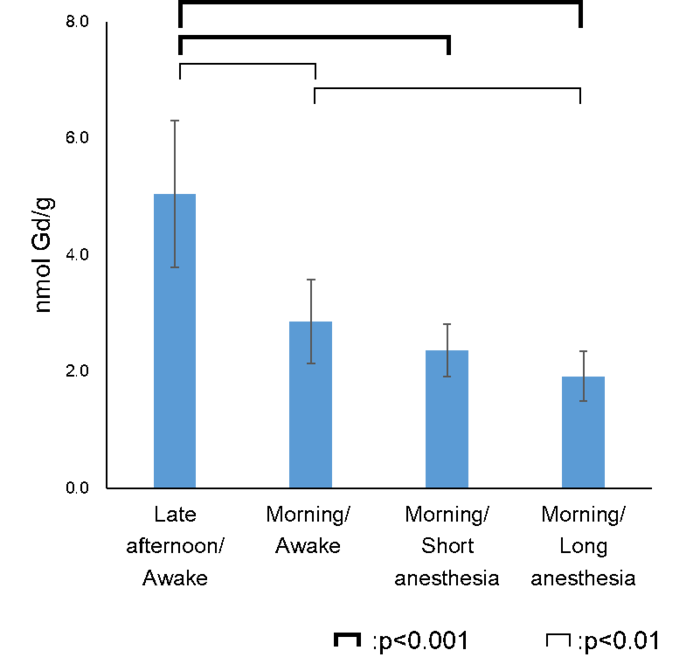- トップ
- 放射線科
放射線科
放射線科では、MRIを用いた脳の機能や微細構造の評価に関しての基礎的な研究を行っています。脳内の老廃物排泄系であるGlymphaticシステムのヒトでの画像評価に関して研究をおこなっています。また、脳の拡散画像に関しての後処理も含めた解析手法を含め、他の様々な画像的手法に関しても研究を行っています。
ヒト脳内Glymphatic システムの画像評価法の開発
Glymphaticシステムは、中枢神経系の廃棄物を、星状膠細胞により血管周囲に形成されたトンネル様の構造で脳脊髄液と共に除去する系であり、アルツハイマー病等の変性疾患に関連する異常蓄積蛋白もこの系で除去されます。この系の解明は主にラット脳での髄腔内へのトレーサー投与の実験によりなされ、ヒト脳での評価方法は確立されていません。私たちはその評価方法の確立を目指して研究を行っています。
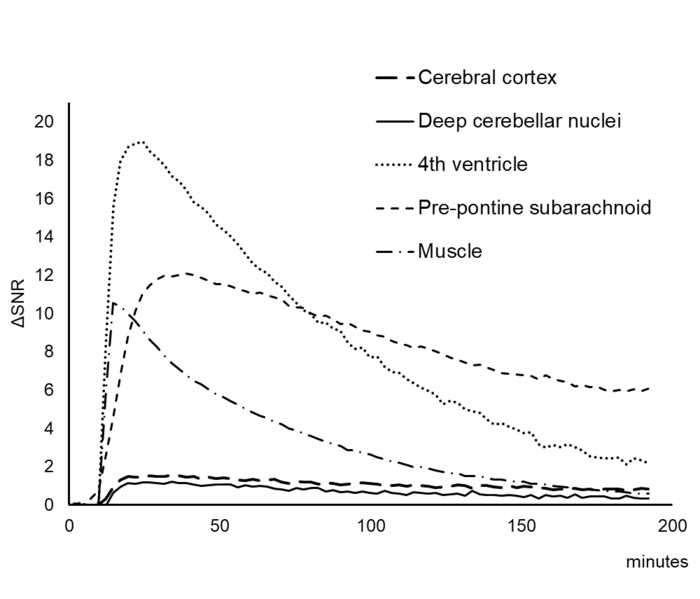
一つの手法はガドリニウム造影剤を経静脈的に投与して、脳脊髄液腔に漏出した微量の造影剤を経時的に追跡することで、Glymphaticシステムの評価を行うことを試みています。ヒト脳への応用の前段階として、ラットでの静脈内へのガドリニウム造影剤投与後の評価を行い、その手がかりを得ています。ラットに高用量のガドリニウム造影剤を静注した後、脳脊髄液や脳実質の信号強度を測定した実験では、静注したガドリニウム造影剤は比較的短い時間で脳脊髄液に移行することが確認されています。
また、経静脈的投与でのガドリニウムの脳内沈着のメカニズムに関しても検討しました。生理的状態では、Glymphaticシステムの活性は睡眠と関連しており、睡眠時には覚醒時と比較して活性が大幅に増大することが示されていて、睡眠時にグリア細胞の容積が縮小し、間質腔が拡張することが原因とされています。また、同様の効果が麻酔によっても得られる事も示されています。この知見に基づいて、2週間にわたって直鎖型ガドリニウム造影剤を睡眠前に繰り返し投与したラット群と、同じく睡眠後に投与した群での、脳内に残留するガドリニウムを測定したところ、睡眠前に投与した群で、残留ガドリニウムは有意に少ないことが示されました。投与時に麻酔を併用した群では、さらに残留ガドリニウムが少ないこともわかりました。このことから脳組織からのガドリニウムの洗い出しの効率に睡眠や麻酔が関与していることが示され、睡眠時に活性の増大するGlymphaticシステムが関連している可能性が示唆される結果となりました。
Taoka T, Jost G, Frenzel T, Naganawa S, Pietsch H. Investigative radiology 2018;53:529-34.
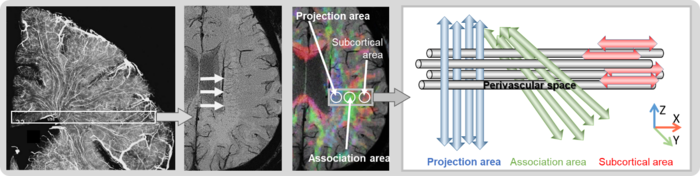
造影剤を使わずにGlymphatic systemを評価する手法として、拡散画像での評価に関しても検討をおこなっています。我々は血管周囲腔の走行方向に限定した拡散能がGlymphaticシステムの活性に相関すると仮定し、拡散テンソル画像から深部白質での水分子の動きを評価する手法として、diffusion tensor image analysis along the perivascular space (DTI-ALPS)という評価方法を提案しています。脳内での水分子の拡散能を評価しようとした場合、大きな白質線維の拡散の影響が大きく、血管周囲腔方向の評価は困難です。しかし、大きな白質線維と直交する方向であれば、その影響を分離できるはずです。ヒトの脳では、側脳室体部外側の白質では、髄質動静脈は脳室壁と直交する方向、つまり横断面での左右方向に走ります。また、側脳室に近い領域では錐体路をはじめとする投射線維が上下方向に走り、その外側では上縦束をはじめとする交連線維が前後方向に走ります。つまり、この領域では髄質動静脈の血管周囲腔の方向の拡散は、大きな白質線維の拡散の影響と分離して測定することができます。
DTI-ALPS法では側脳室体部外側の白質での血管周囲腔方向の拡散の程度の指標として、血管周囲腔の方向の拡散能を、血管周囲腔、および主な白質線維の走行方向と直交する方向の拡散能との比(ALPS index)を用いて評価します。
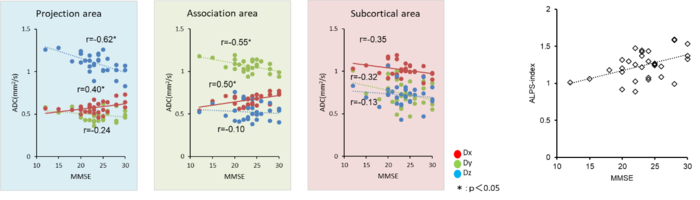
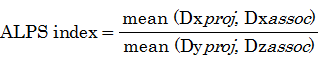 正常例、軽度認知機能低下症例、Alzheimer病症例を対象とした評価では、ALPS indexはMMSEスコアと有意に逆相関し、また年齢と有意に相関しました。このことから、ALPS indexがGlymphaticシステムの機能を反映した指標となり得る可能性が示唆されました。
正常例、軽度認知機能低下症例、Alzheimer病症例を対象とした評価では、ALPS indexはMMSEスコアと有意に逆相関し、また年齢と有意に相関しました。このことから、ALPS indexがGlymphaticシステムの機能を反映した指標となり得る可能性が示唆されました。
Taoka T, et al. Japanese journal of radiology 2017;35(4):172-78.
非正規分布拡散画像の評価方法の開発
MRIを用いて水分子の自由拡散の空間的な広がりを評価する拡散テンソル法は、1990年代に実用化され、主に白質構造の解析に用いられてきました。1999年にジョンスホプキンズ大学の森進教授によりトラクトグラフィーが開発されてからは、臨床での有用性が確立されるとともに、さらに多くの脳神経領域の研究に用いられてきています。拡散テンソル法は「拡散は正規分布に従う」という仮定に基づき、単一のb値、つまりsingle shellでの情報収集および解析を行う。しかし、生体内には複雑な壁構造があり、多数のコンパートメントが存在するため、single shell法による単純な正規分布モデルによる近似には限界があります。これを克服するには、様々なb値で(multi shells)、速い拡散から遅い拡散までの評価をすることが必要で、その手法を非正規分布拡散画像と呼びます。その一つにq-space imaging (QSI)があり、各ボクセルの拡散を詳細な確率分布関数の形で表現することができます。しかし、multi shells法には、必然的に撮像時間が長くなるという問題があります。これを解決する手法として、二つのb値(two shells)を用いた拡散尖度画像があります。拡散尖度は、比較的短い撮像時間で得られ、正規分布からの逸脱を評価することで、組織内の拡散分布の多様性、つまり、組織構築の複雑さ・不均一性を評価できます。ただ、拡散尖度の上昇が意味するものが具体的には明らかになりません。このことに対する解決法の一つがNeurite orientation dispersion and density imaging (NODDI)と呼ばれる非正規分布拡散画像の後処理の手法です。この手法はワトソン分布という数理モデルを用いて、脳内の微細構造を、細胞内の制限拡散、細胞間の束縛拡散、そして脳脊髄液成分の自由拡散の3つのコンパートメントに分けて解析する手法です。これまでに私たちは拡散尖度による脳梗塞組織の時間経過に関して、ラットモデル、臨床例での評価を行ってきました(図)。他施設との共同研究も行っており、神奈川県立こども医療センターと共同で、結節性硬化症での白質組織の変化に関して、上述のNODDIでの評価を行っています。
拡散尖度画像によるラット脳梗塞の時間経過。梗塞後の比較的早期から拡散尖度の上昇が見られ、正規分布モデルによるADC画像とは異なる時間経過を示します。
Taoka T,, Naganawa S et al.J Stroke Cerebrovasc Dis. 2016;25:610-7