心臓外科学(胸部外科学)
HEAD

LAB MEMBER
| 構成員名 | 役職 | 研究者総覧 |
|---|---|---|
| 櫻井 一 | 病院教授 | 研究者総覧 |
| 成田 裕司 | 准教授 | 研究者総覧 |
| 徳田 順之 | 病院准教授 | 研究者総覧 |
| 寺澤 幸枝 | 病院講師 | 研究者総覧 |
| 林 泰成 | 病院講師 | 研究者総覧 |
| 緒方 藍歌 | 助教 | 研究者総覧 |
CONTACT
| 病院 | 外来担当表 |
|---|---|
| HP | 心臓外科独自ホームページ ハートチームのページ |
OUTLINE
診療内容
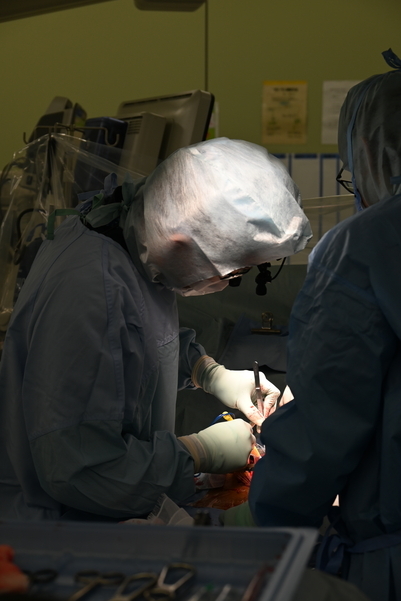
心臓外科学は心臓外科および胸部大血管外科を専門領域としています。名古屋大学心臓外科教室では冠動脈バイパス術などの虚血性心疾患手術、弁形成術・置換術などの心臓弁膜症に対する手術、大動脈弓部を中心とする胸部大血管手術など、後天性心疾患を中心に年間約300例以上の心臓・大血管手術 (心臓血管外科手術)を施行しています。名大病院 心臓外科独自ホームページはこちら
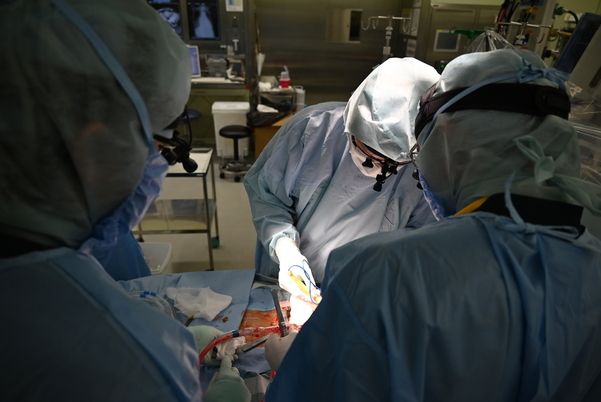
循環器内科と共同で、重症心不全治療センターを運用し、薬物治療,CRT等も組み合わせ難治性の心不全治療に取り組んでいます。心原性ショックに陥った重症患者さんなどの緊急搬送紹介なども多くお受けしています。重症心不全の外科治療として、植込型補助人工心臓治療、心臓移植治療を行っています。心臓移植に関しては中部地区唯一の実施施設です。
大動脈手術は大学病院としては全国有数の治療数を誇ります。難しい症例を含めて関連施設より多数の紹介を頂いています。開胸型の大動脈手術の他、血管外科教室と協力してステントグラフト内挿術(TEVAR)と、それと手術を組み合わせたハイブリッド治療を数多く行っています。名古屋大学附属病院は、循環器疾患だけを扱う単科病院ではありませんので、関連診療科のバックアップ体制は万全で、併存疾患を数多く抱えた患者さんでも安心して治療を受けることができます。術後回復を補助するため心臓大血管術後のリハビリテーションについても力をいれており、多くのスタッフを投入しています。これらについてはリハビリテーション領域でも高い評価を受けています。
SICDを含めた植込み型除細動器や、リードレスペースメーカーを含めたペースメーカー植込術の他、レーザーシースによるペースメーカー抜去術を行っております。循環器内科不整脈チームと共同し不整脈治療全般に対応し、加えて、従来難治性とされてきたペースメーカー感染の治療にも対応しています。ペースメーカー感染については県外など遠方からの紹介も多いです。
大動脈弁狭窄症に対する経カテーテル大動脈弁置換(TAVR TAVI)といった低侵襲治療にも取り組んでいます。従来であれば、併存疾患や高齢などの理由で治療が不可能とされていた患者さんにも治療の道が開かれた形となり、当院での治療例数も大きく増加しています。僧帽弁閉鎖不全症に対するMitraclip、心房中隔欠損症(ASD)や動脈管開存(PDA)に対するカテーテル閉鎖など、構造的心疾患(SHD)といわれる分野のカテーテル治療は、昨今急速展開している分野です。低侵襲治療TAVI ハートチームのページはこちら
このように、我々は、循環器病に罹患され心臓血管手術を必要とされる患者さんの個々の病状に応じて様々な治療選択肢を用意し、その方にとって最適な方法を選択できる診療体制をとっています。特に、循環器疾患(心臓血管の病気)以外のお病気も併せてお持ちの患者さんは、総合病院である当院での治療をお薦めします。
手術をさせていただいた患者さんの経過は詳細に記録し、常に検討を重ねています。その内容はNCDに基づいたデータベース化を行っています。それをもとに臨床研究を展開し手術成績の向上に努めています。
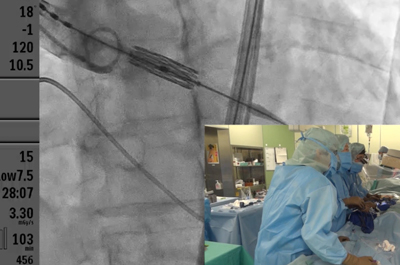
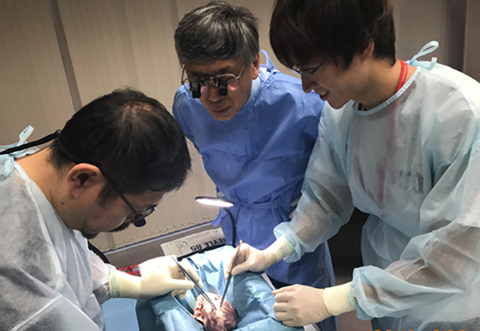
研究体制
心臓外科学は心臓外科および胸部大血管外科に関する基礎および臨床研究を専門領域としています。
教室には1952年に日本で初めて人工心肺を開発した歴史があり(戸田博教授)、この伝統を受け継ぎ、「臨床に即した研究」をモットーに研究に取り組んでいます。
再生医療を用いた大動脈瘤抑制療法の開発、不全心筋再生療法の開発、組織工学技法を用いた小口径人工血管の開発、心筋ネットを用いた心不全治療療法の開発などの臨床に即した基礎研究を行っています。
手術をさせていただいた患者さんの経過は詳細に記録し、日常的に検討を重ねています。その内容はNCDに基づいたデータベース化を行っています。それをもとに臨床研究を展開し手術成績の向上に努めています。
RESEARCH PROJECTS
臨床研究プロジェクト
心臓血管外科データベース事業 と 手術成績の検証
現在、わが国では病院医療の崩壊や医師の偏在が叫ばれ、多くの学会や団体が医療再建に向けて新たな提言や行動を行っていますが、どのような場所でどのような医療が行われているかが把握されていない状況では、良質な医療は提供できません。現状を把握することによって、医療のありかたを 根拠に基づいて検討し、社会に示していくことが重要であり、それにより最善の医療を提供することができます。そこでわが国では日本外科学会を基盤として、日本心臓血管外科学会、日本胸部外科学会、日本血管外科学会、日本呼吸器外科学会、日本消化器外科学会などの多くの各臨床学会が協働し、一般社団法人National Clinical Database(NCD)を立ち上げ、日本全国の外科系施設における外科症例の全体把握を目的としたデータベース事業を行っております。名古屋大学医学部附属病院では、NCD及び日本心臓血管外科手術データベース(JCVSD:Japan Cardiovascular Surgery Database)の趣旨に賛同し、この事業に参加しています。NCDは個人情報が特定されない形で運用され、我々が術前および術後の経過を検討するのに必要な様々な情報を記録しております。記録情報はNCDおよび、名古屋大学附属病院が管理する電子カルテと安全に隔絶された電子サーバーに記録されます。その趣旨を何卒ご理解の上、ご協力賜りますようよろしくお願い申し上げます。
NCDデータベース事業への参加について
私達は、一般社団法人National Clinical Database(NCD)が実施するデータベース事業に参加しています。
この事業は、日本全国の手術・治療情報を登録し、集計・分析することで医療の質の向上に役立て、患者さまに最善の医療を提供することを目指すプロジェクトです。
この法人における事業を通じて、患者さまにより適切な医療を提供するための医師の適正配置が検討できるだけでなく、当科が患者さまに最善の医療を提供するための参考となる情報を得ることができます。何卒趣旨をご理解の上、ご協力を賜りますよう宜しくお願い申し上げます。
1.NCDに登録する情報の内容
2011年1月1日以降、当科で行われた手術と治療に関する情報、手術や治療の効果やリスクを検証するための情報(年齢や身長、体重など)を登録します。NCDに患者さまのお名前を登録することはなく、氏名とは関係のないIDを用いて登録します。IDと患者さまを結びつける対応表は私達で厳重に管理し、NCDには提供しません。
2.登録する情報の管理・結果の公表
登録する情報は、それ自体で患者さま個人を容易に特定することはできないものですが、患者さまに関わる重要な情報ですので厳重に管理いたします。
私達及びNCDでは登録する情報の管理にあたって、情報の取り扱いや安全管理に関する法令や取り決め(「個人情報の保護に関する法律」、「人を対象とした医学系研究に関する倫理指針」、「医療・介護関係事業者における個人情報の適切な取扱いのためのガイダンス」、「医療情報システムの安全管理に関するガイドライン」等)を遵守しています。
データの公表にあたっては、NCDが承認した情報のみが集計データとして公表されます。登録するデータがどなたのものであるか特定されることはありません。
3.登録の拒否や登録情報の確認
データを登録されたくない場合は、登録を拒否して頂くことができます。スタッフにお伝えください。
また、登録されたご自身のデータの閲覧や削除を希望される場合も、スタッフにお知らせください。なお、登録を拒否されたり、閲覧・修正を希望されたりすることで、日常の診療等において患者さまが不利益を被ることは一切ございません。
4.NCD担当者の訪問による登録データ確認への協力
私達からNCDへ登録した情報が正しいかどうかを確認するため、NCDの担当者が患者さまのカルテや診療記録を閲覧することがあります。
私達がこの調査に協力する際は、NCDの担当者と守秘義務に関する取り決めを結び、患者さまとIDの対応表や氏名など患者さんを特定する情報を院外へ持ち出したり、口外したりすることは禁じます。
本研究に直接関係はしない第三者(企業監査担当者・厚生労働省)の人が、病院にあるあなたの記録(カルテなど)を見ることがあります。これらの人達は、法律上の守秘義務があり、あなたやあなたのご家族のプライバシーが外部に漏れる心配は一切ありません。又、登録された情報を基に、匿名化されたのち、学会や論文などで公表することや、海外学会との共同研究・規制当局・企業への報告に用いることもあります。
本事業への参加に関してご質問がある場合は、スタッフにお伝えください。また、より詳細な情報は下記に掲載されていますので、そちらもご覧ください。
一般社団法人National Clinical Database(NCD)ホームページ http://www.ncd.or.jp/
なお現在、本邦心臓血管外科学会が定める基幹施設は全施設がNCD JCVSDデータベース事業に参画しています。

心臓外科学教室における予後調査事業
- 胸部大動脈瘤患者さんの長期予後調査
- 弁膜症患者さんの長期予後調査
- 心臓大血管術後患者さんのADL(activity of daily life)調査
当院では、院内倫理委員会の了承のもと、上記疾患の患者さんの長期に渡る生活の質(QOL)の把握のための調査を行っております。これは質問紙法で、同意を頂いた方のみにお答えを頂く形で行っています。手術の後などに、患者さんがどのような生活を送っているのか、それをより良いものにするにはどのような改善が必要なのかを正確に把握するための調査です。一人でも多くの方が術後早く日常生活に復帰頂くためは状態把握が不可欠と考えております。質問紙への回答はご面倒かと思いますが、ご協力をお願いいたします。
拡張型心筋症に対するテイラーメイド方式 心臓形状矯正ネットの医師主導治験(jRCT2042210157)
名古屋大学医学部付属病院では日本医療研究開発機構(AMED)・橋渡し研究プログラム」の助成の下に、下記要領にて全国の5つの大学附属病院とともに、拡張型心筋症に対する開発中の医療機器である心臓(しんぞう)形状(けいじょう)矯正(きょうせい)ネットの効き目と安全性を調べるための臨床試験(治験)を行いました。名古屋大学3例と東北大学1例の組み入れがあり、術後24週の評価が完了し、現在術後5年までの観察研究に移行しています。
【治験の目的と内容】
左室拡張をきたした拡張型心筋症患者に対し、進行性の心拡大(=心臓リモデリング)を防止する目的で開発されたテイラーメイド方式心臓形状矯正ネットを心臓に装着し、術後24週での有効性・安全性を評価すること
【研究の背景】
特発性拡張型心筋症は進行性に心拡大と心機能低下が進む難病(指定難病57: https://www.nanbyou.or.jp/entry/3985)で、中等度以上の心不全症状を有する難病受給者証を有する患者は令和2年現在20,387人います。心不全が進行した場合は心移植以外に根治的療法はありませんが、極端なドナー不足のため毎年100名程度しか心移植は行われていないのが現状です。
原疾患を問わず心不全は進行性の心拡大(=心臓リモデリング)によって悪化していきます。メッシュ状の袋で心室を包み、物理的に防止しようという心臓サポートネット治療(Acorn CorCap)が欧米で試みられていました。このデバイスは壁の厚さが大きく異なる右心室と左心室を均等に包むため十分な効果を上げることができませんでした。私たちは心臓リモデリングが主として左心室に起こること、両心室を包むと右心室がネットと左心室に圧迫されて心拍出量が低下することを見いだしました。
特定臨床研究「拡張型心筋症に対するテイラーメイド方式心臓形状矯正ネットの臨床研究」の実施(jRCTs042180025)
先行品の問題点を改良した「テイラーメイド方式右室拘束軽減型心臓形状矯正ネット」を開発し、特定臨床研究「拡張型心筋症に対するテイラーメイド方式心臓形状矯正ネットの臨床研究」を3例の方に実施し、心臓リモデリングの防止効果だけでなく、運動能の大幅な改善が得られる結果を得ました。術後2年までは3名とも活動的な日常生活を享受され、2名は5年のフォローアップを終了しました。
AMED橋渡し研究の助成(令和4年~7年)の下に「拡張型心筋症に対するテイラーメイド方式心臓形状矯正ネットの医師主導治験」を全国5大学(名古屋大学、東京大学、大阪大学、東北大学、慈恵会医科大学)で実施し、名古屋大学3例、東北大学1例の組み入れがあり、募集は終了しました。術後24週の評価を終え、術後5年までの観察研究に移行しています。
【治験の内容】
対象疾患:非虚血性拡張型心筋症
目標症例数:5例
対象年齢:20歳~75歳
【選択基準】
1)本人の自由意思による治験参加の同意を文書で得た患者
2)同意取得時点で年齢が満20歳以上、75歳以下の患者
3)同意取得時点で心不全に対する3か月以上の最適な薬物内服治療(ACE阻害薬、ARB、利尿薬、β遮断薬、経口強心薬、SGLT2阻害薬、ARNI、HCNチャネル阻害薬など)にもかかわらず、心不全症状が持続し、現治療による症状改善が見込めない患者
4)NYHA分類がⅡmからⅣの患者及びINTERMACS ProfileのLevel 4~7の患者
5)心エコー検査で、LVEDD≧60 mm若しくはLVEDDi≧30 mm/m2の患者
6)心エコー検査で、LVEF≦35%の患者
7)心肺運動負荷試験で、Peak VO2が7.0~16.0 mL/kg/minの患者
8)治験機器製造のための心臓MRI検査又は造影心臓CT検査と心臓カテーテル検査が可能な患者
9)フォローアップ検査・観察に従う意思があり、実施医療機関に来院可能な患者
主要評価項目:安全性評価:手術から術後24週までの有害事象、治験機器の不具合
有効性評価:術後24週の運動耐容能(心肺運動負荷試験:Peak VO2)
副次評価項目:
1) 心機能改善及び左室リモデリング防止評価
2) 運動耐容能
3) 術後24週までの心臓関連イベント
連絡先:名古屋大学医学部心臓外科 秋田利明 :akita.toshiaki.j7◎f.mail.nagoya-u.ac.jp (送信の際は◎を@に変更してください)
外部リンク:
臨床研究等提出・公開システム:https://jrct.niph.go.jp/latest-detail/jRCT2042210157
治験機器製造元:(株)iCorNet研究所 https://www.icornet.jp
基礎研究プロジェクト
研究プロジェクト
重症心不全における心筋配向変化が心機能増悪をもたらす機序の解明
重症心不全における心筋配向変化が心機能増悪をもたらす機序の解明
(科学研究費基盤B)
【研究目的】
重症心不全における心筋配向の変化と乱れが心収縮能と拡張能・心臓リモデリングに及ぼす影響をMicro CTと心機能シミュレーション技術を用いて解析し、心不全悪化のメカニズムを力学的観点から明らかにすること
【研究背景】
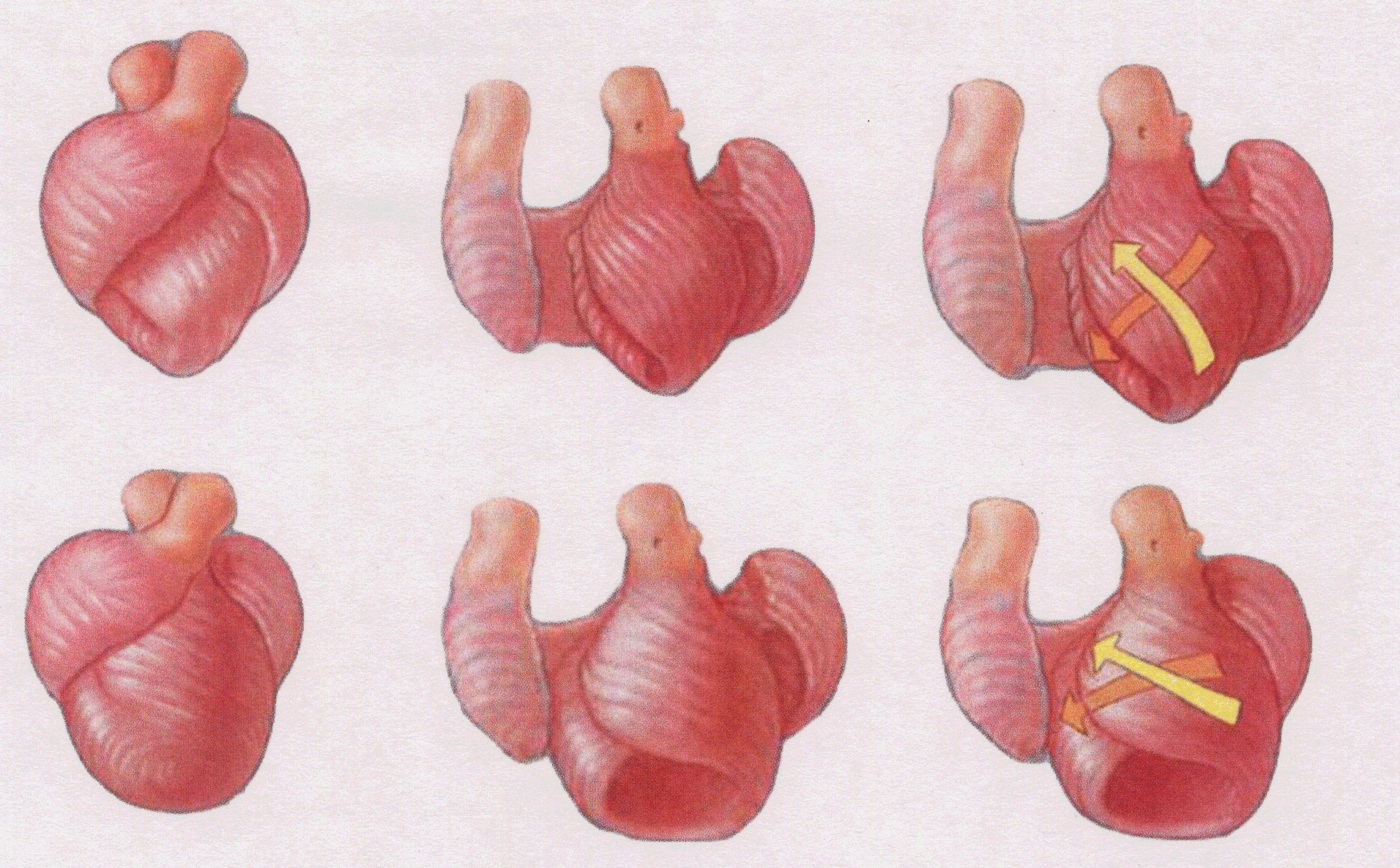
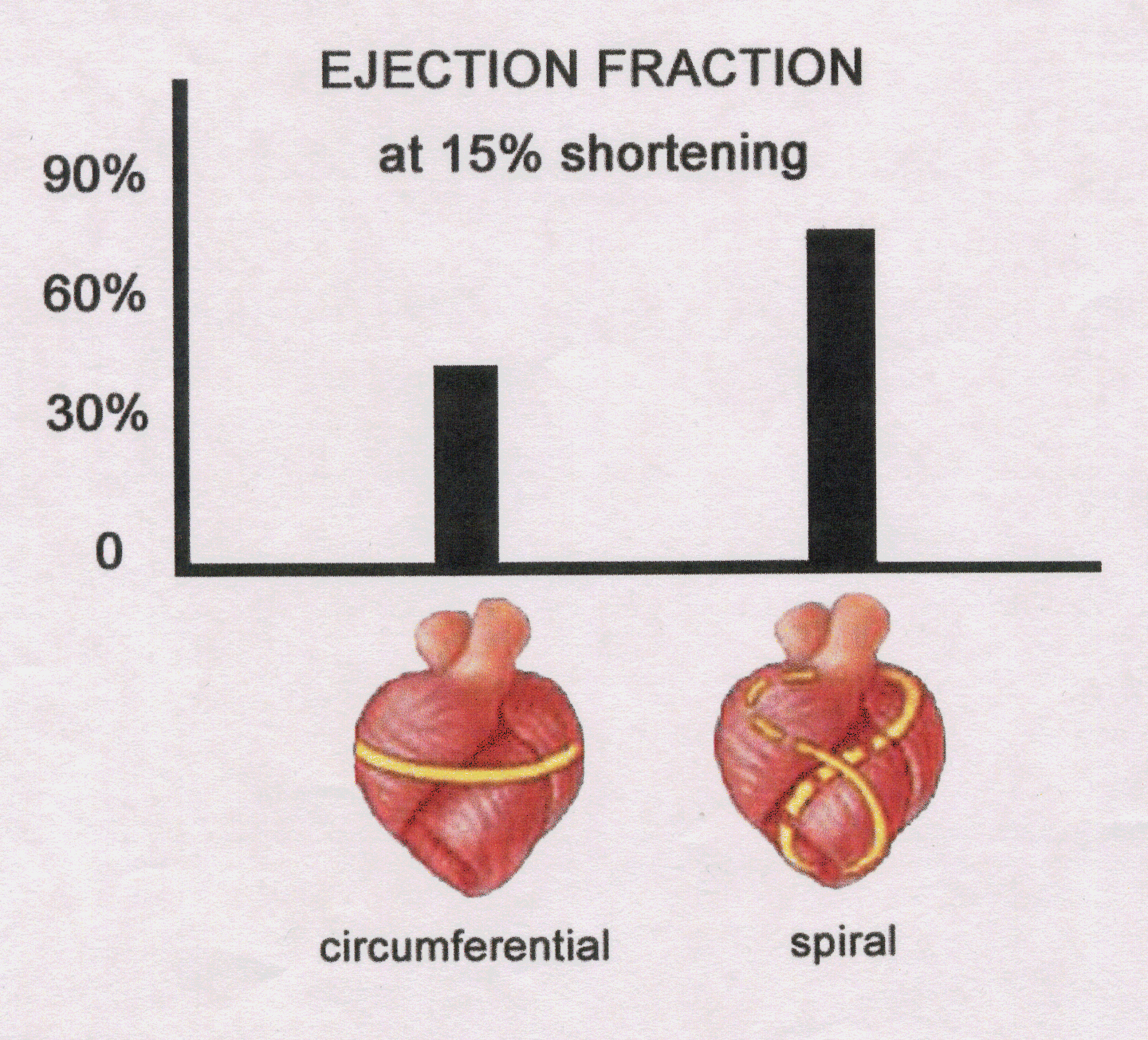
心不全が進行した心臓では、心形状が円錐形から球状化し、心筋配向がらせん構造から水平方向に傾き、さらに収縮効率が悪化する(図1)。さらに心筋シート(右図)の傾きは心室壁伸展に伴い、垂直方向に傾く。
【研究内容】
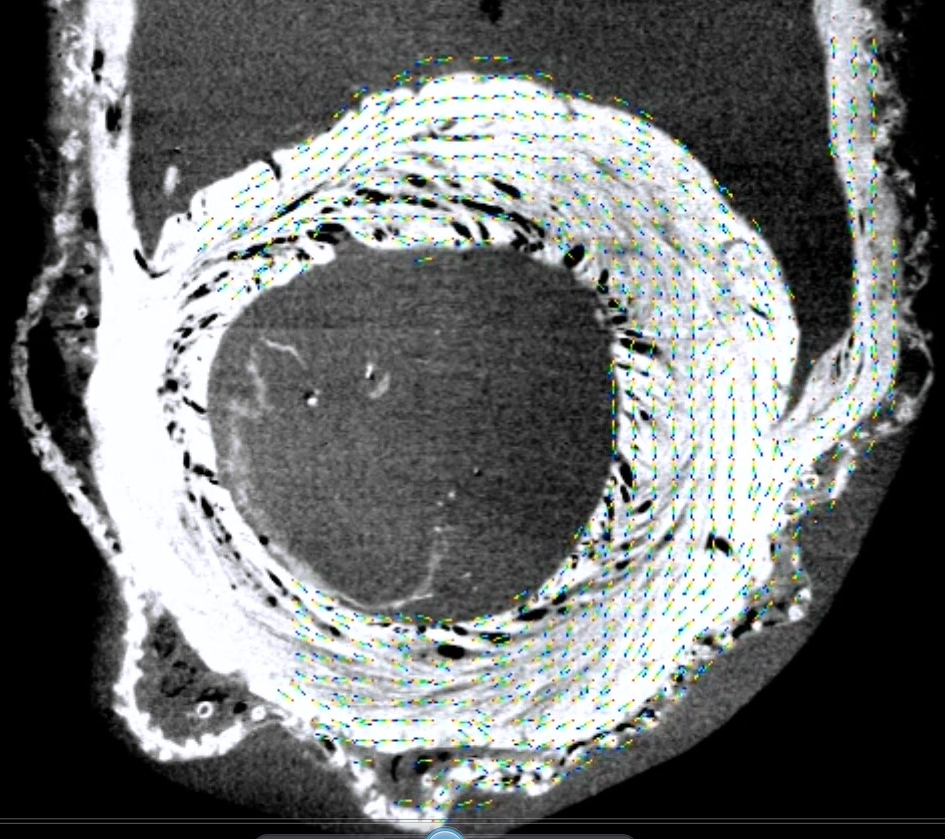
MicroCTを用いて正常心と不全心の心筋配向変化、心筋シートの傾きを評価する(名古屋大学工学部森健策教授研究室)。UT-Heart研究所の心臓シミュレーション技術に上記結果を組み込み、心機能(収縮能&拡張能)に与える影響を検討する。
 |
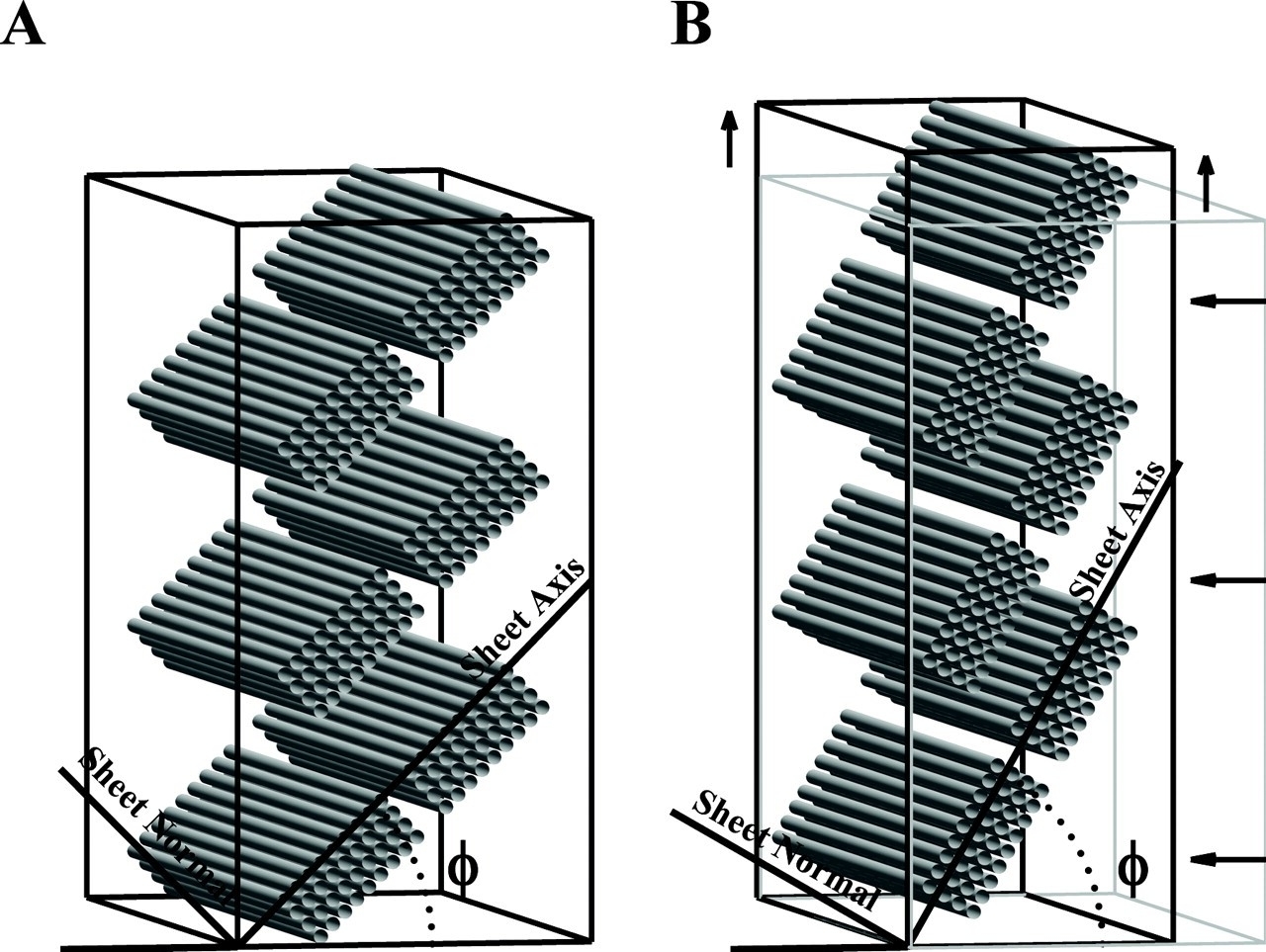 |
| 図1A. 正常心(上段:60°)と不全心(下段:30°)における心筋配向変化 | 図2A.Patrick A. Helm et al. Circulation Research. 2006;98:125-132earch. 2006;98:125-132 |
 |
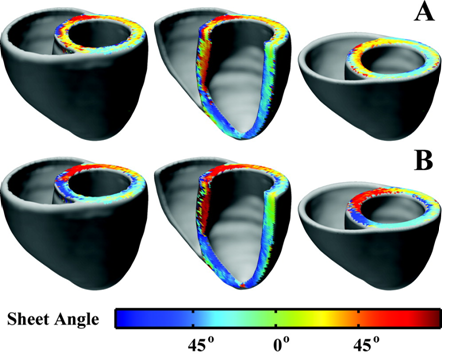 |
| 図1B.心筋配向がらせん構造から水平方向になった場合の左室駆出率変化(70%⇒40%) | 図2B |
 |
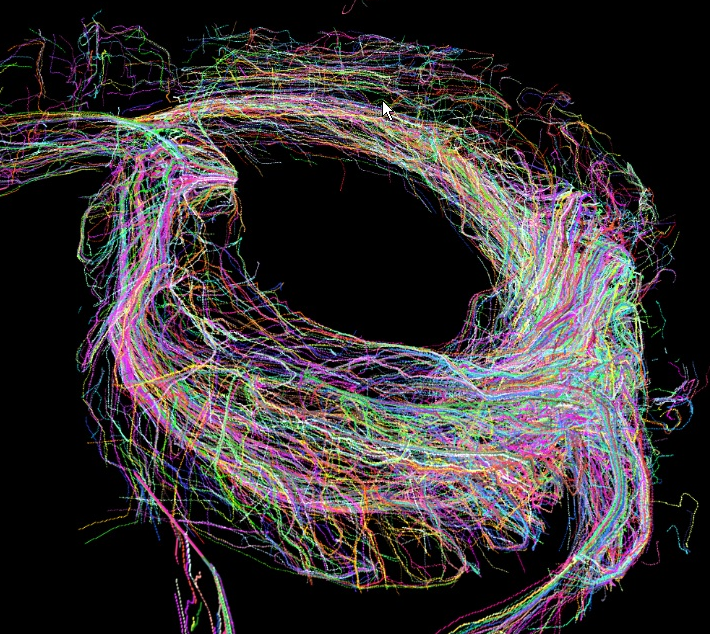 |
| 図9 microCT画像 | 図10.心筋配向ベクトル表示 |
研究プロジェクト 新しい大動脈瘤治療の開発
i) 間葉系幹細胞を用いた大動脈治療
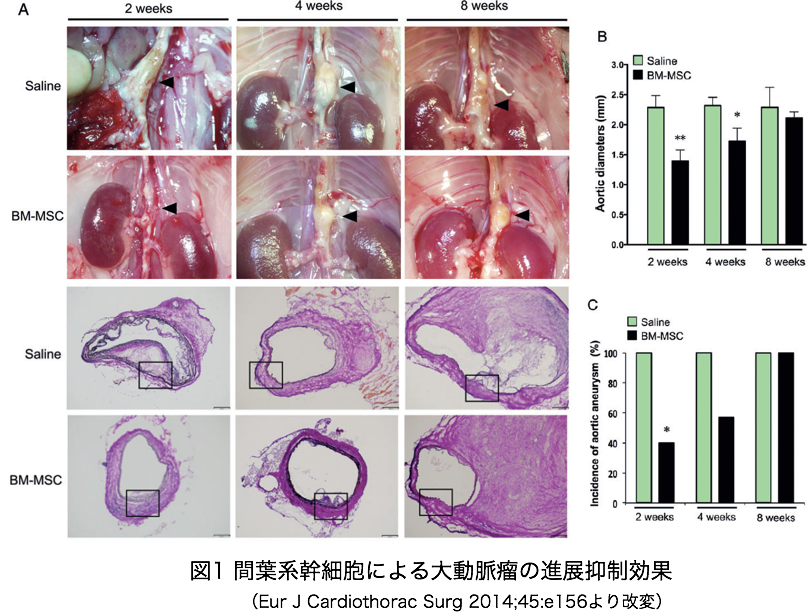
大動脈瘤の病態生理は、動脈硬化に伴う慢性炎症の成れの果てで、動脈張力・構造を維持する膠原線維の合成・分解のバランス破綻を来した結果、大動脈の組織強度を失い、瘤状に膨らんでしまう病態である。破裂すると救命率の低い、生命に直接関わる疾患である。手術(人工血管置換)が唯一の破裂予防法であるが、手術侵襲が大きく、合併症も多いため、リスクの高い患者では手術が困難な場合もある。従って、底侵襲治療が求められている。一方、間葉系幹細胞は、抗炎症作用、免疫抑制作用、組織修復作用があり、これらの作用を応用した、大動脈治療を考案した。大動脈瘤を局所投与、あるいは静脈投与することで、予防効果に加え、治療効果もあることを見出した。
J Vasc Surg 2011;54:1743, J Transl Med 2013;11:175, Eur J Cardiothorac Surg 2014;45:e156, World J Stem Cells 2014;6:278
ii) クラリスロマイシンを用いた大動脈瘤治療
クラリスロマイシンは膠原線維を分解する、マトリクスメタロプロテアーゼの分泌を阻害したり、抗炎症作用を有することがわかり、それらを利用した大動脈瘤治療では、大動脈瘤の破裂を抑制することがわかった。
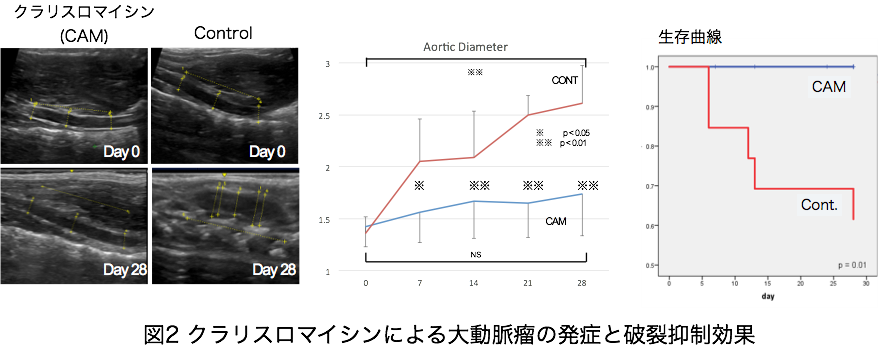
iii) エクソソームを用いた大動脈瘤治療
エクソソームとはほとんどすべての細胞が分泌する微細顆粒である。様々な蛋白、脂質、RNAを含み、様々な生理活性作用を有している。その生理活性作用は由来細胞に依存することがいわれている。そのエクソソームを間葉系幹細胞から単離し、大動脈瘤治療を行うと、治療効果を発現することを我々は世界で初めて発見した。
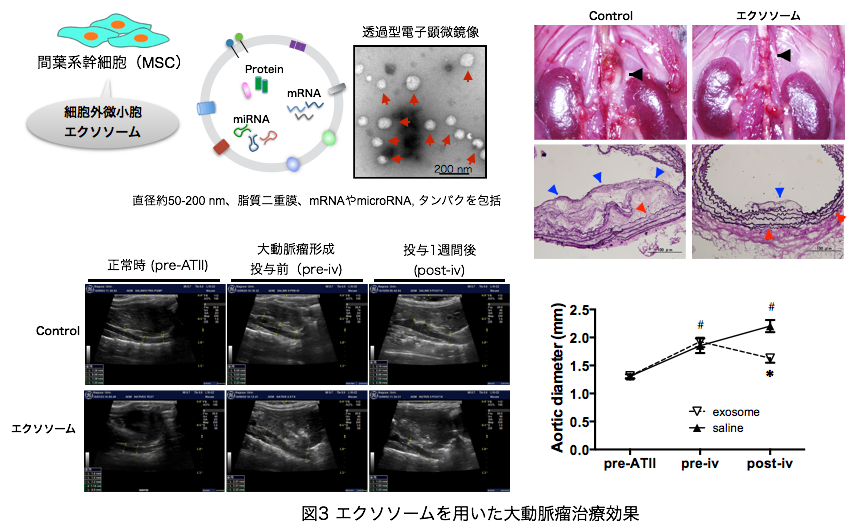
研究プロジェクト 再生医療技術を応用した手術材料の開発
i) 再生医療技術を利用した小口径人工血管の開発
市販の小口径人工血管は開存率が低く、現状では、心臓手術(冠動脈バイパス術等)に用いることは困難である。我々は、脱細胞化組織や生体吸収性材料を用いて、組織再生を人工血管自信がはかりながら自己血管のように再生する人工血管を開発している。
J Artif Organs 2012;15:399, Ann Thorac Surg 2012;93:156, J Artif Organs 2008;11:91
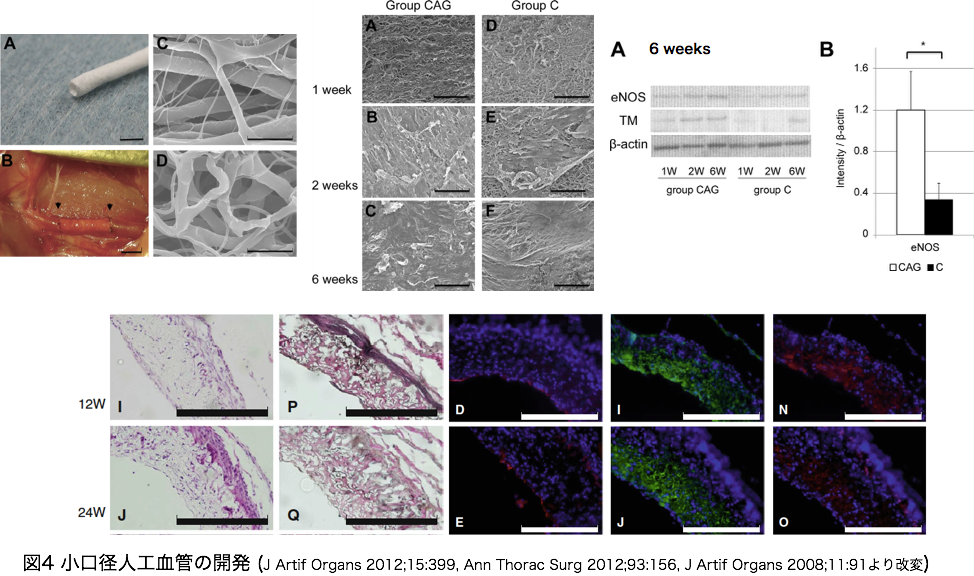
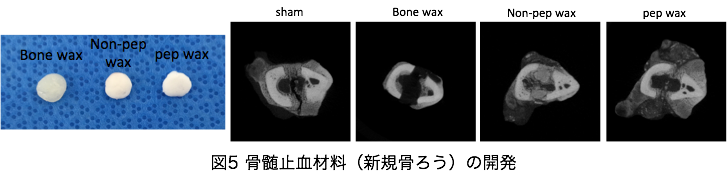
ii) 骨再生を促進する骨髄止血材料(新規骨ろう)の開発
手術等で骨を切開した場合、骨髄からの出血を制御しないと、失血し術野の操作に支障をきたす。この制御にはミツロウ(骨ろう)が使用されてきたが、感染を惹起したり、骨折治癒を抑制することがある。我々は、生体吸収性ポリマーにペプチドを配合し、ミツロウ同等の物性で、骨再生を促す材料を、他施設との共同研究で成功した。
iii) 組織再生を促す癒着防止膜の開発
心臓手術後の心臓周囲の癒着は、再手術時の剥離を困難にするだけでなく、癒着によって心臓機能も障害する。癒着を抑制する材料はいくつかあるが理想的とは言い難い。我々は、心臓を覆う心膜を再生させることで、癒着を防止するというコンセプトで、生体吸収性材料と心膜中皮細胞親和性の高いペプチドとを組み合わせることで、心膜再生を促す材料を開発している。
BIBLIOGRAPHY
2023
- Mutsuga M. Kyobu Geka. [Perioperative Management of Coagulation After the Weaning of Cardiopulmonary Bypass in Cardiac Surgery] 2023 Sep;76(10):824-828.
- Tobe A, Tanaka A, Tokuda Y, Shirai Y, Miyazaki T, Yuhara S, Akita S, Furusawa K, Ishii H, Mutsuga M, Murohara T Impact of Albuminuria on the Prognosis After Transcatheter Aortic Valve Implantation Am J Cardiol 186 156-162 2023
- Tobe A, Tanaka A, Tokuda Y, Shirai Y, Miyazaki T, Yuhara S, Akita S, Furusawa K, Ishii H, Mutsuga M, Murohara T Transcatheter aortic valve replacement for bicuspid aortic stenosis with a severely calcified raphe using an under-sized SAPIEN 3 valve: Sizing by the circle method and deployment by the pressure-regulated method Cardiovasc Revasc Med 2023
- Oishi H, Morimoto R, Ito R, Kazama S, Kimura Y, Araki T, Mizutani T, Kuwayama T, Hiraiwa H, Kondo T, Okumura T, Mutsuga M, Usui A, Murohara T Increased risk of purge system malfunction after Impella 5.0 replacement: a case series J Artif Organs 26(1) 79-83 2023
- Tsuchikawa Y, Tokuda Y, Ito H, Shimizu M, Tanaka S, Nishida K, Takagi D, Fukuta A, Takeda N, Yamamoto H, Hori M, Nishida Y, Mutsuga M Impact of Early Ambulation on the Prognosis of Coronary Artery Bypass Grafting Patients Circ J 87(2) 306-311 2023
- Mutsuga M, Okumura T, Morimoto R, Kondo T, Ito H, Terazawa S, Tokuda Y, Narita Y, Nishida K, Murohara T, Usui A Impact of an improved driveline management for HeartMate II and HeartMate 3 left ventricular assist devices Artif Organs 47(2) 387-395 2023
- Sakurai H,Nonaka T,Sakurai T,Okawa H Rapid two-stage Norwood procedure using an auto-pericardial patch fixed with an arch-shaped mold Operative techniques in thoracic and cardiovascular surgery In Press 2023
- Yamawaki-Ogata A, Mutsuga M, Narita Y. A review of current status of cell-based therapies for aortic aneurysms.Inflamm Regen. 2023 Aug 7;43(1):40
- Ashida S, Yamawaki-Ogata A, Tokoro M, Mutsuga M, Usui A, Narita Y. Administration of anti-inflammatory M2 macrophages suppresses progression of angiotensin II-induced aortic aneurysm in mice. Sci Rep. 2023 Jan 25;13(1):1380.
- Tobe A, Tanaka A, Tokuda Y, Shirai Y, Miyazaki T, Yuhara S, Akita S, Furusawa K, Ishii H, Mutsuga M, Murohara T.Impact of Albuminuria on the Prognosis After Transcatheter Aortic Valve Implantation. Am J Cardiol. 2023 Jan 1;186:156-162.
- Mutsuga M, Okumura T, Morimoto R, Kondo T, Ito H, Terazawa S, Tokuda Y, Narita Y, Nishida K, Murohara T, Usui A. Impact of an improved driveline management for HeartMate II and HeartMate 3 left ventricular assist devices. Artif Organs. 2023 Feb;47(2):387-395.
- Osawa T, Schaeffer T, Borgmann K, Schmiel M, Staehler H, Di Padua C, Heinisch PP, Piber N, Mutsuga M, Hager A, Ewert P, Hörer J, Ono M. Impact of aortopulmonary collaterals on adverse events after total cavopulmonary connection. Eur J Cardiothorac Surg. 2023 Dec 1;64(6)
- Ohno T, Mutsuga M, Saito S, Tokuda Y, Nagai K, Umemoto N, Abe T, Usui A. Incidence and clinical impact of silent pancreatitis after aortic arch surgery. Asian Cardiovasc Thorac Ann. 2023 May;31(4):303-311.
- Tokuda Y, Terazawa S, Yoshizumi T, Ito H, Banno H, Mutsuga M. Hybrid Repair of Extensive Aortic Arch Aneurysms: Outcomes of Isolated Frozen Elephant Trunk Repair and of Elephant Trunk with Second Stage Thoracic Endovascular Aortic Repair. Eur J Vasc Endovasc Surg. 2023 Aug;66(2):284-285.
- Nishi T, Fujimoto KL, Hiramatsu M, Okada T, Suzuki Y, Shimoyama Y, Terazawa S, Tokuda Y, Mutsuga M, Usui A. Surgical reconstruction after resection of cardiac metastasis from oropharyngeal carcinoma: a case report. Nagoya J Med Sci. 2023 Nov;85(4):875-879.
- Takahiro Tamura, Shogo Suzuki, Tasuku Fujii, Takahiro Hirai, Takahiro Imaizumi, Yoko Kubo, Yasuyuki Shibata, Yuji Narita, Masato Mutsuga, Kimitoshi Nishiwaki Thromboelastographic evaluation after cardiac surgery optimizes transfusion requirements in the intensive care unit: a single-center retrospective cohort study using an inverse probability weighting method PGen Thorac Cardiovasc Surg. 2024 Jan;72(1):15-23. doi: 10.1007/s11748-023-01941-8. Epub 2023 May 12.
- Kiyonori Kobayashi, Toshiaki Akita, Sho Akita, Hideki Ito, Sachie Terazawa, Masato Mutsuga, Akihiko Usui Cardiac rehabilitation in a heart-failure patient using customized \"cardiac support net\" treatment: a case report Nagoya J Med Sci. 2023 Aug;85(3):626-634.
- Miho Shimizu , Hiroaki Hiraiwa, Shinya Tanaka, Yohei Tsuchikawa, Ryota Ito,Shingo Kazama, Yuki Kimura, Takashi Araki, Takashi Mizutani, Hideo Oishi, Tasuku Kuwayama, Toru Kondo, Ryota Morimoto, Takahiro Okumura, Hideki Ito, Tomo Yoshizumi, Masato Mutsuga, Akihiko Usui, Toyoaki Murohara Cardiac Rehabilitation in Severe Heart Failure Patients with Impella 5.0 Support via the Subclavian Artery Approach Prior to Left Ventricular Assist Device Implantation J Pers Med. 2023 Apr 3;13(4):630
- Shota Nakamura, Harushi Ueno, Masato Mutsuga ,Toyofumi F Chen-Yoshikawa Cadaver surgical training for brain-dead donor lung procurement: Educational note JTCVS Tech. 2023 Aug 11:21:261-264.
- Yusuke Miki, Akihito Tanaka, Yoshiyuki Tokuda, Akihiro Tobe , Yoshinori Shirai, Satoshi Yuhara , Sho Akita, Kenji Furusawa, Hideki Ishii, Masato Mutsuga, Toyoaki Murohara Clinical implications of the cardio-ankle vascular index before and after transcatheter aortic valve implantation J Cardiovasc Med (Hagerstown). 2023 May 1;24(5):302-307.
- Ryota Morimoto, Ryota Ito, Takashi Araki, Takashi Mizutani, Yuki Kimura, Shingo Kazama, Hideo Oishi, Tasuku Kuwayama, Yuki Sugiura, Hiroaki Hiraiwa, Toru Kondo, Takahiro Okumura, Koichi Kobayashi, Masato Mutsuga, Toyoaki Murohara Contractile pericarditis-like hemodynamics in dilated-phase hypertrophic cardiomyopathy with giant atrium J Cardiol Cases. 2023 Feb 9;27(5):199-202
- Tsukasa Ohno, Hiroto Suenaga, Aika Yamawaki-Ogata, Kei Kanie, Ryuji Kato, Koichiro Uto, Mitsuhiro Ebara, Hideki Ito, Yuji Narita, Akihiko Usui, Masato Mutsuga Development of novel waxy bone haemostatic agents composed of biodegradable polymers with osteogenic-enhancing peptides in rabbit models Interdiscip Cardiovasc Thorac Surg. 2023 Nov 2;37(5):ivad170
- Miho Shimizu , Takuji Adachi, Kiyonori Kobayashi,Masato Mutsuga, Hideki Oshima, Akihiko Usui, Sumio Yamada Factors associated with postsurgical muscle weakness in patients who undergo thoracic aortic surgery: a retrospective cohort study Physiother Theory Pract. 2023 Oct 3;39(10):2180-2188
2022
- Mutsuga M. Kyobu Geka. [Traumatic Thoracic Aortic Injury] 2022 Sep;75(10):759-762.
- Mutsuga M, Chen-Yoshikawa TF. J Thorac Cardiovasc Surg. Commentary: Continuous steady development is made by taking 2 steps forward, 1 step back. 2022 Aug;164(2):539-540.
- Ishida S, Mutsuga M, Fujita T, Yagami K. Circ Rep. Lateralized Purplish Skin Discoloration Due to Aortic Dissection. 2022 Jun 3;4(7):332.
- Ishida S, Mutsuga M, Fujita T, Yagami K. Gen Thorac Cardiovasc Surg. Late detection of communication between juxtaposed atrial appendages. 2022 Feb;70(2):190-192.
- Usui A, Mutsuga M. Ann Thorac Cardiovasc Surg. Surgical Management for Systolic Anterior Motion (SAM) of the Mitral Valve in Obstructive Hypertrophic Myopathy. 2022 Aug 20;28(4):239-248.
- Ishida S, Mutsuga M, Fujita T, Yagami K. J Surg Case Rep. Late-phase left ventricular pseudoaneurysm after three-time mitral valve surgery. 2022 Jan 20;2022(1):rjab602.
- Usui R, Mutsuga M, Yoshizumi T, Oshima H, Usui A. Ann Thorac Surg. A Surgical Case for Pregnancy-Related Spontaneous Coronary Artery Dissection. 2022 Feb;113(2):e115-e117.
- Mutsuga M, Narita Y, Tokuda Y, Uchida W, Ito H, Terazawa S, Nakaguro M, Usui A. Ann Thorac Surg. Predictors of Failure of Mitral Valve Repair Using Artificial Chordae. 2022 Apr;113(4):1136-1143.
- Mutsuga M, Banno H, Okumura T, Morimoto R, Kondo T, Kimura Y, Hiraiwa H, Murohara T, Usui A. Heart Lung Circ. Impella5.0 \"ILIPELLA\" Approach for a Fulminant Myocarditis Patient With a Small Peripheral Artery. 2022 May;31(5):e72-e74.
- Kozakai M, Narita Y, Yamawaki-Ogata A, Fujimoto KL, Mutsuga M, Tokuda Y, Usui A. Expert Opin Biol Ther. Alternative therapeutic strategy for existing aortic aneurysms using mesenchymal stem cell-derived exosomes. 2022 Jan;22(1):95-104.
- Ishida S, Mutsuga M, Fujita T, Yagami K. Indian J Thorac Cardiovasc Surg. Plaster technique for filling up a future entry at the suture hole in type A aortic dissection. 2022 May;38(3):339-341.
- Hiraiwa H, Kimura Y, Morimoto R, Ito R, Araki T, Mizutani T, Kazama S, Oishi H, Kuwayama T, Kondo T, Furusawa K, Okumura T, Mutsuga M, Usui A, Murohara T. J Artif Organs. Flexion limitation of the Impella 5.0 when implanted using the femoral approach in patients with small stature. 2022 Jun;25(2):182-183.
- Kobayashi K, Mutsuga M, Usui A. Sci Rep. Relationship between muscle strength and rehospitalization in ventricular assist device patients. 2022 Jan 7;12(1):50.
- Usui R, Mutsuga M, Narita Y, Tokuda Y, Terazawa S, Ito H, Uchida W, Inden Y, Murohara T, Usui A. Gen Thorac Cardiovasc Surg. Higher F-wave frequency associates with poor procedural success rate after Maze procedure. 2022 Dec;70(12):997-1004.
- Tobe A, Tanaka A, Tokuda Y, Shirai Y, Miyazaki T, Yuhara S, Akita S, Furusawa K, Ishii H, Mutsuga M, Murohara T. Am J Cardiol. Impact of Albuminuria on the Prognosis After Transcatheter Aortic Valve Implantation. 2023 Jan 1;186:156-162.
- Morita K, Mutsuga M, Uchida W, Usui A. J Card Surg. Effectiveness of the scheduled transfusion strategy for factor V deficiency with platelet dysfunction during coronary artery surgery. 2022 Dec;37(12):5493-5495.
- Fujii T, Mutsuga M, Narita Y, Tokuda Y, Terazawa S, Ito H, Uchida W, Yuhara S, Usui A. SAGE Open Med Case Rep. Multiple giant coronary artery aneurysms with extended coronary ectasia emerging 12 years after previous coronary artery bypass grafting. 2022 Aug 5;10:2050313X221116681.
- Shimizu M, Adachi T, Kobayashi K, Mutsuga M, Oshima H, Usui A, Yamada S. Physiother Theory Pract. Factors associated with postsurgical muscle weakness in patients who undergo thoracic aortic surgery: a retrospective cohort study. 2022 May 23:1-9.
- Ishida S, Mutsuga M, Fujita T, Yagami K. J Cardiol Cases. Surgical techniques for infectious endocarditis of the mitral valve with hypertrophic cardiomyopathy in Costello syndrome. 2022 Jan 14;25(6):367-369.
- Tobe A, Tanaka A, Tokuda Y, Shirai Y, Miyazaki T, Yuhara S, Akita S, Furusawa K, Ishii H, Mutsuga M, Murohara T. Cardiovasc Revasc Med. Transcatheter aortic valve replacement for bicuspid aortic stenosis with a severely calcified raphe using an under-sized SAPIEN 3 valve: Sizing by the circle method and deployment by the pressure-regulated method. 2022 Aug 22:S1553-8389(22)00726-6.
- Ozaki A, Kishi E, Ooshima T, Kakutani N, Abe Y, Mutsuga M, Yamaguchi Y, Yamano T. Food Chem. Determination of potential volatile compounds in polyethylene terephthalate (PET) bottles and their short- and long-term migration into food simulants and soft drink. 2022 Dec 15;397:133758.
- Oishi H, Morimoto R, Ito R, Kazama S, Kimura Y, Araki T, Mizutani T, Kuwayama T, Hiraiwa H, Kondo T, Okumura T, Mutsuga M, Usui A, Murohara T. J Artif Organs. HYPERLINK \"https://pubmed.ncbi.nlm.nih.gov/35575950/\"Increased risk of purge system malfunction after Impella 5.0 replacement: a case series. 2023 Mar;26(1):79-83.
- Tsuchikawa Y, Tokuda Y, Ito H, Shimizu M, Tanaka S, Nishida K, Takagi D, Fukuta A, Takeda N, Yamamoto H, Hori M, Nishida Y, Mutsuga M. Circ J. Impact of Early Ambulation on the Prognosis of Coronary Artery Bypass Grafting Patients. 2023 Jan 25;87(2):306-311.
- Hiraiwa H, Okumura T, Sawamura A, Araki T, Mizutani T, Kazama S, Kimura Y, Shibata N, Oishi H, Kuwayama T, Kondo T, Furusawa K, Morimoto R, Adachi T, Yamada S, Mutsuga M, Usui A, Murohara T. BMC Res Notes. Relationship between spleen size and exercise tolerance in advanced heart failure patients with a left ventricular assist device. 2022 Feb 10;15(1):40.
- Mutsuga M, Okumura T, Morimoto R, Kondo T, Ito H, Terazawa S, Tokuda Y, Narita Y, Nishida K, Murohara T, Usui A. Artif Organs. Impact of an improved driveline management for HeartMate II and HeartMate 3 left ventricular assist devices. 2023 Feb;47(2):387-395.
- Oishi H, Kondo T, Kawamura M, Shimada K, Mutsuga M, Kurokawa T, Kuwayama T, Hiraiwa H, Morimoto R, Okumura T, Nishida T, Kiyoi H, Naganawa S, Usui A, Murohara T. J Artif Organs. Methods for confirming the safety of radiation therapy in patients with left ventricular assist device: a case of extranodal NK/T-cell lymphoma, nasal type. 2022 Sep;25(3):274-278.
- Tobe A, Tanaka A,Tokuda Y, Shirai Y, Otsuka S, Yamamoto T, Tokoro M, Furusawa K, Ishii H, Usui A, Murohara T. Cardiovasc Revasc Med. Albuminuria Predicts Short-Term Worsening Renal Function After Transcatheter Aortic Valve Replacement. 2022 Sep;42:178-181.
- Tobe A, Tanaka A,Tokuda Y, Fujii T, Furusawa K, Ishii H, Usui A, Murohara T. J Cardiol. 2022 May;79(5):648-654. Albuminuria predicts worsening renal function after transcatheter aortic valve replacement.
- Yano D, Yokoyama Y,Tokuda Y, Kato M, Mashiko Y, Kuwabara F, Ebata T, Usui A. Surg Today. Multidisciplinary surgical approach for renal cell carcinoma with inferior vena cava tumor thrombus. 2022 Jul;52(7):1016-1022.
- Shirai Y, Tanaka A,Tokuda Y, Tobe A, Furusawa K, Usui A, Murohara T. J Card Surg. Large interventricular membranous septal aneurysm renders the anatomy unsuitable for transcatheter aortic valve replacement. 2022 Jul;37(7):2103-2104.
- Koyanagi H, Tsutsumi Y,Tokuda Y, Tanaka A, Endo M, Furukawa Y, Abe S. Heart Vessels. Computed tomography imaging using split-bolus contrast injection with volume scan of aortic root and heart for preoperative evaluation of transcatheter aortic valve implantation. 2022 Jan;37(1):132-141.
- Wang Y, Kanie K, Takezawa T, Horikawa M, Kaneko K, Sugimoto A, Yamawaki-Ogata A,Narita Y, Kato R. Carbohydr Polym. Bi-layered carboxymethyl cellulose-collagen vitrigel dual-surface adhesion-prevention membrane. 2022 Jun 1;285:119223.
2021
- Fujimoto K,Yamawaki-Ogata A,Uto K,Usui A,Narita Y,Ebara M Long term efficacy and fate of a right ventricular outflow tract replacement using an elastomeric cardiac patch consisting of caprolactone and D,L-lactide copolymers Acta Biomaterialia 2021;123:222-9
- Tokuda Y,Fujimoto K,Narita Y,Mutsuga M,Usui A Sutures on the Anterior Mitral Leaflet to Prevent Systolic Anterior Motion Ann Thorac Surg 2021;111:213-5
- Mutsuga M,Tokuda Y,Fujimoto K,Terazawa S,Ito H,Narita Y,Usui A Surgery for Anomalous Papillary Muscle Directly Into the Anterior Mitral Leaflet Ann Thorac Surg 2021;111:1512-8
- Akita N,Narita Y,Yamawaki-Ogata A,Usui A,Komori K Therapeutic effect of allogeneic bone marrow-derived mesenchymal stromal cells on aortic aneurysms Cell Tissue Res 2021;383:781-93
- Mutsuga M,Usui A Beating heart left ventricle thrombectomy through mini-left-anterior thoracotomy for a patient with cardiogenic shock Gen Thorac Cardiovasc Surg 2021;69:614-7
- Usui R,Mutsuga M,Yoshizumi T,Oshima H,Eda T,Usui A Do meteorological factors influence the occurrence of acute aortic dissection? A 10-year retrospective institutional study Gen Thorac Cardiovasc Surg 2021;69:654-61
- Nishi T,Mutsuga M,Akita T,Narita Y,Fujimoto K,Tokuda Y,Nishida K,Matsui S,Nishiwaki K,Usui A Hypofibrinogenemia can be estimated by the predictive formula in aortic surgery Gen Thorac Cardiovasc Surg 2021;69:1376-82
- Mutsuga M,Tokuda Y,Narita Y,Terazawa S,Ito H,Usui A Is Hybrid Repair for an Entire Shaggy Aorta Feasible ? Heart Lung Circ 2021;30:765-72
- Mutsuga M,Banno H,Tokuda Y,Usui A Beating-heart total arch replacement for an octogenarian patient with severe heart failure J Card Surg 2021;36:1126-9
- Usui R,Mutsuga M,Narita Y,Tokuda Y,Terazawa S,Ito H,Uchida W,Usui A Sudden circulatory collapse caused by mechanical obstruction of the left main coronary trunk with infective endocarditis vegetation: a case report Surg Case Rep 2021;7:223
2020
- Nishi T, Tokuda Y, Tanaka A, Furusawa K, Miki Y, Tobe A, Murohara T, Usui A:Cholesterol Crystal Embolization After Transcatheter Aortic Valve Replacement.Circ Rep. 2020 Oct 7;2(11):701-702. doi: 10.1253/circrep.CR-20-0060.
- Yamamoto T, Mutsuga M, Matsuura A, Miyahara K, Takemura H, Saito S, Otsuka R, Usui A:Long-term outcome 10 years after free gastroepiploic artery graft for coronary artery bypass surgery.Ann Thorac Surg. 2020 Dec 24:S0003-4975(20)32166-4. doi: 10.1016/j.athoracsur.2020.09.080.
- Mutsuga M, Banno H, Narita Y, Komori K, Usui A:<Editors' Choice> Which is superior, the frozen elephant trunk technique alone or the classical elephant trunk technique followed by second-stage thoracic endovascular aortic repair for extensive aortic arch repair?Nagoya J Med Sci. 2020 Nov;82(4):657-666. doi: 10.18999/nagjms.82.4.657.
- Mutsuga M, Narita Y, Usui A:Mid-term results of Biological Bentall using a larger valve implantation technique.Nagoya J Med Sci. 2020 Nov;82(4):645-655. doi: 10.18999/nagjms.82.4.645.
- Tobe A, Tanaka A, Tokuda Y, Akita S, Miki Y, Furusawa K, Ishii H, Usui A, Murohara T:Serial Images of Aortic Plaque Rupture During Transfemoral Transcatheter Aortic Valve Replacement.JACC Cardiovasc Interv. 2020 Nov 23;13(22):e203-e204. doi: 10.1016/j.jcin.2020.09.007.
- Kuroda T, Mutsuga M, Yamada M, Yamakawa M, Yuhara S, Hasegawa H, Yokote J, Yokoyama Y, Yamada T, Koyama T, Usui A:Efficacy of Plasma free Hemoglobin for detecting centrifugal pump thrombosis.Perfusion. 2020 Sep 10:267659120957183. doi: 10.1177/0267659120957183.
- Kimura Y, Kondo T, Mutsuga M, Morimoto R, Kazama S, Shibata N, Oishi H, Arao Y, Kuwayama T, Kato H, Yamaguchi S, Hiraiwa H, Okumura T, Fujimoto K, Usui A, Murohara T:Impella 5.0 for Cardiogenic Shock After Thrombectomy in a Patient With Intraventricular Thrombosis.Can J Cardiol. 2020 Oct;36(10):1690.e13-1690.e15. doi: 10.1016/j.cjca.2020.04.005.
- Mutsuga M, Ito H, Usui A:Exclusion Technique for Entire Shaggy Aorta Followed by One-Stage Repair of the Aortic Arch and Descending Aorta.Heart Lung Circ. 2020 Nov;29(11):e269-e272. doi: 10.1016/j.hlc.2020.06.016.
- Oishi H, Kondo T, Fujimoto K, Mutsuga M, Morimoto R, Hirano KI, Sawamura A, Kazama S, Kimura Y, Shibata N, Kato H, Arao Y, Kuwayama T, Yamaguchi S, Hiraiwa H, Okumura T, Usui A, Murohara T:Aortic insufficiency associated with Impella that required surgical intervention upon implantation of the durable left ventricular assist device.J Artif Organs. 2020 Dec;23(4):378-382. doi: 10.1007/s10047-020-01184-x.
- Tokuda Y, Usui A:Management of Patients With Aortic Stenosis Requiring Non-Cardiac Surgery.Circ J. 2020 Jun 25;84(7):1064-1066. doi: 10.1253/circj.CJ-20-0437.
- Mashiko Y, Abe T, Tokuda Y, Oshima H, Usui A:Correction to: Extracorporeal membrane oxygenation support for postcardiotomy cardiogenic shock in adult patients: predictors of in‑hospital mortality and failure to be weaned from extracorporeal membrane oxygenation.J Artif Organs. 2020 Sep;23(3):233. doi: 10.1007/s10047-020-01171-2.
- Ito H, Mutsuga M, Tokuda Y, Usui A:Upper thoracoabdominal aortic repair through partial posterior incision of the diaphragm via left thoracotomy.Gen Thorac Cardiovasc Surg. 2020 Dec;68(12):1594-1595. doi: 10.1007/s11748-020-01387-2.
- Hiraiwa H, Okumura T, Shimizu S, Arao Y, Oishi H, Kato H, Kuwayama T, Yamaguchi S, Haga T, Yokoi T, Kondo T, Sugiura Y, Kano N, Watanabe N, Fukaya K, Furusawa K, Sawamura A, Morimoto R, Fujimoto K, Mutsuga M, Usui A, Murohara T:Pathological changes of the myocardium in reworsening of anthracycline-induced cardiomyopathy after explant of a left ventricular assist device.Nagoya J Med Sci. 2020 Feb;82(1):129-134. doi: 10.18999/nagjms.82.1.129.
- Mashiko Y, Abe T, Tokuda Y, Oshima H, Usui A:Extracorporeal membrane oxygenation support for postcardiotomy cardiogenic shock in adult patients: predictors of in-hospital mortality and failure to be weaned from extracorporeal membrane oxygenation.J Artif Organs. 2020 Sep;23(3):225-232. doi: 10.1007/s10047-020-01160-5.
- Ito H, Mutsuga M, Tokuda Y, Usui A:Modified sutureless repair using left atrial appendage flap for acquired left-sided pulmonary vein stenosis.Eur J Cardiothorac Surg. 2020 Aug 1;58(2):395-397. doi: 10.1093/ejcts/ezaa032.
- Tokuda Y, Yamamoto H, Miyata H, Usui A, Motomura N:Contemporary Outcomes of Surgical Aortic Valve Replacement in Japan.Circ J. 2020 Jan 24;84(2):277-282. doi: 10.1253/circj.CJ-19-0674.
- Tokoro M, Sawaki S, Ozeki T, Orii M, Usui A, Ito T:Totally endoscopic aortic valve replacement via an anterolateral approach using a standard prosthesis.Interact Cardiovasc Thorac Surg. 2020 Mar 1;30(3):424-430. doi: 10.1093/icvts/ivz287.
- Munakata H, Tajima K, Kato W, Tanaka K, Tokuda Y, Mutsuga M, Usui A:Bilateral versus single internal thoracic artery grafting in hemodialysis patients.Gen Thorac Cardiovasc Surg. 2020 Aug;68(8):768-773. doi: 10.1007/s11748-019-01254-9.
- Nishi T, Mutsuga M, Akita T, Narita Y, Fujimoto K, Tokuda Y, Terazawa S, Ito H, Nishiwaki K, Usui A:The incidence and risk factors of hypofibrinogenemia in cardiovascular surgery.Gen Thorac Cardiovasc Surg. 2020 Apr;68(4):335-341. doi: 10.1007/s11748-019-01201-8.
- Mutsuga M, Narita Y, Usui A:A Floating Stitch on the Anterior Mitral Leaflet Can Eliminate Systolic Anterior Motion in Hypertrophic Obstructive Cardiomyopathy.Semin Thorac Cardiovasc Surg. 2020 Summer;32(2):266-268. doi: 10.1053/j.semtcvs.2019.09.006.
- Ozeki N, Yamawaki-Ogata A, Narita Y, Mii S, Ushida K, Ito M, Hirano SI, Kurokawa R, Ohno K, Usui A:Hydrogen water alleviates obliterative airway disease in mice.Gen Thorac Cardiovasc Surg. 2020 Feb;68(2):158-163. doi: 10.1007/s11748-019-01195-3.
- Tokuda Y, Fujimoto K, Narita Y, Mutsuga M, Terazawa S, Ito H, Matsumura Y, Uchida W, Munakata H, Ashida S, Ono T, Nishi T, Yano D, Ishida S, Kuwabara F, Akita T, Usui A:Spinal cord injury following aortic arch replacement.Surg Today. 2020 Feb;50(2):106-113. doi: 10.1007/s00595-019-01853-2.
2019
- Kawai Y, Narita Y, Yamawaki-Ogata A, Usui A, Komori K:Montelukast, a Cysteinyl Leukotriene Receptor 1 Antagonist, Induces M2 Macrophage Polarization and Inhibits Murine Aortic Aneurysm Formation.Biomed Res Int. 2019 May 27;2019:9104680. doi: 10.1155/2019/9104680.
- Yokote J, Araki Y, Saito S, Hasegawa H, Usui A:Effect of an artificial ring on mitral valve function.Nagoya J Med Sci. 2019 May;81(2):207-215. doi: 10.18999/nagjms.81.2.207.
- Konishi Y, Fukunaga N, Abe T, Nakamura K, Usui A, Koyama T:Efficacy of new multimodal preventive measures for post-operative deep sternal wound infection.Gen Thorac Cardiovasc Surg. 2019 Nov;67(11):934-940. doi: 10.1007/s11748-019-01139-x.
- Ito H, Mutsuga M, Oshima H, Usui A.The efficacy of immediate bridging thoracic endovascular aortic repair for ruptured infected thoracic aortic aneurysms.J Vasc Surg Cases Innov Tech. 2019 Apr 30;5(2):152-155. doi: 10.1016/j.jvscit.2018.10.005.
- Uchida W, Tokuda Y, Takehara Y, Usui A.Mechanical haemolytic anaemia assessed with four-dimensional flow cardiac magnetic resonance.Eur J Cardiothorac Surg. 2019 Oct 1;56(4):813-814. doi: 10.1093/ejcts/ezz031.
- Tokuda Y, Narita Y, Fujimoto K, Mutsuga M, Terazawa S, Ito H, Uchida W, Usui A:Neurologic Deficit After Aortic Arch Replacement: The Influence of the Aortic Atherosclerosis.Ann Thorac Surg. 2019 Jul;108(1):107-114. doi: 10.1016/j.athoracsur.2019.01.004.
- Yoshizumi T, Tokuda Y, Abe T, Usui A:Conservative treatment of type A aortic dissection following hybrid arch repair.Gen Thorac Cardiovasc Surg. 2019 Jul;67(7):602-607. doi: 10.1007/s11748-019-01075-w.
- Teramoto C, Mutsuga M, Kawaguchi O, Araki Y, Matsuda J, Usui A:A functional evaluation of cerebral perfusion for coronary artery bypass grafting patients.Heart Vessels. 2019 Jul;34(7):1122-1131. doi: 10.1007/s00380-019-01348-7.
- Hayashi Y, Maekawa A, Sawaki S, Ozeki T, Orii M, Saiga T, Kato R, Usui A, Ito T:Left-Sided Complete Revascularization With Bilateral Internal Thoracic Arteries in Patients With Diabetes.Ann Thorac Surg. 2019 Jun;107(6):1727-1735. doi: 10.1016/j.athoracsur.2018.12.023.
- Akita S, Tajima K, Kato W, Tanaka K, Goto Y, Yamamoto R, Yazawa T, Kozakai M, Usui A:The long-term patency of a gastroepiploic artery bypass graft deployed in a semiskeletonized fashion: predictors of patency.Interact Cardiovasc Thorac Surg. 2019 Jun 1;28(6):868-875. doi: 10.1093/icvts/ivy346.
- Ito H, Usui A, Uchida W, Mutsuga M:Usefulness of lymphography and computed tomography for detecting the site of chyle leakage.Indian J Thorac Cardiovasc Surg. 2019 Jan;35(1):104-107. doi: 10.1007/s12055-018-0735-y.
- Morioka H, Tokuda Y, Oshima H, Iguchi M, Tomita Y, Usui A, Yagi T:Fungal endocarditis after transcatheter aortic valve replacement (TAVR): Case report and review of literature.J Infect Chemother. 2019 Mar;25(3):215-217. doi: 10.1016/j.jiac.2018.08.017.
2018
- Sachie Terazawa, Hideki Oshima, Yuji Narita, Kazuro Fujimoto, Masato Mutsuga, Yoshiyuki Tokuda, Tomo Yoshizumi, Hideki Ito, Wataru Uchida, Akihiko Usui: Strategy of Cardiovascular Surgery for Patients With Dementia as Evaluated by Mini-Mental State Examination. Circulation Journal 09/2018; 82(12)., DOI:10.1253/circj.CJ-18-0312
- Hiroshi Morioka, Yoshiyuki Tokuda, Hideki Oshima, Mitsutaka Iguchi, Yuka Tomita, Akihiko Usui, Tetsuya Yagi: Fungal endocarditis after transcatheter aortic valve replacement (TAVR): Case report and review of literature. Journal of Infection and Chemotherapy 09/2018;, DOI:10.1016/j.jiac.2018.08.017
- Toshijiro Aoki, Akihito Tanaka, Yoshiyuki Tokuda, Hideki Oshima, Susumu Suzuki, Hideki Ishii: Temporary immobile leaflet following transcatheter aortic valve replacement of a SAPIEN-XT valve. Cardiovascular Intervention and Therapeutics 07/2018;, DOI:10.1007/s12928-018-0536-7
- Wataru Uchida, Yoshiyuki Tokuda, Masato Mutsuga, Akihiko Usui: Aortic sarcoidosis complicated by a pulmonary artery aneurysm. European journal of cardio-thoracic surgery: official journal of the European Association for Cardio-thoracic Surgery 03/2018; 54(4)., DOI:10.1093/ejcts/ezy131
- Wataru Uchida, Yuji Narita, Aika Yamawaki-Ogata, Yoshiyuki Tokuda, Masato Mutsuga, Kazuro Lee Fujimoto, Tomonobu Abe, Hideki Oshima, Akihiko Usui: The oral administration of clarithromycin prevents the progression and rupture of aortic aneurysm. Journal of Vascular Surgery 03/2018; 68(6S)., DOI:10.1016/j.jvs.2017.12.047
- Uchida W,MutsugaM,Ito H,OshimaH,Usui A Nonbacterial Thrombotic Endocarditis Associated With Crohn disease, Ann ThoracSurgDisease 105(5) e199-201
- Hideki Ito · Akihiko Usui · WataruUchida · Masato Mutsuga Usefulnessof lymphography and computed tomography for detecting the site of chyleleakage Indian Journal of Thoracic and Cardiovascular Surgery DOI: 10.1007/s12055-018-0735-y
2017
- Hibino M, Abe T, Oshima H2, Narita Y, Mutsuga M, Fujimoto KL, Tokuda Y, Yamana K, Kuroda T, Usui A. Entire Circumferential Reconstruction of the Right Atrium Surrounded by Angiosarcoma. Ann Thorac Surg. 2017 Jun;103(6):e483-e485.
- Abe, Tomonobu; Terazawa, Sachie; Ito, Hideki; Tokuda, Yoshiyuki; Fujimoto, Kazuro; Mutsuga, Masato; Narita, Yuji; Oshima, Hideki; Usui, Akihiko Clinical outcomes and quality of life after surgery for dilated ascending aorta at the time of aortic valve replacement; wrapping versus graft replacement. Nagoya J Med Sci. 2017 Nov; 79(4): 443–451.
- Hibino M, Mutsuga M, Oshima H, Narita Y, Abe T, Fujimoto K, Tokuda Y, Usui A. total Arch Replacement Using Manufactured Frozen Elephant Trunk after Acute Type-A Dissection Repair Kyobu Geka. 2017 Apr;70(4):281-285.
2016
- Tokuda Y, Oshima H, Narita Y, Abe T, Araki Y, Mutsuga M, Fujimoto K, Terazawa S, Yagami K, Ito H, Yamamoto K, Komori K, Usui A. Hybrid versus open repair of aortic arch aneurysms: comparison of postoperative and mid-term outcomes with a propensity score-matching analysis. Eur J Cardiothorac Surg. 2016;49(1):149-56.
- Tokuda Y, Oshima H, Narita Y, Abe T, Mutsuga M, Fujimoto K, Terazawa S, Ito H, Hibino M, Uchida W, Komori K, Usui A. Extended total arch replacement via the L-incision approach: single-stage repair for extensive aneurysms of the aortic arch. Interact Cardiovasc Thorac Surg 2016; 22(6); 750-5
- Suenaga H, Usui A, Mutsuga M, Oshima H, Abe T, Narita Y, Fujimoto K, Tokuda Y. The changes of aortic diameter after aortic repair with aortic tailoring technique for chronic type B aortic dissection. Eur J Cardiothorac Surg. 2016 pii: ezw240. [Epub ahead of print]
- Hibino M, Oshima H, Narita Y, Abe T, Mutsuga M, Fujimoto KL, Tokuda Y, Terazawa S, Ito H, Usui A. Early and Late Outcomes of Thoracic Aortic Surgery in Hemodialysis Patients. Ann Thorac Surg. 2016;102(4):1282-8.
- Oshima H, Tokuda Y, Araki Y, Ishii H, Murohara T, Ozaki Y, Usui A. Predictors of early graft failure after coronary artery bypass grafting for chronic total occlusion. Interact Cardiovasc Thorac Surg. 2016;23(1):142-9.
- Harada K, Shibata R, Ouchi N, Tokuda Y, Funakubo H, Suzuki M, Kataoka T, Nagao T, Okumura S, Shinoda N, Kato B, Sakai S4, Kato M, Marui N, Ishii H, Amano T, Matsubara T, Murohara T. Increased expression of the adipocytokine omentin in the epicardial adipose tissue of coronary artery disease patients. Atherosclerosis. 2016 Aug;251:299-304
- Yamamoto K, Komori K, Narita H, Morimae H, Tokuda Y, Araki Y, Oshima H, Usui A. A 'through-and-through bowing technique' for antegrade thoracic endovascular aneurysm repair with total arch debranching: a technical note and the initial results. Eur J Cardiothorac Surg. 2016 Apr;49(4):1264-9.
2015
- Araki Y, Usui A, Oshima H, Abe T, Fujimoto K, Mutsuga M, Tokuda Y, Terazawa S, Yagami K, Ito H. Impact of the intraoperative use of fibrinogen concentrate for hypofibrinogenemia during thoracic aortic surgery. Nagoya J Med Sci. 2015;77(1-2):265-73.
- Okada N, Oshima H, Narita Y, Abe T, Araki Y, Mutsuga M, Fujimoto KL, Tokuda Y, Usui A. Impact of Surgical Stroke on the Early and Late Outcomes After Thoracic Aortic Operations. Ann Thorac Surg. 2015;99(6):2017-23.
- Abe T, Oshima H, Narita Y, Araki Y, Mutsuga M, Fujimoto K, Tokuda Y, Terazawa S, Yagami K, Usui A. Influence of the characteristics of Japanese patients on the long-term outcomes after aortic valve replacement: results of a microsimulation. Gen Thorac Cardiovasc Surg. 2015;63(5):260-6
2013
- Tokuda Y, Oshima H, Araki Y, Narita Y, Mutsuga M, Kato K, Usui A. Detection of thoracic aortic prosthetic graft infection with 18F-fluorodeoxyglucose positron emission tomography/computed tomography. Eur J Cardiothorac Surg. 2013;43(6):1183-7.
- Tokuda Y, Miyata H, Motomura N, Araki Y, Oshima H, Usui A, Takamoto S; Japan Adult Cardiovascular Database Organization.. Outcome of pericardiectomy for constrictive pericarditis in Japan: a nationwide outcome study. Ann Thorac Surg. 2013;96(2):571-6.
2012
- Usui A, Miyata H, Ueda Y, Motomura N, Takamoto S. Risk-adjusted and Case-matched Comparative Study Based on the Japan Adult Cardiovascular Surgery Database between Antegrade and Retrograde Cerebral Perfusion in Aortic Arch Surgery. Gen Thorac Cardiovasc Surg. 2012 Mar;60(3):132-9.
- Fujimoto KL, Tobita K, Guan J, Hashizume R, Takanari K, Alfieri CM, Yutzey KE, Wagner WR. Placement of an elastic biodegradable cardiac patch on a subacute infarcted heart leads to cellularization with early developmental cardiomyocyte characteristics.J Card Fail. 2012 Jul;18(7):585-95.
2011
- Fujimoto KL, Clause KC, Liu LJ, Tinney JP, Verma S, Wagner WR, Keller BB, Tobita K.Engineered fetal cardiac graft preserves its cardiomyocyte proliferation within postinfarcted myocardium and sustains cardiac function.Tissue Eng Part A. 2011 Mar;17(5-6):585-96
2010
- Suzuki S, Usui A, Yoshida K, Matsuura A, Ichihara T, Ueda Y. Effect of cardiopulmonary bypass on cancer prognosis. Asian Cardiovasc Thorac Ann. 2010;18(6):536-40.
- Mutsuga M, Narita Y, Araki Y, Maekawa A, Oshima H, Usui A, Ueda Y. Spinal cord protection during a thoracoabdominal aortic repair for a chronic type B aortic dissection using the aortic tailoring strategy. Interact Cardiovasc Thorac Surg. 2010;11(1):15-9.
2009
- Fujimoto KL, Ma Z, Nelson DM, Hashizume R, Guan J, Tobita K, Wagner WR.Synthesis, characterization and therapeutic efficacy of a biodegradable, thermoresponsive hydrogel designed for application in chronic infarcted myocardium.Biomaterials. 2009 Sep;30(26):4357-68. doi: 10.1016/j.biomaterials.2009.04.055. Epub 2009 May 31.
- Fujimoto KL, Miki T, Liu LJ, Hashizume R, Strom SC, Wagner WR, Keller BB, Tobita K.Naive rat amnion-derived cell transplantation improved left ventricular function and reduced myocardial scar of postinfarcted heart. Cell Transplant. 2009;18(4):477-86. doi: 10.3727/096368909788809785.
- Mutsuga M, Narita Y, Yamawaki A, Satake M, Kaneko H, Suematsu Y, Usui A, Ueda Y. A new strategy for prevention of anastomotic stricture using tacrolimus-eluting biodegradable nanofiber. J Thorac Cardiovasc Surg. 2009;137(3):703-9.
2008
- Yoshiyuki Tokuda, Min-Ho Song, Hideki Oshima, Akihiko Usui, Yuichi Ueda: Predicting Midterm Coronary Artery Bypass Graft Failure by Intraoperative Transit Time Flow Measurement. The Annals of thoracic surgery 08/2008; 86(2):532-6.
2007
- Usui A, Ueda Y. Arch first technique under deep hypothermic circulatory arrest with retrograde cerebral perfusion. Multimed Man Cardiothorac Surg. 2007;2007(102)
- Fujimoto KL, Tobita K, Merryman WD, Guan J, Momoi N, Stolz DB, Sacks MS, Keller BB, Wagner WR.An elastic, biodegradable cardiac patch induces contractile smooth muscle and improves cardiac remodeling and function in subacute myocardial infarction. J Am Coll Cardiol. 2007 Jun 12;49(23):2292-300. Epub 2007 May 25.
- Fujimoto KL, Guan J, Oshima H, Sakai T, Wagner WR.In vivo evaluation of a porous, elastic, biodegradable patch for reconstructive cardiac procedures. Ann Thorac Surg. 2007 Feb;83(2):648-54.
- Yoshiyuki Tokuda, Min-Ho Song, Norifumi Mabuchi, Akihiko Usui, Yuichi Ueda: Right Ventricular End-Diastolic Volume in the Postoperative Care of Cardiac Surgery Patients. Circulation Journal 09/2007; 71(9):1408-1411., DOI:10.1253/circj.71.1408
- Yoshiyuki Tokuda, Min-Ho Song, Yuichi Ueda, Akihiko Usui, Toshiaki Akita: Predicting Early Coronary Artery Bypass Graft Failure by Intraoperative Transit Time Flow Measurement. The Annals of thoracic surgery 01/2008; 84(6):1928-33., DOI:10.1016/j.athoracsur.2007.07.040
- Yoshiyuki Tokuda, Min-Ho Song, Yuichi Ueda, Akihiko Usui, Toshiaki Akita, Shigeru Yoneyama, Shigeru Maruyama: Three-dimensional numerical simulation of blood flow in the aortic arch during cardiopulmonary bypass. European Journal of Cardio-Thoracic Surgery 03/2008; 33(2):164-7., DOI:10.1016/j.ejcts.2007.11.021
2006
- Yoshiyuki Tokuda, Peter W Grant, Hugh D Wolfenden, Con Manganas, William J Lyon, John S K Murala: Levosimendan for patients with impaired left ventricular function undergoing cardiac surgery. Interactive Cardiovascular and Thoracic Surgery 06/2006; 5(3):322-6., DOI:10.1510/icvts.2005.122390
MESSAGE
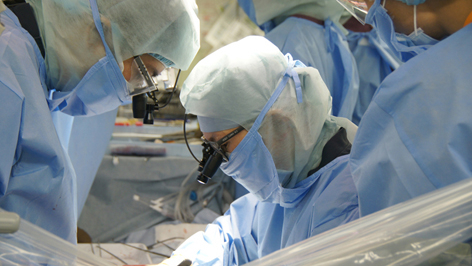
心臓外科を志す若手医師の先生へ
名古屋大学では20の関連施設と協力して、心臓外科を志す若手医師の方々に心臓血管外科専門医教育を行っています。心臓血管外科専門医を取得するためには最低50例の術者経験とともに多くの臨床経験を必要とします。名古屋大学には関連施設を含め年間約2500例の心臓・大血管手術総数があり、若手外科医に十分な臨床経験を提供できる基盤があります。
2年間の初期臨床研修後、心臓外科臨床研修は卒後3年目以降に開始します。卒後4年目までに一般外科系研修を行い、外科専門医受験資格が得られるように関連施設と協力してカリキュラム調整を行っています。3年目以降の心臓外科修練は初期臨床研修病院で行うことが一般的ですが、経験症例数に応じて複数の施設への異動も考慮しています。
心臓外科臨床研修は卒後4年次以降に本格化します。この期間は心臓手術数の多い大規模施設で研修を行う事を基本とし、卒後7、8年目までに心臓血管外科専門医取得が可能な手術数を経験できるように指導します。
私たちは大学院教育を卒後教育期間の一環と位置づけ、心臓血管外科専門医実地修練に準拠した臨床指導およびacademic supportを行っています。原則として卒後6、7年目に社会人大学院生として大学院に入学し、1年間以上の臨床研修を医学部附属病院で行います。附属病院では、補助人工心臓・心臓移植などの重症心不全の外科治療、および大動脈外科治療を中心に研修します。カテーテル弁置換も経験可能です。臨床研究、全国学会発表、論文作成を行い、心臓血管外科専門医取得に必要な業績をあげるとともに、学位論文相応の研究を指導します。
私たちは卒後約10年間で外科専門医、心臓血管外科専門医、医学博士を取得することを目標とし、心臓血管外科に関する卒後臨床教育を行っています。
心臓血管外科専門医の詳細は http://cvs.umin.jp/ (日本心臓血管外科専門医認定機構)を参照してください。
外科専門医の詳細は http://www.jssoc.or.jp/procedure/specialist/(日本外科学会ホームページ)を参照してください。
キャリアについて少し相談してみたいという先生や医学生の方、あるいは入局を希望される先生は、お気軽に ご連絡ください
https://form.run/@heartteamnagoya-1635673339
名古屋大学医学部心臓外科 関連施設一覧
名古屋大学心臓外科学教室の関連施設は以下の通りです
教室は関連病院として、東海地区を中心に多くの心臓血管外科施設を擁しています。成人、小児 双方の臨床経験を積むのに十分な指導医数と手術数がありレベルの高い臨床修練が可能です。重症心不全治療 小切開手術 低侵襲治療 血管内治療などの経験も積むことも可能です。
名古屋大学医学部附属病院 https://www.med.nagoya-u.ac.
名古屋医療センター http://www.nnh.go.jp/index.php
一宮市立市民病院 http://www.municipal-hospital.ichinomiya.aichi.jp/
岡崎市民病院 http://www.okazakihospital.jp/
春日井市民病院 http://www.hospital.kasugai.aichi.jp/
公立陶生病院 http://www.tosei.or.jp/
小牧市民病院 http://www.komakihp.gr.jp/
豊橋市民病院 http://www.municipal-hospital.toyohashi.aichi.jp/
中京病院 http://www.chukyo-hosp.jp/
名古屋掖済会病院 http://nagoya-ekisaikaihosp.jp/
名古屋第一赤十字病院 http://www.nagoya-1st.jrc.or.jp/
名古屋第二赤十字病院 http://www.nagoya2.jrc.or.jp/
岐阜県立多治見病院 http://www.tajimi-hospital.jp/
大垣市民病院 http://www.omh.ogaki.gifu.jp/
静岡済生会総合病院 http://www.siz.saiseikai.or.jp/hosp/
四日市市立四日市病院 http://www.city.yokkaichi.mie.jp/hospital/index.html
厚生連 豊田厚生病院 http://www.toyota.jaaikosei.or.jp/
厚生連 海南病院 http://www.jaaikosei.or.jp/kainan/
あいち小児保健医療総合センター http://www.achmc.pref.aichi.jp/
トヨタ記念病院 http://www.toyota-mh.jp/
藤田医科大学 岡崎医療センター https://okazaki.fujita-hu.ac.jp/

