臨床研究中核病院について
本院は2016年1月に医療法に基づく臨床研究中核病院に承認されました。
臨床研究中核病院とは、日本発の画期的な医薬品や医療技術などを開発するために、国際水準の臨床研究や医師主導治験の中心的な役割を担う病院です。
本院では、臨床研究中核病院としてさらに臨床研究、医師主導治験を加速させ、新しい医療の開発に力を入れていきます。
臨床研究について
新しい治療法を確立するためには、その効き目と安全性を十分に調べなければなりません。まずいろいろな動物を使い、効き目と安全性について調べます。
そして、人の病気に役立つかどうかを健康な方や患者さんにご協力いただき調べます。
このように、病気の予防、診断、治療方法の改善や病気の原因究明のために、ヒトを対象に行われる医学研究のことを「臨床研究」といいます。
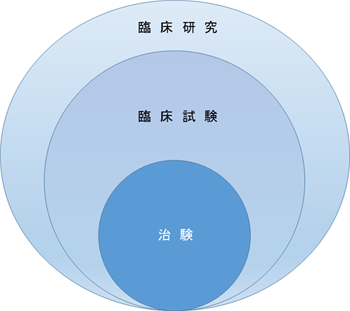
臨床研究は、「観察研究」と「臨床試験(医薬品、医療機器、治療などを試験的に行い、安全性や有用性を調べる)」に分けられます。「臨床試験」のうち、新しい薬や医療機器を製造販売について国の承認を得るために行うものを「治験」といいます。
臨床研究には、一般の治療と異なり、研究的な側面があります。
このような臨床研究によって得られた結果は、患者さんのプライバシーに関わる情報を切り離した上で報告書にまとめ、学術論文の発表といった形で社会に還元され、将来同じ病気になった多くの患者さんの治療に役立つことになります。
臨床研究は参加された方の安全や人権を守るために、「ヘルシンキ宣言(人間を対象とする医学研究の倫理的原則)」、「人を対象とする生命科学・医学系研究に関する倫理指針」、「再生医療等の安全性の確保等に関する法律」などに従って行われます。
本院の臨床研究に関する実施方針
名古屋大学医学部附属病院は、病院理念である「診療・教育・研究を通して社会に貢献します」に則り制定した基本方針のひとつ「次代を担う新しい医療を開拓します」に基づき、以下の方針を定め、臨床研究を実施します。
- 人を対象とした生命科学・医学系研究の倫理規範である「ヘルシンキ宣言」及び関連法規、指針等を遵守します。
- 独立かつ公正な立場に立った関連委員会の承認及び病院長の許可のもと、研究参加者の生命、健康並びに人格を最大限に尊重し臨床研究を実施します。
- 臨床研究の透明性を確保するために、当院で実施する総ての臨床研究を厳重に管理し、不正の防止に努めます。
- 臨床研究の実施に先立ち、臨床研究に関する法規・倫理及び必要な知識に関する教育研修を実施し、臨床研究認定者制度をもって研究者の質を担保しています。
- 研究参加者に対して事前に十分な説明を行い、研究参加者の自由意思による同意を得た上で臨床研究を実施します。
- 臨床研究の実施により知り得た情報は、適切に管理します。
- 国内外の医療機関等と協働して、新たな医療技術創出を加速します。
- 中部先端医療開発円環コンソーシアムならびに関連の医療機関等において実施される国内外の臨床研究を積極的に支援します。
- 質の高い臨床研究を実施し、日本発の革新的な医薬品、医療機器等を開発することで国民の健康及び福祉の向上に貢献します。
当院の治験・臨床研究につきましては下記の委員会で審議・審査を行っております。
・名古屋大学大学院医学系研究科及び医学部附属病院における生命倫理審査委員会
患者申出療養制度について
臨床研究中核病院の役割の一つとして、本院では「患者申出療養制度」を実施することができます。
詳細はこちらからご覧下さい。
問い合わせ先
本院における治験・臨床研究についてのお問い合わせ及びご意見(疑義を含む)は,以下の窓口へご連絡ください。
対 応 時 間:8時30分~17時00分(土曜日,日曜日,祝休日及び年末年始を除きます。)
連 絡 先:①治験に関すること。
先端医療・臨床研究支援センター 臨床研究支援部門
052-744-1956
②臨床研究に関すること。
経営企画課臨床審査公正係
052-744-2479
※窓口の対応時間外のお問い合わせは,以下のe-mailアドレス,もしくはFAX番号宛にご連絡ください。
翌診療日以降,速やかに対応いたします。
e-mail : ack-tiken@med.nagoya-u.ac.jp
F A X : 052-744-2948
2018年09月01日現在






