腹膜播種を有する進行胃癌に対する新たな挑戦 ~SYT13を標的としたアンチセンス核酸医薬品ASO-4733の第Ⅰ相医師主導治験を開始~
このたび、国立大学法人東海国立大学機構名古屋大学大学院医学系研究科 消化器外科学の神田 光郎 教授らの研究グループは、腹膜播種(※1)を有する切除不能な進行・胃癌患者に対して、新規アンチセンス核酸医薬品(※2)「ASO-4733」を腹腔内に投与する第Ⅰ相医師主導治験を開始しました。
ASO-4733は、腹膜播種を起こす胃癌で特異的に高発現するsynaptotagmin 13(SYT13)を標的とするアンチセンス核酸医薬品です。腹腔内に投与してSYT13発現を選択的に抑制することで直接的にがん細胞を攻撃するアプローチです。本薬は、名古屋大学、国立研究開発法人医薬基盤・健康・栄養研究所 創薬デザイン研究センター及び国立大学法人大阪大学の連携により創製された国産の核酸医薬品であり、アカデミアによるトランスレーショナルリサーチの成果が臨床応用に至った例となります。
【本研究のポイント】
- 腹膜播種に特異的に発現する分子「SYT13」を標的としたアンチセンス核酸医薬品「ASO-4733」を、世界で初めてヒトに投与する第Ⅰ相医師主導治験を名古屋大学医学部附属病院で実施。
- ASO-4733は、独自の製剤設計と腹腔内への直接投与により、高い薬剤濃度を維持し、全身投与では難しい腹膜播種部位への選択的送達を目指す。
- 全身化学療法と腹膜局所治療を組み合わせた新たな治療アプローチを構築。
- 本治験は安全性と忍容性の確認、及び用法・用量の最適化を目的とする。
- アカデミア創薬研究発の国産核酸医薬品の臨床応用例。
【背景】
胃癌は日本において依然として主要な死因の一つであり、なかでも腹膜播種は、がん細胞が腹腔内に散らばり多数の小結節を形成する転移形式であり、胃癌の中でも特に難治性で予後不良とされています。現在の標準的治療である全身化学療法(点滴や内服による抗がん剤治療)では、腹腔内に拡がったがん細胞に十分薬剤が届かないことが治療効果を制限する要因の一つとされています。そのため、抗がん剤を腹腔内に直接投与する方法(腹腔内投与)が検討されてきましたが、既存の薬剤では効果が限定的で、新たな薬剤の開発が望まれてきました。
神田 光郎 教授らの研究グループは、腹膜播種を有する胃癌で特異的に高発現する分子「SYT13」に着目し、この分子を標的としたアンチセンス核酸医薬品「ASO-4733」の開発を、大阪大学大学院薬学研究科の小比賀 聡 教授、医薬基盤・健康・栄養研究所 創薬デザイン研究センターの笠原 勇矢 プロジェクトリーダーと共同で進めてきました。ASO-4733は、高い標的結合性を有するとともに、大阪大学が独自に開発したアミド架橋型人工核酸(※3)を搭載し、生体内安定性を実現しています。また、本薬は腹腔内に投与することで、特別なキャリアー(※4)を必要とせずにがん細胞内に取り込まれ、薬剤が腹膜内に長時間とどまり、局所のがん細胞に対して持続的に作用するように設計されています。
【関連する過去の研究結果】
本研究グループは、本治験で使用するアンチセンス核酸医薬品「ASO-4733」について、これまでに複数の動物実験による安全性試験を実施してきました。
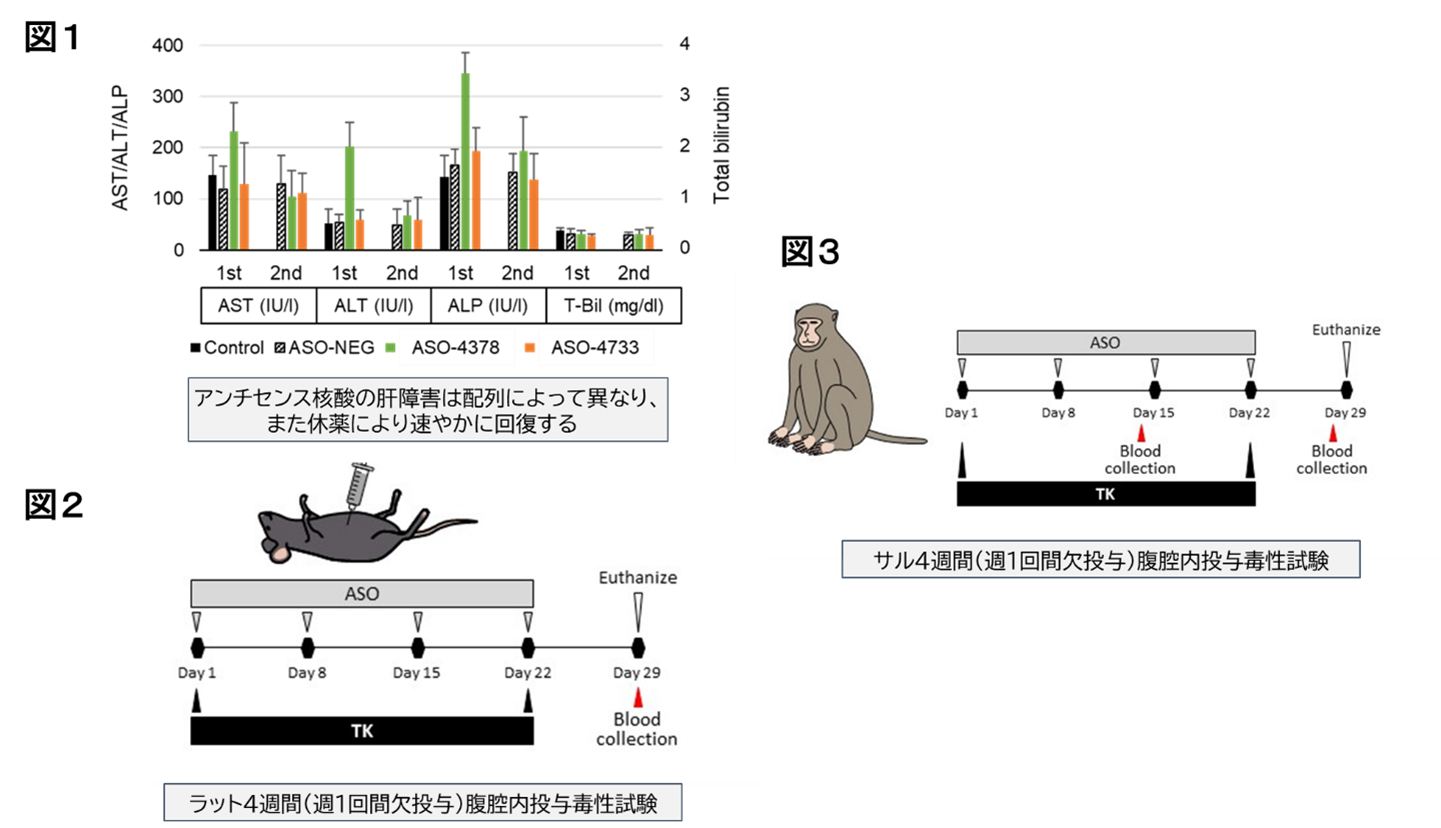
まず、本来の標的以外の遺伝子に作用してしまう「オフターゲット効果」について検討したところ、ASO-4733は他の遺伝子への影響が極めて少なく、標的特異性に優れていることが確認されました。一般に、アンチセンス核酸医薬品は高用量投与により肝障害を引き起こす可能性が指摘されていますが、マウスにASO-4733を投与後、2週間及び休薬2週間後の血液検査において、高用量群では一時的に肝胆道系酵素の上昇が見られたものの、休薬により速やかに回復することが確認されました(図1)。
さらに、ラットを用いた4週間の反復投与毒性試験では、一部の個体で体重減少や血液検査値の変化が見られたものの、致死的な毒性や重篤な臓器障害は認められませんでした(図2)。また、カニクイザルを用いた4週間反復投与毒性試験においては、臨床想定投与量の50倍という高用量でも、全身状態の悪化や主要臓器への明確な有害影響は認められず、全体として良好な安全性プロファイルが示されました(図3)。
これらの結果から、ASO-4733のヒトにおける初回投与試験を実施することは可能であると判断されています。
【研究の概要】
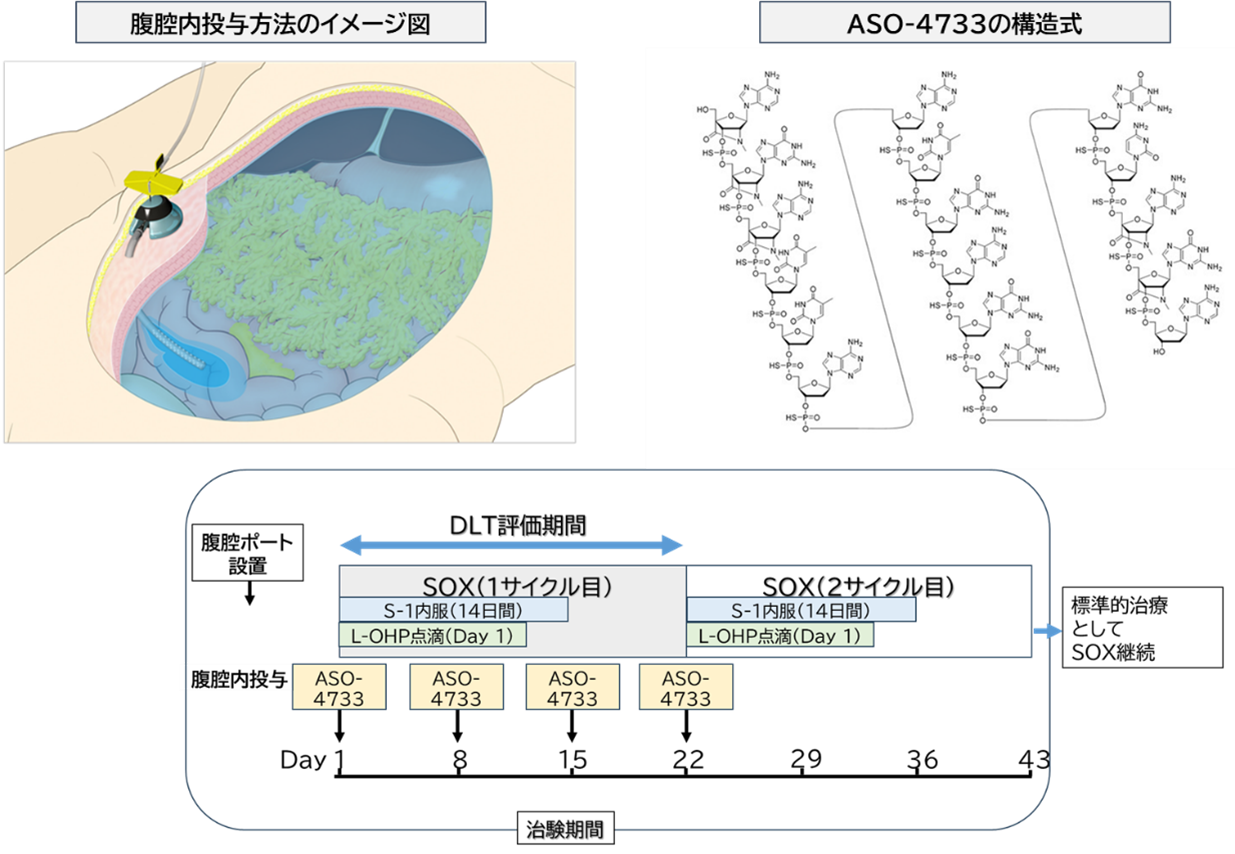
本治験は、令和6年度国立研究開発法人日本医療研究開発機構(AMED)橋渡し研究プログラム(シーズC)の助成を受けて実施されるものであり、名古屋大学医学部附属病院において、「腹膜播種を有する治癒切除不能な進行・再発胃癌に対するASO-4733腹腔内投与とSOX療法併用の第Ⅰ相医師主導治験(jRCT2041250021)」として、本年5月より開始されました。
本治験では、ASO-4733の安全性及び忍容性の評価を主たる目的とし、用量制限毒性(DLT:Dose-Limiting Toxicity:※5)の発現に基づき最大耐用量及び推奨用量を決定します。さらに、血中及び腹水中における薬物動態の解析も併せて実施します。
なお、本治験では、胃あるいは食道胃接合部に発生した腺癌で、腹膜播種又は腹水中にがん細胞が認められる症例を対象としています。周術期治療を除く抗がん剤治療歴がなく、全身状態、腎機能・肝機能など一定の医学的基準を満たすことが前提とされています。
【今後の展開】
本治験により、ASO-4733の忍容性と最適な投与法(最大耐用量及び推奨用量)を確立し、有効性と安全性を検討する次段階の試験への移行を目指しています。
また、治験と並行して、SYT13の腫瘍組織における発現量や腹水中SYT13 mRNA量の変動に着目した探索的バイオマーカー研究も進行中です。これにより、将来的には治療効果の予測や治療対象の選別に資するバイオマーカーの確立が期待されます。
腹膜播種に対する核酸医薬品という新たな治療選択肢の確立を目指し、今後も臨床研究と基礎研究を密接に連携させた取り組みを継続してまいります。
【謝辞】
本治験は、日本医療研究開発機構(AMED)橋渡し研究プログラム「胃癌腹膜播種に特化したアンチセンス核酸医薬開発」の支援を受けて実施されています。また、本治験の実施にあたっては、名古屋大学医学部附属病院 先端医療開発部の協力を得ています。
【用語説明】
※1 腹膜播種(ふくまくはしゅ)
がんの転移の一つで、腹腔内にがん細胞が播種(散らばること)して腹膜上に多数のがん細胞の塊である小結節を形成するものです。腹膜播種が増加することで、腹水や腸閉塞を引き起こします。
※2 アンチセンス核酸医薬品
核酸(DNAやRNA)を治療に応用した核酸医薬の1つです。通常は化学修飾された1本鎖のDNAで、標的とするmRNAに結合し蛋白質合成を制御します。
※3 アミド架橋型人工核酸
標的RNAへの結合性を高めつつ生体内で分解されにくくするために核酸の糖部に人工的にアミド架橋構造を加えた核酸誘導体です。
※4 キャリアー
薬剤を必要な場所へ送り届けるための物質のことです。この場合は、アンチセンス核酸をがん細胞内に取り込ませるための物質を指します。
※5 DLT(用量制限毒性, Dose-Limiting Toxicity)
新しい薬剤の安全性を評価する際に、特に重篤で、薬剤の減量又は中止が必要となりうる副作用を「DLT(用量制限毒性)」と呼びます。第I相治験では、このDLTの有無を指標として、その薬剤をどの程度の量まで安全に投与できるか(最大耐用量)を評価する重要な指標となります。






