CAR-T細胞の安全性に関する臨床第I相試験の第1コホート終了/チュラロンコン大学での治療抵抗性悪性リンパ腫に対するCAR-T細胞を用いた投与の開始について
名古屋大学大学院医学系研究科小児科学分野の高橋義行教授、先端医療開発部の西尾信博特任講師らの研究グループは、非ウイルスベクターであるpiggyBacトランスポゾン法(※1)を用いたキメラ抗原受容体(※2)遺伝子改変T細胞(Chimeric Antigen Receptor modified T cell:以下、CAR-T細胞)の培養法を用い、2018年2月より化学療法抵抗性または造血細胞移植後再発性のCD19陽性急性リンパ性白血病(以下、ALL)に対するCAR-T細胞療法の安全性に関する第1相試験を実施してきましたが、この度第一コホートである16歳以上の3名の患者さんへの投与が終了し、その安全性と一定の有効性が確認されました。また、タイ王国のチュラロンコン大学において、名古屋大学が支援している同培養法を用いた臨床試験を実施し、悪性リンパ腫の1名の患者さんへの投与が完了しました。
ポイント
○名古屋大学で実施しているALLを対象としたpiggyBac法CAR-T細胞療法の臨床研究で、第1コホート(16歳から60歳)の3名に対し安全に投与を完了し、第2コホート(1歳から15歳)に進むことができた。
○名古屋大学が支援しているタイのチュラロンコン大学のCAR-T細胞を用いた臨床研究で、悪性リンパ腫の患者さん1名が治療を受け、安全性に問題なく引き続き治療を進めている。
1.背景
ALLや悪性リンパ腫は、血液中の白血球の中のリンパ球が「がん化」して、患者体内で無限に増殖して発症する疾患です。近年の多剤併用化学療法や造血細胞移植の進歩により、多くの患者さんで長期生存が得られるようになりましたが、治療抵抗例、再発例の難治患者に対する確立された治療法はありません。以上より、難治性のALL、悪性リンパ腫に対する新規治療法が切望されてきました。 近年、CAR-T細胞療法が開発され、治療抵抗性、再発等の難治性の患者を対象としているにもかかわらず、ALLでは70-90%、悪性リンパ腫では40-50%という高い治療反応率が報告されました。CARとは、抗体の抗原認識部位とT細胞受容体の細胞内シグナル伝達部位を繋いだ構造を持つ、人工的なタンパク質です。CAR-T細胞療法とは、このタンパク質を発現する遺伝子を体外でT細胞に遺伝子導入して患者へ戻す治療です。CAR-T細胞の製造では、国内外で承認されている製品を含め、遺伝子導入にレトロウイルスやレンチウイルスなどのウイルスベクターを用いていますが、製造費用が極めて高額であることが問題となっています。本研究グループは非ウイルスベクターであるpiggyBacトランスポゾン法を用いた遺伝子導入によるCAR-T 細胞の作製方法を開発し、臨床試験を行ってきました(図1)。本法は、酵素ベクター法の1つで、ウイルスベクターを用いた場合より製造方法が簡便で、製造の低コスト化が可能であり、かつウイルスベクターと同等の治療効果も期待できると考えられます。一方で、2018年にタイのチュラロンコン大学病院から名古屋大学へ要請があり、名古屋大学で製造している同一プロトコルによる臨床試験に対しての支援を行うとの契約を交わしました(図2)。チュラロンコン大学から2名の細胞培養技術者が名古屋大学で技術供与を受けて帰国し、ALLと悪性リンパ腫に対する臨床試験が開始されました。
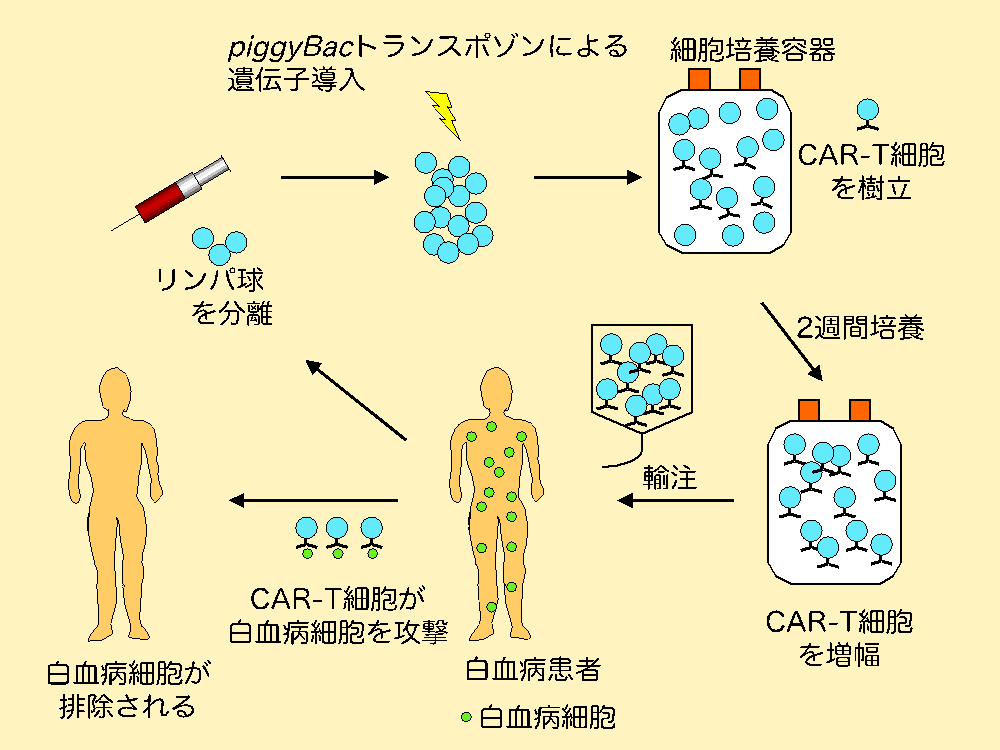
図1:piggyBac法CAR-T細胞療法の模式図

図2:タイのチュラロンコン大学医学部と名古屋大学医学部間でCAR-T細胞療法支援のMTA締結(2018年12月)
2.研究成果
2018年2月より名古屋大学において、化学療法抵抗性または造血細胞移植後再発性のCD19陽性ALLに対するCAR-T細胞療法の安全性に関する第1相試験を実施してきました。第1コホートである16歳以上の3名の患者さんへの投与が終了し、その安全性と一定の有効性が確認され、1歳から15歳の患者さんを対象とした第2コホートへ移行しました。また、タイ王国のチュラロンコン大学において、名古屋大学が支援している同培養法を用いた臨床試験を実施し、PiggyBac法CAR-T細胞治療としては世界で初めて悪性リンパ腫の患者さんへ2020年10月に安全に投与され、引き続き臨床試験を継続しています。
3.今後の展開
多くの患者さんに本治療を届けるため、本治療法の保険収載を目指しています。株式会社ジャパン・ティッシュ・エンジニアリング(J-TEC)は2018年6月に名古屋大学・信州大学とライセンス契約を締結、本技術を導入し、ALLに対するCD19.CAR-T細胞(開発コード:JPCAR019)の臨床治験を来年度に開始する準備を進めています。また、悪性リンパ腫に対しても、同時期にJPCAR019を用いた医師主導治験の開始することを目指して準備しています。さらに、CAR の抗原認識部位を変更することにより、他の固形腫瘍などを標的としたCAR-T細胞製剤にも応用していくことが可能となります。国際協力として、規制やコストの問題でウイルスベクターによるCAR-T製造が困難なタイをはじめとした東南アジアの国においても本製造法を用いてCAR-T細胞療法が実施できるように引き続き支援を行います。タイでの臨床試験の安全性情報はお互いに共有して日本における製造販売承認申請時の参考資料とする予定です。
4.研究費
本研究は、以下の支援を受けて行われました。
- 2015年度~2016年度 日本医療研究開発機構(AMED)革新的がん医療実用化研究事業「小児急性リンパ性白血病に対する非ウイルスベクターを用いたキメラ抗原受容体T細胞療法の開発」(研究開発代表者名、所属・役職:高橋 義行、名古屋大学大学院医学系研究科 小児科学・教授)
- 2017年度~2019年度 日本医療研究開発機構(AMED)革新的がん医療実用化研究事業「小児急性リンパ性白血病に対する非ウイルスベクターを用いたキメラ抗原受容体T細胞療法の実用化」(研究開発代表者名、所属・役職:高橋 義行、名古屋大学大学院医学系研究科 小児科学・教授)
5.用語説明
※1 piggyBacトランスポゾン法:酵素ベクター法の1つであり、ウイルスベクターを用いず、ある特異的な配列に挟まれた遺伝
子を染色体に組み込むことのできる遺伝子導入法。
※2 キメラ抗原受容体(Chimeric Antigen Receptor: CAR): 抗体の抗原認識部位とT細胞受容体の細胞内シグナル伝達部位を繋
いだ構造を持つ、人工的なタンパク質。CAR-T細胞療法とはこのタンパク質を発現する遺伝子を体外でT細胞に遺伝子導入
して患者へ戻す治療。






