臨床医薬学医療薬学(協力)((病)薬剤部)
研究室概要
脳は心拍数から記憶に至る全ての生体活動を司る臓器です。個々の脳機能はシナプス接続で構成された特定の神経回路によって制御されています。最も重要となるシナプスの特徴は活動依存的な可塑性です。当研究室では主に神経精神疾患や高次脳機能について研究を行っています。神経精神疾患研究では統合失調症、薬物依存症およびアルツハイマー型認知症などについて、それらの病因/病態生理学的意義を明らかにしたいと考えています。また、高次脳機能に関する研究では、学習記憶や情動に関わる分子・細胞生物学的メカニズムの解明を目指して、作業記憶/短期記憶および参照記憶/長期記憶を担う分子基盤を研究しています。
研究プロジェクト
1. 精神疾患に関する研究
i) 統合失調症に関する研究
遺伝因子および環境因子の双方が統合失調症の病因に関与していると考えられています。近年、統合失調症について、neuregulin-1, dysbindinやdisrupted-in-schizophrenia 1 (DISC1)などの遺伝子が発症脆弱性因子として研究されています。疫学的研究では統合失調症の環境因子が同定され、周産期における母体のウイルス感染が最も有力な危険因子であると考えられています。ヒトにおいて第二妊娠期の母体ウイルス感染は、生まれた子供が思春期・成人期に統合失調症を発症するリスクを増加させることが報告されています。特に、神経発達期における遺伝—環境相互作用が統合失調症の病因であるという仮説が提唱されています。
私たちはDISC1を含む様々な統合失調症の発症脆弱性遺伝子の変異マウスを用いて行動学的、神経科学的および神経解剖学的な観点から表現型の解析を行っています。また、遺伝子変異マウスに合成二本鎖RNAアナログであるpolyriboinosinic-polyribocytidilic acid(polyI:C)を処置して統合失調症の遺伝—環境相互作用を解析しています。PolyI:Cは、自然免疫を活性化するtoll様受容体3 (TLR3) リガンドであり、ウイルス感染と類似した免疫反応を惹起する薬物です。周産期にpolyI:Cを投与したマウスは統合失調症の神経発達障害モデル動物として使用されています(図1)。
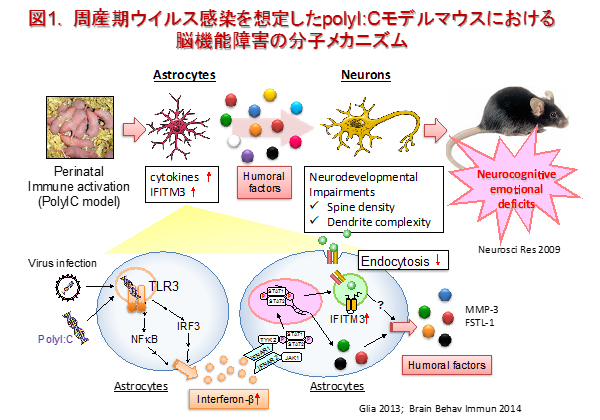
ii) ストレス関連疾患に関する研究
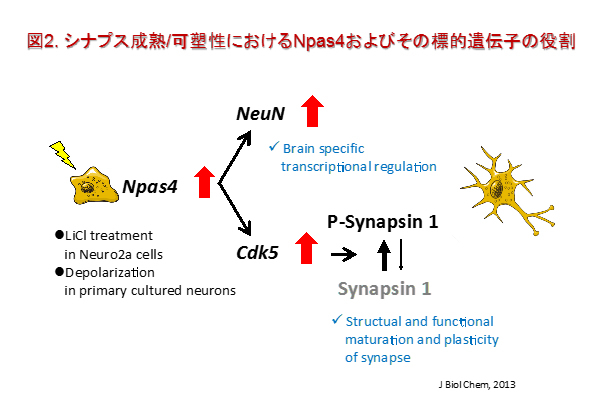
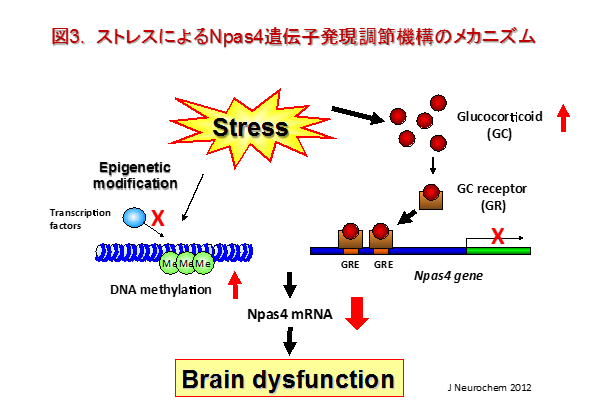
これまでに当研究室では、幼若期から長期隔離飼育を施したマウスにおいて、海馬歯状回における神経新生および学習記憶が障害されることを報告しました。また、隔離飼育により海馬歯状回における転写調節因子neuronal PAS domain protein 4(Npas4)のmRNA発現量が低下することも見いだしました。Npas4遺伝子は、神経細胞の分化や発達に関与しており、ストレスと神経発達における転写調節因子の役割について解析を進めています(図2、3)。
iii) 薬物依存症に関する研究
薬物依存症は長期にわたり再燃を繰り返す疾患であり、強迫的な薬物摂取、使用制限の欠如および薬物に対する激しい渇望によって特徴づけられます。薬物の正の強化/報酬効果の作用は、側坐核に投射する中脳辺縁系のドパミン作動性神経系によって引き起こされます。一方、薬物に対する渇望は前頭前皮質の活性化が関与しています。薬物の慢性的な摂取は、薬物依存症の形成に最も重要なシナプスの構成分子および機能に代償的な変化を惹起します。私たちは、TNF-αやGDNFなどのサイトカイン類、tissue plasminogen activator(tPA)や matrix metalloproteinase(MMP-2/MMP-9)などのプロテアーゼが依存性薬物を処置した脳内で産生され、薬物依存症の形成に重要な役割を果たしていることを明らかにしました。これらの薬物依存症の内因性調節因子は依存促進因子と依存抑制因子に分類されます。私たちはこれら依存促進因子と依存抑制因子の不均衡が薬物依存症の形成や再燃に関与していることを提唱しています。これらの内因性調節因子を創薬標的とすることが薬物依存症の新規治療方法の開発に繋がると考えています(図4)。
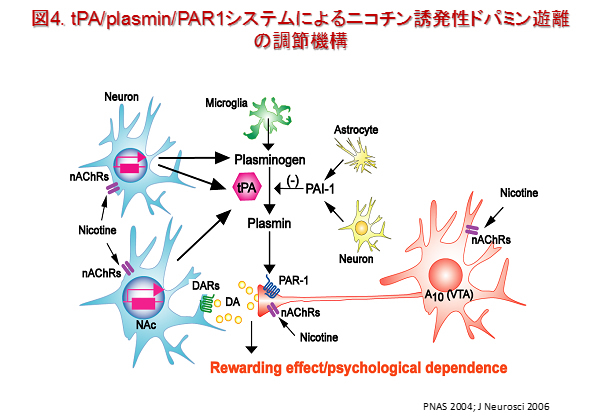
iv) 意思決定障害に関する研究
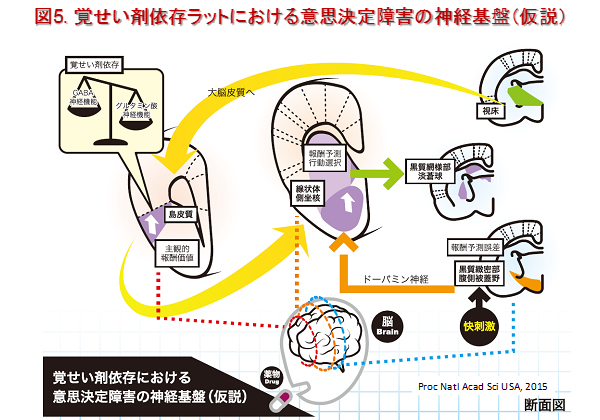
意思決定は日常生活を過ごすための重要な活動要素です。したがって、適切な意思決定を行う能力や起こりうる結果の予測能力の破綻は、社会学的、医療学的および経済学的に重大な問題を引き起こします。物質関連および嗜癖障害のような神経精神疾患患者では意思決定に障害が認められます。おそらく、この意思決定の障害が神経精神疾患で観察される行動障害と関連しているのではないかと考えられます。しかしながら、意思決定障害の神経機序についてはよく分かっていません。私たちはラットを用いた独自のギャンブル試験を開発し、覚せい剤(メタンフェタミン)依存ラットは高リスク/高報酬の選択肢を選ぶ頻度が普通のラットに比べて高くなること、高報酬に対してより高い主観的価値を見出すことを証明しました。したがって、薬物依存状態では意思決定が障害されることを示しました。また、メタンフェタミン依存ラットにおける意思決定の障害機序について研究を進めています(図5)。
2.神経変性疾患に関する研究
i) アルツハイマー型認知症に関する研究
アルツハイマー型認知症は老人斑、神経原繊維変化および神経脱落を伴う進行性の神経変性疾患です。アルツハイマー型認知症の病理学的特徴は、膜貫通型アミロイド前駆タンパク(APP)に由来する39-43個のアミノ酸で構成されるアミロイドβ(Aβ)の沈着です。Aβ繊維の沈着は細胞外に存在する老人斑の中心部で観察され、アルツハイマー型認知症の後期で起こる神経細胞の脱落に関与しています。私たちは、Aβを脳室内に直接注入した動物を用いてAβ誘発性の神経毒性のメカニズムを研究することにより、Aβ誘発性の神経毒性を防ぐ新規化合物を発見することができました。
ii) てんかんに関する研究
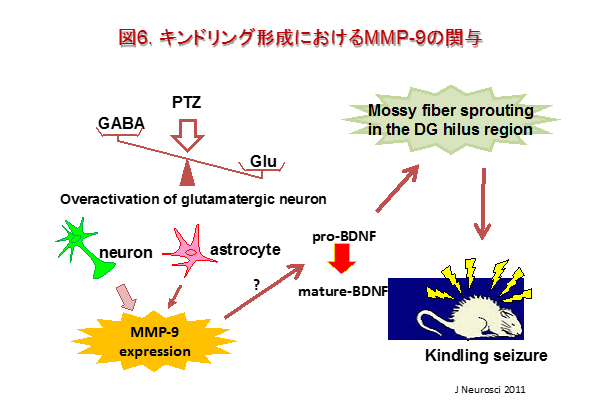
てんかん患者に認められるけいれん発作は、神経学的異常や認知機能障害などの脳に重大な障害を引き起こします。重度のけいれん発作は神経細胞死を惹起しますが、軽度の発作では細胞死を伴わずに神経構造や神経機能を障害することもあります。キンドリングは実験的なてんかんモデルであり、電気刺激や薬物投与により動物の脳に繰り返し刺激を与えると、脳波や行動で認められるけいれん発作の強度が次第に増大します。一旦形成されたキンドリングはけいれん発作に対する脆弱性が恒常的に形成された状態にあり、自発的なてんかん様のけいれん発作として出現します。キンドリングは脳内で、海馬歯状回顆粒細胞から伸びる苔状繊維の異常発芽や海馬の神経細胞脱落などの多様な構造変化を引き起こすことが示されています。ペンチレンテトラゾールを反復投与したキンドリングモデルマウスを用いて、私たちは永続的な構造変化の多様性を生み出すてんかん発作の脆弱性を規定する分子機構について研究しています(図6)。
3. 学習・記憶および他の高次脳機能の神経基盤に関する研究
i) 認知記憶に関する研究
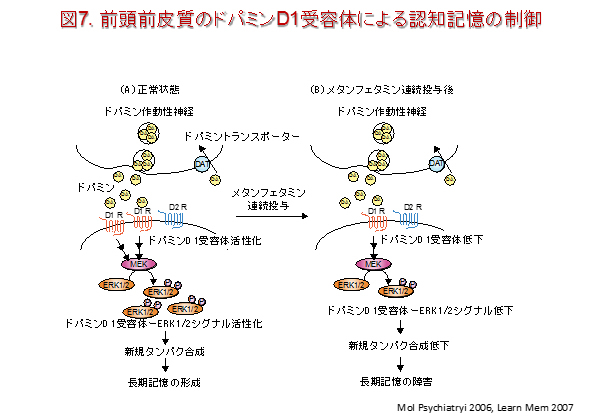
認知記憶は物事を判別して覚えるための能力を担っており、認知症ではこの記憶に障害が認められます。新奇な事象と馴化した事象を弁別する能力は、認知記憶によって生み出されています。この能力は、実験動物でも保存されているため認知記憶に関する基礎研究が盛んに行われています。例えば、嗅周皮質が損傷したり、一時的に嗅周皮質の機能を抑制したサルやネズミは、新奇物体を弁別する試験の遂行能力が低下します。これらの知見から認知記憶に関する最近の研究では、嗅周皮質との関連性に関心が寄せられています。私たちは、前頭前皮質に存在するドパミンD1受容体の刺激がERK1/2の活性化を介して新規タンパク質合成を伴う長期間保持される認知記憶の形成に必要であることを示しました(図7)。現在では、ドパミン作動性神経系とグルタミン酸作動性神経系がどのように協調してタンパク質合成依存的な認知記憶を生み出しているのかについて注目しています。さらに、ドパミンD1受容体とERK1/2シグナルの標的分子についても探索しています。
ii) 神経可塑性に関する研究
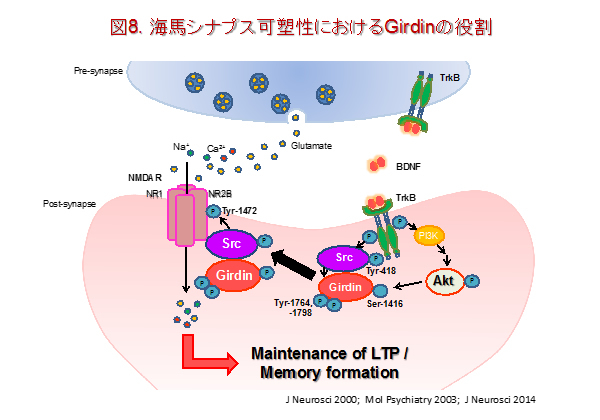
海馬神経のシナプス可塑性は種々の記憶形成に関与していることが知られています。シナプス可塑性は、神経活動に応答する化学的または電気的シナプスにおける伝達効率の強度を反映しています。シナプスにおける神経伝達およびその強度は細胞膜に存在する受容体の発現量や細胞外への神経伝達物質遊離量、神経突起の伝導速度、受容体サブユニットのリン酸、細胞内カルシウム量や細胞骨格リモデリングなど様々な要因によって調節されています。また、神経栄養因子は、シナプス可塑性に関与する重要な分子であると考えられています。例えば、脳由来神経栄養因子(BDNF)やその受容体であるTrkBは、学習・記憶に関する神経生物学的基盤の主要な要素です。私たちは、BDNFがTrkBを介したPI3K/Akt経路の活性化が空間記憶に重要なシグナルであることを明らかにしています。また、TrkBはセリン/スレオニンリン酸化酵素のAktを活性化して様々なリン酸化基質を介して脳発達、老化、神経変性疾患や精神疾患に関連していることが知られています。Girdin(APE, GIV, HkRP1)は、Aktの基質として同定されている分子です。私たちは、Girdinが神経活動依存的にリン酸化され、リン酸化したGirdinがスパインの形態変化、長期増強の維持および記憶形成に必要であることを明らかにしました。さらに、GirdinがSrcやNMDA受容体NR2Bサブユニットと結合することによりNMDA受容体を活性化することを示しました。したがって、Girdinは、BDNF/TrkB/Aktシグナルと海馬記憶の基盤となる神経可塑性を調節するNMDA受容体を繋ぐ重要な分子として作用しているのです(図8)。
iii) 情動行動に関する研究
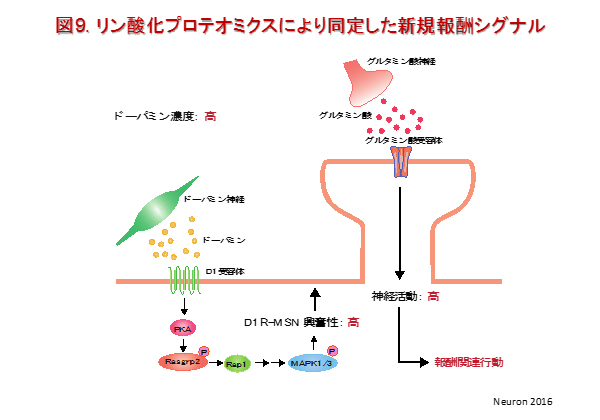
近年では、ドパミンD1受容体の下流に存在するリン酸化シグナルの網羅的なリン酸化プロテオミクス解析を学内共同研究で実施し(神経情報薬理学 貝淵弘三教授と共同研究)、プロテインキナーゼA(PKA)のリン酸化基質を多数同定することに成功しました。さらに、側坐核のドパミンD1受容体を発現する中型有棘神経細胞の興奮性と報酬関連行動を制御する細胞内シグナルを明らかにしました(図9)。
教員
| 構成員名 | 役職 | 所属 |
|---|---|---|
| 池末裕明 | 教授 | 医療薬学/薬剤部 |
| 溝口博之 | 准教授 | 医療薬学/薬剤部 |
| 松崎哲郎 | 特任助教 | 医療薬学/薬剤部 |
研究実績
- 2016年
- Itoh N, Enomoto A, Nagai T, Takahashi M, Yamada K. Molecular mechanism linking BDNF/TrkB signaling with the NMDA receptor in memory: The role of Girdin in the CNS. Rev Neurosci., 2016; 27: 481-90.
- Aoyama Y, Toriumi K, Mouri A, Hattori T, Ueda E, Shimato A, Sakakibara N, Soh Y, Mamiya T, Nagai T, Kim HC, Hiramatsu M, Nabeshima T, Yamada K. Prenatal nicotine exposure impairs the proliferation of neuronal progenitors, leading to fewer glutamatergic neurons in the medial prefrontal cortex. Neuropsychopharmacology, 2016; 41: 578-589.
- Nagai T, Nakamuta S, Kuroda K, Nakauchi S, Nishioka T, Takano T, Zhang X, Tsuboi D, Funahashi Y, Nakano T, Yoshimoto J, Kobayashi K, Uchigashima M, Watanabe M, Miura M, Nishi A, Kobayashi K, Yamada K, Amano M, Kaibuchi K. Phospho-proteomics of the dopamine pathway enables discovery of Rap1 activation as a reward signal in vivo. Neuron, 2016; 89: 550-565.
- 2015年
- Ibi D, Yamada K. Therapeutic targets for neurodevelopmental disorders emerging from animal models with perinatal immune activation. Int. J. Mol. Sci., 2015; 16: 1-12 (doi:10.3390/ijms161226092)
- Mizoguchi H, Katahira K, Inutsuka A, Fukumoto K, Wang T, Nagai T, Sato J, Sawada M, Ohira H, Yamanaka A, Yamada K. Insular neural system controls decision-making in healthy and methamphetamine-treated rats. Proc. Natl. Acad. Sci. USA., 2015; 112: E3930-3939.
- Furukawa-Hibi Y, Yun J, Nagai T, Yamada K. Stress increases DNA methylation of the neuronal PAS domain 4 (Npas4) gene. Neuroreport, 2015; 26: 827-832.
- Nakajima A, Aoyama Y, Shin, EJ, Nam Y, Kim HC, Nagai T, Yokosuka A, Mimaki Y, Yokoi, T, Ohizumi Y, Yamada K. Nobiletin, a citrus flavonoid, improves cognitive impairment and reduces soluble Aβ levels in a triple transgenic mouse model of Alzheimer's disease (3XTg-AD). Behav. Brain Res., 2015; 289: 69-77.
- Yamada K, Nabeshima T. Pharmacist-managed clinics for patient education and counseling in Japan: current status and future perspectives. J. Pharm. Health Care Sci., 2015; 1: 2 (doi:10.1186/s40780-014-0001-4)
- Ichikawa K, van Ingen J, Koh WJ, Wagner D, Salfinger M, Inagaki T, Uchiya KI, Nakagawa T, Ogawa K, Yamada K, Yagi T. Genetic diversity of clinical Mycobacterium avium subsp. hominissuis and Mycobacterium intracellulare isolates causing pulmonary diseases recovered from different geographical regions. Infect Genet Evol., 2015; 36: 250-255.
- Yamamura K, Yano K, Kirooka Y, Hirashiki A, Murohara T, Yamada K. A successful case of a ptient undergoing warfarin and S-1 therapy using internet-based control of hemo-measured PT-INR. YAKUGAKU ZASSHI, 2015; 135: 925-927.
- Kato H, Miyazaki M, Takeuchi M, Tsukuura H, Sugishita M, Noda N, Yamada K. A retrospective study to identify risk factors for somnolence and dizziness in patients treated with pregabalin. J. Pharm. Health Care Sci., 2015; 1: 22 (10.1186/s40780-015-0022-7).
- 2014年
- Nakai T, Nagai T, Tanaka M, Itoh N, Asai N, Enomoto A, Asai M, Yamada S, Saifullah MAB, Sokabe M, Takahashi M, and Yamada K. Girdin phosphorylation is crucial for synaptic plasticity and memory: a potential role in the interaction of BDNF/TrkB/Akt signaling with NMDA receptor. J. Neurosci., 2014; 34: 14995-15008.
- Nakajima A, Ibi D, Nagai T, Yamada S, Nabeshima T, Yamada K. Induction of interferone-induced transmembrane protein 3 gene expression by lipopolysaccharide in astrocytes. Eur. J. Pharmacol., 2014; 745: 166-175.
- Yamada S, Nagai T, Nakai T, Ibi D, Nakajima A, Yamada K: Matrix metalloproteinase-3 is a possible mediator of neurodevelopmental impairment due to polyI:C-induced innate immune activation of astrocytes. Brain Behav Immun., 2014; 38: 272-282.
- Nakai T, Nagai T, Wang R, Yamada S, Kuroda K, Kaibuchi K, Yamada K: Alterations of GABAergic and dopaminergic system in mutant mice with disruption of exons 2 and 3 of the Disc1 gene. Neurochem. Int., 2014; 74: 74-83.
- Nakajima N, Ohizumi Y, Yamada K. Anti-dementia activity of nobiletin, a citrus flavonoid. Clin. Psychopharmacol. Neurosci., 2014; 12: 75-82.
- 2013年
- Mizoguchi H, Yamada K. Roles of matrix metalloproteinases and their targets in epileptogenesis and seizures. Clin. Psychopharmacol. Neurosci., 2013; 11:45-52.
- Mouri A, Nagai T, Ibi D, Yamada K. Animal models of schizophrenia for molecular and pharmacological intervention and potential candidate molecules. Neurobiol. Dis., 2013; 53: 61-74.
- Nakajima A, Aoyama Y, Nguyen TTL, Shin EJ, Kim HC, Yamada S, Nakai T, Nagai T, Yokosuka A, Mimaki Y, Ohizumi Y, Yamada K. Nobiletin, a citrus flavonoid, ameliorates cognitive impairment, oxidative burden, and hyperphosphorylation of tau in senescence-accelerated mouse. Behav. Brain Res., 2013; 250: 351-360.
- Miyazaki M, Noda Y, Mouri A, Kobayashi K, Mishina M, Nabeshima N, Yamada K. Role of convergent activation of glutamatergic and dopaminergic systems in the nucleus accumbens in the development of methamphetamine psychosis and dependence. Int. J. Neuropsychopharmacol., 2013; 16: 1341-1350.
- Yun J, Nagai T, Furukawa-Hibi Y, Kuroda K, Kaibuchi K, Yamada K. Neuronal Per Arnt Sim (PAS) domain protein 4 (Npas4) regulates neurite outgrowth and phosphorylation of synapsin I. J. Biol. Chem., 2013; 288: 2655-2664.
- Ibi D, Nagai T, Nakajima A, Mizoguchi H, Kawase T, Tsuboi D, Kano S, Sato Y, Hayakawa M, Lange UC, Adams DJ, Surani MA, Satoh T, Sawa A, Kaibuchi K, Nabeshima T, Yamada K. Astroglial IFITM3 mediates neuronal impairments following neonatal immune challenge in mice. Glia, 2013; 61: 679-693.
- 2012年
- Furukawa-Hibi Y, Nitta A, Fukumitsu H, Somiya H, Toriumi K, Furukawa S, Nabeshima T, Yamada K. Absence of SHATI/Nat81 reduces social interaction in mice. Neurosci. Lett., 2012; 526: 79-84.
- Nagai T, Yu J, Kitahara Y, Nabeshima T, Yamada K. D-serine ameliorates neonatal polyI:C treatment-induced emotional and cognitive impairments in adult mice. J. Pharmacol. Sci., 2012; 120: 213-227.
- Furukawa-Hibi Y, Yun J, Nagai T, Yamada K. Transcriptional suppression of the neuronal PAS domain 4 (Npas4) gene by stress via the binding of agonist-bound glucocorticoid receptor to its promoter. J. Neurochem., 2012; 123: 866-875.
- Watanabe N, Yamamura K, Suzuki Y, Umegaki H, Shigeno K, Sai Y, Miyamoto K, Yamada K. Pharmacist-based donepezil outpatient consultation service to improve medication persistence. Patient Preference Adherence, 2012; 6: 1-7.
- Takuma K, Mizoguchi H, Funatsu Y, Kitahara Y, Ibi D, Kamei H, Matsuda T, Koike K, Inoue M, Nagai T, Yamada K. Placental extract improves hippocampal neuronal loss and fear memory impairment resulting from chronic restraint stress in ovariectomized mice. J. Pharmacol. Sci., 2012; 120: 89-97.
- Mizuno T, Sato W, Ishikawa K, Shinjo H, Miyagawa Y, Noda Y Imai E, Yamada K. KDIGO criteria could be useful outcome predictor of cisplatin-induced acute kidney injury. Oncology, 2012; 82: 354-359.
- Takuma K, Mizoguchi H, Funatsu Y, Hoshina Y, Himeno Y, Fukuzaki E, Kitahara Y, Arai S, Ibi D, Kamei H, Matsuda T, Koike K, Inoue M, Nagai T, Yamada K. Combination of chronic stress and ovariectomy causes conditioned fear memory deficits and hippocampal cholinergic neuronal loss in mice. Neuroscience, 2012; 207: 261-273.
- Mizuno T, Ito K, Miyagawa Y, Kimura K, Suzuki Y, Mizuno M, Ito Y, Funahasi Y, Hattori R, Gotoh M, Noda Y, Yamada K. Renal impairment after laparoscopic radical nephrectomy affects hypoglycaemic therapy. J Clinic. Pharm. Therapeu., 2012; 37: 49-52.
- 2011年
- Mizoguchi H, Nakade J, Tachibana M, Ibi D, Someya E, Koike H, Kamei H, Nabeshima T, Itohara S, Takuma K, Sawada M, Sato J, Yamada K. Matrix metalloproteinase-9 contributes to kindlined seizure development in pentylenetetrazole-treated mice by converting pro-BDNF to mature BDNF in the hippocampus. J Neurosci., 2011; 31: 12963-12971.
- Kuroda K, Yamada S, Tanaka, Iizuka M, Yano H, Mori D, Tsuboi D, Nishioka T, Namba T, Iizuka Y, Kubota S, Nagai T, Ibi D, Wang R, Enomoto A, Isotani-Sakakibara M, Asai N, Kimura K, Kiyonari H, Abe T, Mizoguchi A, Sokabe M, Takahashi M, Yamada K, Kaibuchi K. Behavioral alterations associated with targeted disruption of exons 2 and 3 of the DISC1 gene in the mouse. Hum. Mol. Genet., 2011; 20: 4666-4683.
- Furukawa-Hibi Y, Alkam T, Nitta A, Matsuyama A, Mizoguchi H, Suzuki K, Moussaoui S, Yu Q-S, Greig NH, Nagai T, Yamada K: Butyrylcholinesterase inhibitors ameliorate cognitive dysfunction induced by amyloid-ß peptide in mice. Behav Brain Res., 2011; 225: 222-229.
- Nagai T, Kitahara Y, Ibi D, Nabeshima T, Sawa A, Yamada K: Effects of antipsychotics on the behavioral deficits in human dominant-negative DISC1 transgenic mice with neonatal polyI:C treatment. Behav. Brain Res., 2011; 225: 305-310.
- Ishizuka M, Fujimoto Y, Itoh Y, Sano M, Miyagawa Y, Ando A, Hiramatsu M, Hirasawa N, Ishihara S, Nabeshima T, Yamada K. Relationship between hematotoxicity and serum albumin level in the treatment of head and neck cancers with concurrent chemoradiotherapy using cisplatin. Jpn. J. Clin. Oncol., 2011; 41: 973-979.
- Furukawa-Hibi Y, Nitta A, Ikeda T, Morishita K, Liu W, Ibi D, Alkam T, Nabeshima T, Yamada K. The hydrophobic dipeptide Leu-Ile inhibits immobility induced by repeated forced swimming via the induction of BDNF. Behav Brain Res., 2011; 220: 271-280.
- Mizoguchi H, Ibi D, Takase F, Nagai T, Kamei H, Toth E, Sato J, Takuma K, Yamada K. Nicotine ameliorates impairment of working memory in methamphetamine-treated rats. Behav. Brain Res., 2011; 220: 159-163.
研究キーワード
意思決定、学習記憶、情動、神経精神疾患、動物モデル、薬物依存