消化器外科学
KEYWORDS
- 消化器癌
- 炎症の病態解明と外科臨床研究
HEAD

LAB MEMBER
| 構成員名 | 役職 | 研究者総覧 |
|---|---|---|
| 田中 千恵 | 病院准教授 | 研究者総覧 |
| 林 真路 | 講師 | 研究者総覧 |
| 髙見 秀樹 | 病院講師 | 研究者総覧 |
| 清水 大 | 病院講師 | 研究者総覧 |
| 佐藤 雄介 | 病院講師 | 研究者総覧 |
| 田中 晴祥 | 病院講師 | 研究者総覧 |
| 中西 香企 | 病院講師 | 研究者総覧 |
| 梅田 晋一 | 助教 | 研究者総覧 |
| 栗本 景介 | 病院助教 | 研究者総覧 |
| 筒山 将之 | 病院助教 | 研究者総覧 |
| 中川 暢彦 | 助教 | 研究者総覧 |
| 笹原 正寛 | 病院助教 | 研究者総覧 |
| 飯塚 彬光 | 病院助教 | 研究者総覧 |
| 中村 正典 | 病院助教 | 研究者総覧 |
CONTACT
| surg2◎med.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | 消化器外科学 独自ホームページ |
OUTLINE
優れた外科医を育成し、臨床・研究の両面で世界に発信する
当教室は、消化器外科領域において、確かな臨床力と高度な研究力を併せ持つ外科医の育成を使命としています。臨床においては、教室伝統のがん手術の基本を忠実に継承しつつ、機能温存・低侵襲手術から拡大根治手術に至るまで、科学的根拠に基づいた最先端の外科治療を実践しています。
研究面では、消化器がんおよび炎症性腸疾患を主軸に、バイオマーカー探索や創薬研究など、新規治療法の開発を目指した基礎・臨床研究を積極的に推進しています。豊富な臨床経験と最新の知見を融合させ、世界に発信可能な研究成果を創出するとともに、次世代を担う外科医の育成にも注力しています。
近年、全国的な外科医減少は深刻な社会問題となっています。当教室ではこれに先駆け、腹腔鏡手術およびロボット支援下手術を中心とした体系的な修練環境の整備に加え、若手外科医が継続的に成長できる教育体制、ならびに女性医師を含む多様な人材が長期的に活躍できる労働環境の構築に取り組んでいます。
外科医には、卓越した手術手技のみならず、幅広い医学知識と総合的判断力、そして重症患者およびその家族と真摯に向き合い、協働して疾患に立ち向かう高い倫理観と人間性が求められます。その重責の先にある外科医としての達成感と誇りを、知識・技術とともに、次世代の医療を担う若手医師へと伝えていきたいと考えています。当教室は各関連病院と密接に連携し、まず外科学会専門医取得を前提とした、偏りのない総合的な臨床能力の修得を重視します。その後、最短で消化器外科学会専門医を取得できるよう、豊富な症例を経験できる環境を提供します。また、特定の分野に偏らない広い視野を備えた外科医を育成するため、可能な限り多くの指導医から指導を受けられる修練体制を整えています。
これらの教育・臨床基盤を礎として、大学院医学研究科における高度な専門性の追求へとつなげ、国内外へ発信する基礎・臨床研究の展開を目指します。先人から受け継いだ外科の伝統と最先端医療を融合させ、「優れた外科医を育成し、臨床・研究の両面で世界に発信する」ことが、教室全体の到達目標です。
RESEARCH PROJECTS
1. 食道グループ
- 食道癌における癌関連遺伝子の網羅的検索と発現機能解析
- 食道がんに対するダビンチ手術システムを用いたロボット支援下食道切除術の有効性と安全性を検証する研究
- 進行食道癌に対する術前 Docetaxel+Oxaliplatin+S-1療法の有効性と安全性を検討する臨床第II相試験(CCOG2102)
- 食道癌患者を対象とした術前補助化学療法後の術直前栄養介入の有効性に関する研究(CCOG2103)
- 食道癌周術期における、振動型呼気陽圧療法の研究(CCOG2302)
- 臨床病期I-IVA(T4を除く)胸部上中部食道扁平上皮癌に対する予防的鎖骨上リンパ節郭清省略に関するランダム化比較試験(JCOG2013)
- 食道胃接合部腺癌に対するDOS or FLOTを用いた術前化学療法のランダム化第II/III相試験(JCOG2203)
- 術前化学療法後に根治手術が行われ病理学的完全奏効とならなかった食道扁平上皮癌における術後無治療/ニボルマブ療法/S-1療法のランダム化比較第III相試験(JCOG2206)
2. 胃グループ
1. 新規胃癌腹膜播種特異的分子標的治療薬の開発
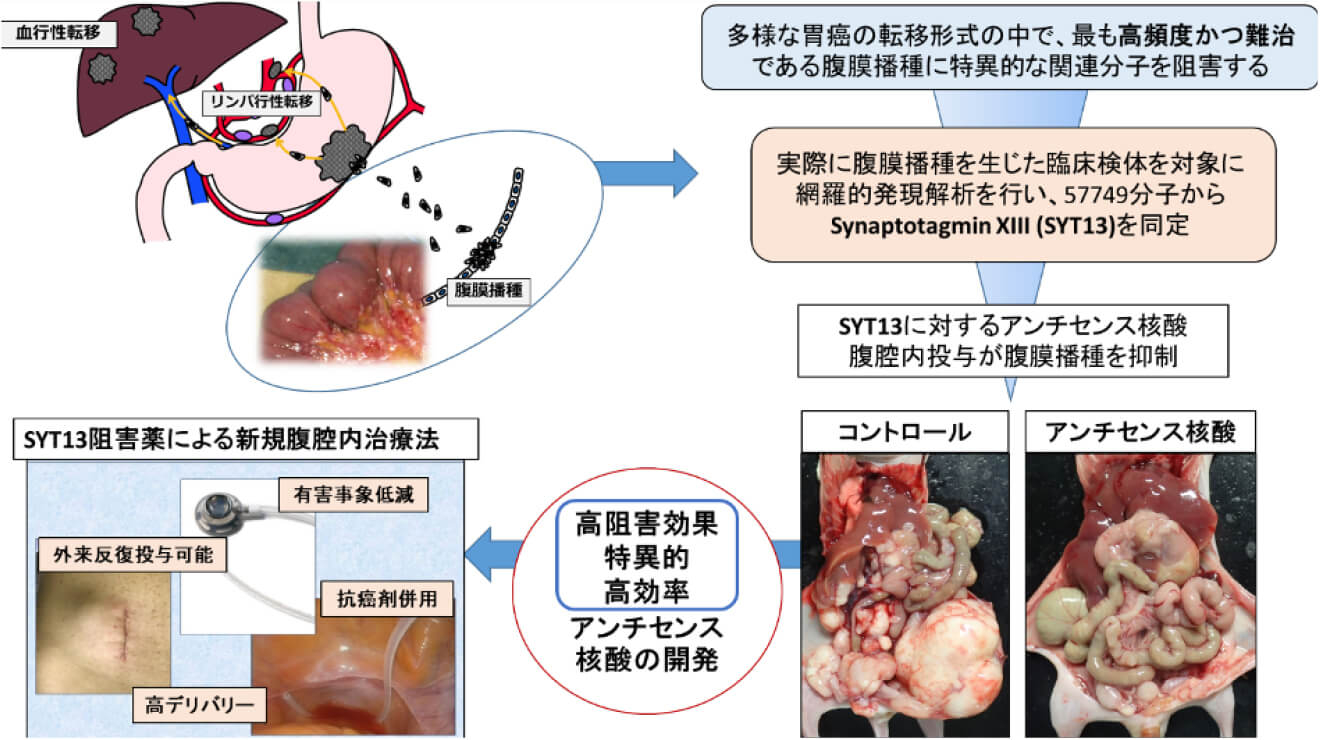
腹膜播種は胃癌において高頻度に認められる転移再発様式であり、依然として治療抵抗性が高く、予後を規定する重要な因子です。当教室では、胃癌腹膜播種に特異的に高発現し、その形成・進展に深く関与する分子 SYT13 に着目し、基礎研究から創薬研究へと一貫したトランスレーショナルリサーチを進めてきました。これまでに、SYT13を標的とするアミド架橋型人工核酸を搭載したアンチセンス核酸医薬 ASO-4733 を創製し、腹膜播種モデルにおいて有効性と安全性を示す非臨床データを蓄積してきました。これらの成果を基盤として、現在は 腹膜播種を有する切除不能進行・再発胃癌を対象とした第I相医師主導治験 を実施しており、腹腔内投与という新たな治療戦略の臨床的妥当性を検証してます。
2. 転移形式別Transcriptome解析による胃癌肝転移特異的バイオマーカーの研究
肝転移に代表する胃癌の血行性転移は多くの分子が関与する多段階の過程を経て形成されることが知られていますが、その中には転移経路に特異的な分子が存在すると考えています。そこで、肝転移・再発をきたした症例に特異的に発現異常を認める分子を網羅的発現解析から同定し、その胃癌肝転移診断・予測バイオマーカーとしての有用性を研究しています。
3. ICGによる新しい早期胃癌マーキング法の研究
4.胃癌手術における高齢者機能評価に関する研究
5.内視鏡手術シミュレーション訓練の新しい統合的基本タスク作成
6.胃癌術後患者におけるアナモレリン塩酸塩投与の術後補助化学療法相対用量強度に与える影響に関する無作為化比較試験
7.大規模検診でのスクリーニング、がん診断、治療方針決定のための進行度診断、治療の効果判定、切除術後の再発モニタリングのいずれの場面においても、非侵襲的かつ簡便に採取可能な血清がんマーカーが切望されています。当科では独自に発見した血清マーカーに対する測定キットを構築し、これを検証するための韓国・米国との国際共同前向き研究を行っています。
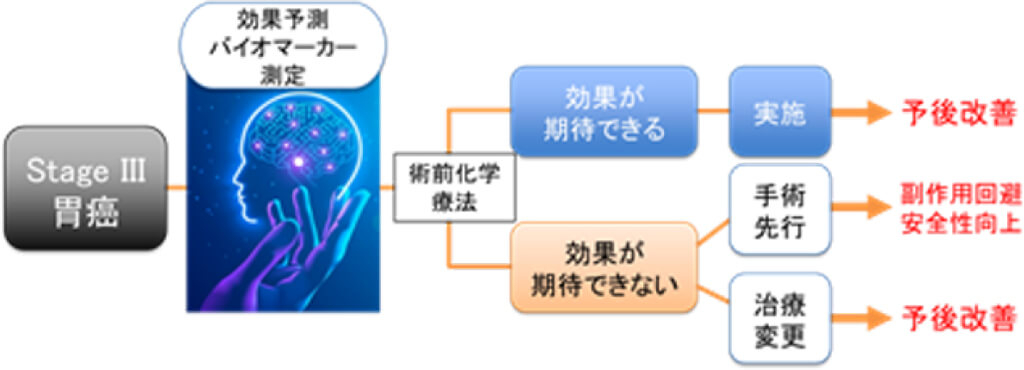
8. 進行胃癌術前化学療法の効果予測バイオマーカー開発
研究血液検体、組織検体を用いたマルチオミクスデータをAI解析することで、高性能かつ新規性の高い進行胃癌術前化学療法の効果予測バイオマーカー同定を試みています。
3. 肝臓グループ
1. 肝細胞癌の進行に寄与すると想定されるメチル化遺伝子の同定
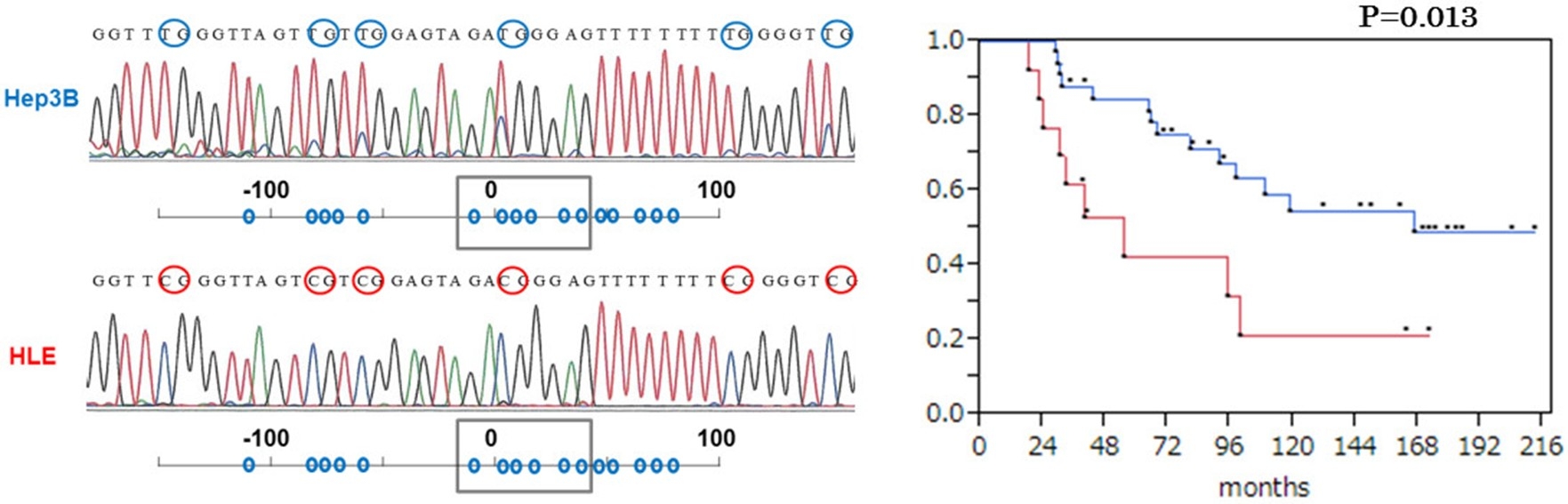
肝細胞癌細胞株のbisulfite検体をシークエンスすると、Hep3B(中分化癌)ではCpGサイトがTGである(メチル化陰性)のにたいし、HLE(未分化癌)ではCpGサイトがCGに変化していた(メチル化陽性)。肝細胞癌切除検体において、メチル化陽性症例(赤線)は陰性症例(青線)と比較して術後全生存率が有意に不良であった。(BMC Cancer, 2014)。
2. 胆道再建のない肝切除症例における周術期ICG-K値測定と術後肝不全予測
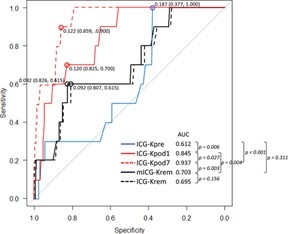
術前ICG-K値(ICG-Kpre)、術後残肝ICG-K値(mICG-Krem)検査に加え、術後1日目のICG-K値(ICG-Kpod1)、術後7日目のICG-K値(ICG-Kpod7)を測定し、術後肝不全(Grade B/C)との相関関係を評価した。mICG-KremはICG-Kpod1、ICG-Kpod7とよく相関していた。多変量解析ではICG-Kpod7、および術後胆汁瘻が有意な肝不全予測因子となった(J Hepatobiliary Pancreatic Sci, 2021)。
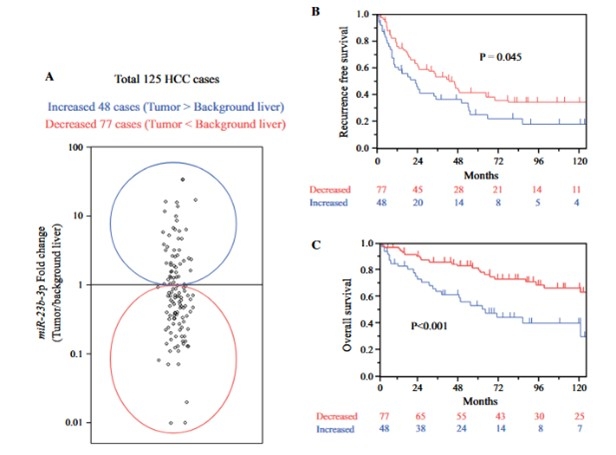
3. 肝細胞癌組織でのmiR-23b発現上昇は肝切除後予後不良因子となる
肝細胞癌において、背景肝と比較して癌部でmiR-23b発現が上昇する症例は、有意に肝切除術後の予後が不良であった。miR-23bの発現上昇は、ミトコンドリア機能維持に関与するMICU3やAUH遺伝子の発現低下を招き、癌細胞の悪性化に関与すると考えられた(Ann Surg Oncol, 2021)。
4. 膵臓グループ
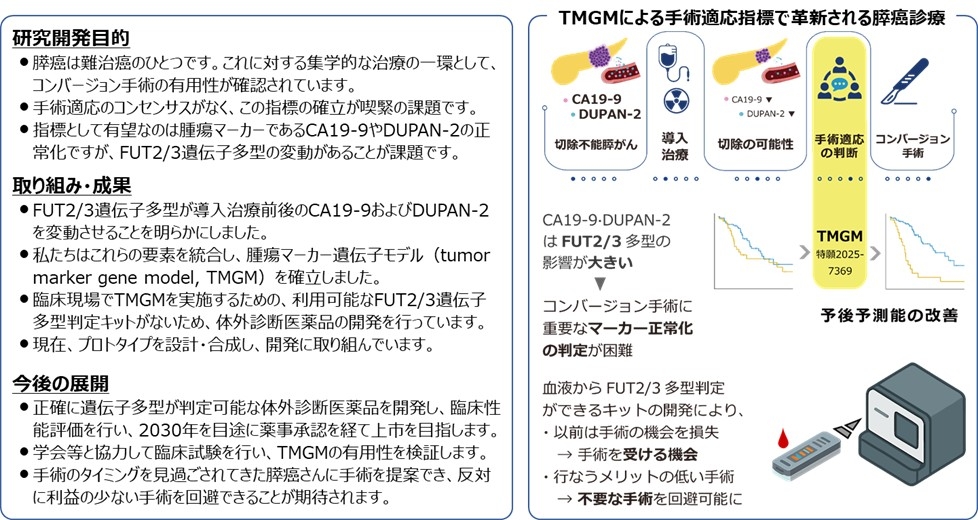
1. 進行膵がんに対する腫瘍マーカー遺伝子モデルの開発:進行膵臓がんに対しては集学的治療の一環として適切な時期に手術することが重要です。手術の可否の判断には腫瘍マーカー、とくにCA19-9やDUPAN-2などが参考になりますが、その個人差が課題でした。私たちは、CA19-9・DUPAN-2とFUT2・FUT3遺伝子多型を組み合わせた腫瘍マーカー遺伝子モデル(Tumor marker gene model; TMGM)を開発し、これが高い予後予測能を示しました。現在TMGMを手術適応判断の参考となるモデルとして臨床応用するために、FUT2/3遺伝子多型判定キットの開発を行っています。
Tanaka H, Sakai A, Suenaga M, et al. FUT2 and FUT3-specific normalization of DUPAN-2 and carbohydrate antigen 19-9 in preoperative therapy for pancreatic cancer: multicentre retrospective study (GEMINI-PC-01). Br J Surg. 2025;112:znaf049.
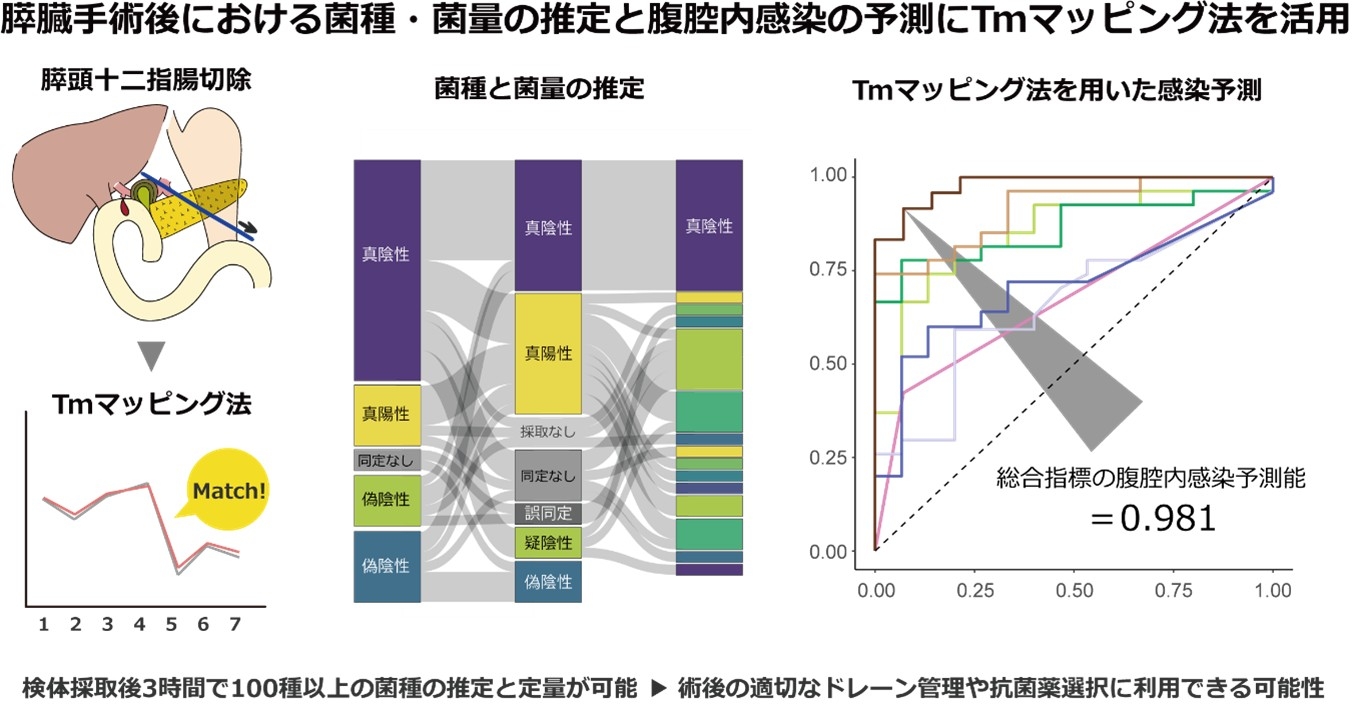
2. 膵頭十二指腸切除術の安全な周術期感染対策に関する研究:当科では富山大学と共同研究として、術後感染症を予測する新規迅速細菌検査技術の臨床応用に向けた研究開発を行っています。膵頭十二指腸切除術は負担の大きな消化器外科手術のひとつで、その術後の腹腔内感染は依然として重要な課題です。膵切除術後の腹腔内感染症のコントロールは今でも重要な課題です。従来の細菌培養やグラム染色検査は、迅速性や詳細さに限界がありました。新技術 「Tmマッピング法」 は最短約3時間で原因菌の“種類と量”を推定します。今回、膵頭十二指腸切除術後の患者さんでその有用性を検証しました。Tmマッピングを含む予測モデルのAUCは0.981で、術後管理の意思決定の質向上が期待されました。
Tanaka H, Fukasawa M, Kimura N, et al. A novel melting temperature mapping method may improve the prediction of postoperative intra-abdominal infection after pancreatoduodenectomy. Br J Surg. 2025 Oct 3;112:znaf222.
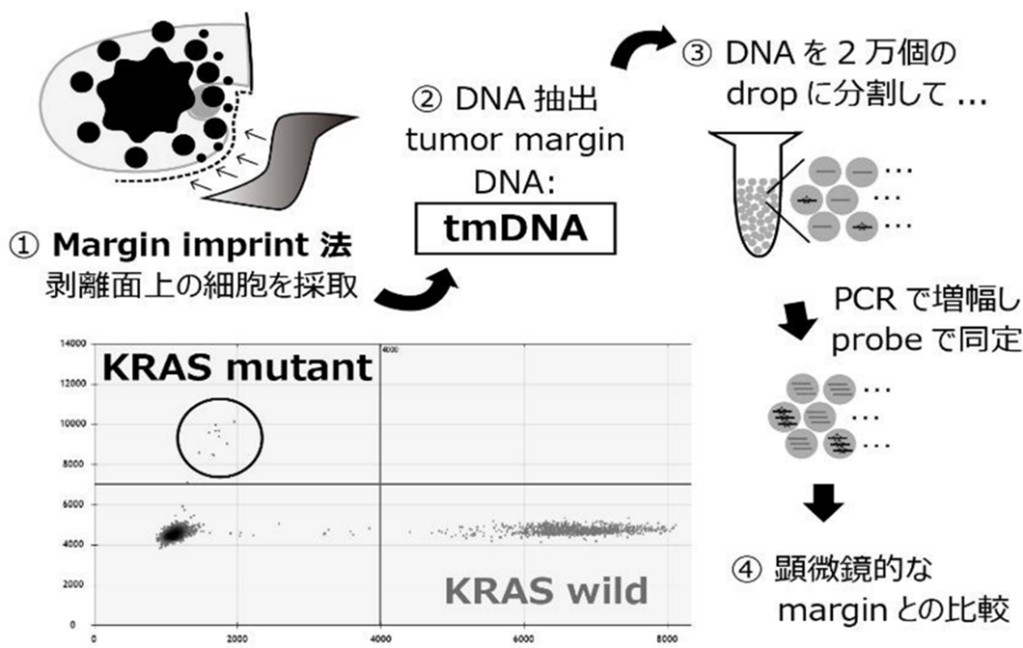
3. マージンインプリントデジタルPCR法を用いた分子生物学的な膵周囲剥離面断端診断法の開発Development of diagnostics for pancreatic cancer's molecular Resection margin status at dissected peripancreatic tissue margin by margin imprint droplet digital PCR (PIRAMID study): 膵がんは極めて制御困難ながん種のひとつで、肉眼的に全切除したつもりでも、時に顕微鏡的に遺残を認めることがあります。さらには病理学的に完全切除と診断されても、根治切除後に局所で再発することもあります。この課題を克服するために、膵がん切除時のがんの遺残を検出するために分子生物学的なアプローチを試みています。膵がんの外科的剝離面上のがんの存在を分子生物学的に診断するため、独自にmargin imprint デジタルPCR法を確立しました。切除したばかりの膵がん標本の外科剥離面にimprint membraneを貼付することで、凹凸のある広い外科的剥離面から効率的に切除断端上の細胞を回収し、これから抽出した核酸をもちいて、超低頻度のがん細胞を分子生物学的に同定する試みをしています。将来的には実臨床で術後腹腔内の再発を予測する体外診断医薬品としての開発を進めます。
4. 腹腔細胞診陽性膵がんの予測因子の探索:膵がんの予後を左右する要素のひとつに腹腔細胞診陽性、つまり膵がん細胞が腹腔内に浮遊している病態があり、予後不良因子のひとつとされています。私たちは腹腔細胞診陽性の膵がん患者で CA19-9 ≥250 U/mL、DUPAN-2 ≥150 U/mL、切除可能境界である頻度が高いことをあきらかにしました。Tanaka N, Takami H, Hayashi M, et al. Predictive impacts of peritoneal washing cytology for surgical resection-intended pancreatic cancer cases: Establishment of planned staging laparoscopy criteria. J Hepatobiliary Pancreat Sci. 2023;30:1273-1281.
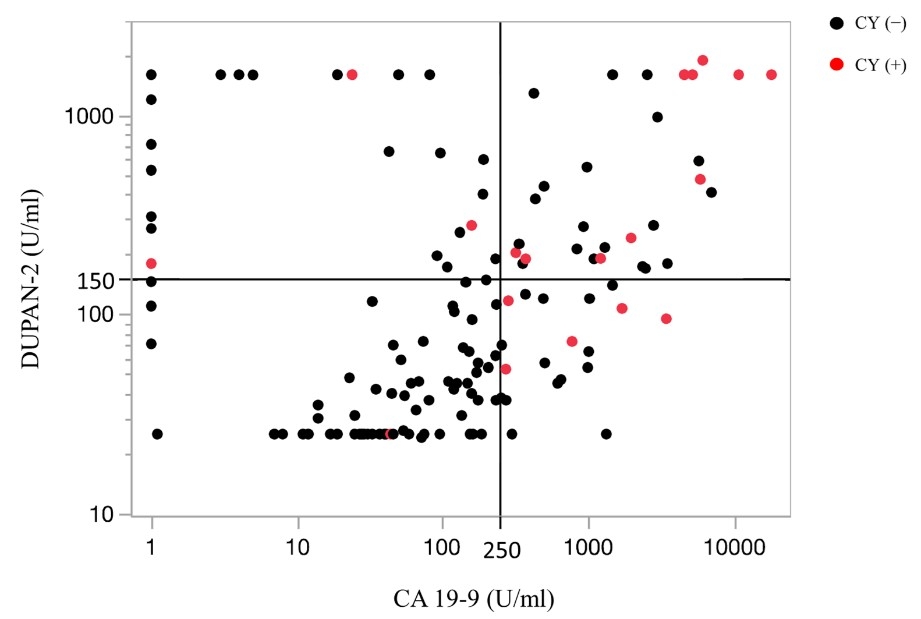
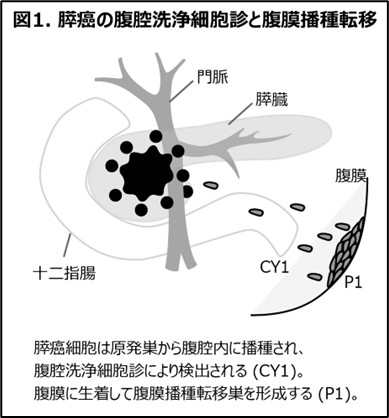
5. 腹腔洗浄細胞診陽性膵がんに対する全身化学療法の有効性を検証するための多施設共同第II相試験 付随研究:腹腔洗浄細胞診陽性膵がんに対する全身化学療法中の効果判定としての腹腔内浮遊腫瘍DNA定量法の有用性の検証および新規バイオマーカーの探索:上述の研究に関連して、腹腔細胞診陽性の膵がんに対して、細胞診が陰性となるまで術前治療を行う戦略の有効性を検証しており、名古屋大学も積極的に参加しています(WALCURE試験)。本研究は富山大学が主導し、現在進行中の臨床試験ですが、本学では、この治療効果をデジタルPCRなどの分子生物学な視点から検証する付随研究事務局を担当しています:
Accompanying study of a multicenter phase II study to investigate the efficacy of systemic chemotherapy in patients with peritoneal washing cytology-positive potentially curable pancreatic cancer: Validation of quantifying peritoneal tumor DNA during systemic chemotherapy to monitor negative conversion of cancerous cytology and exploration for novel biomarkers of pancreatic cancer(WALCURE DRIVE)
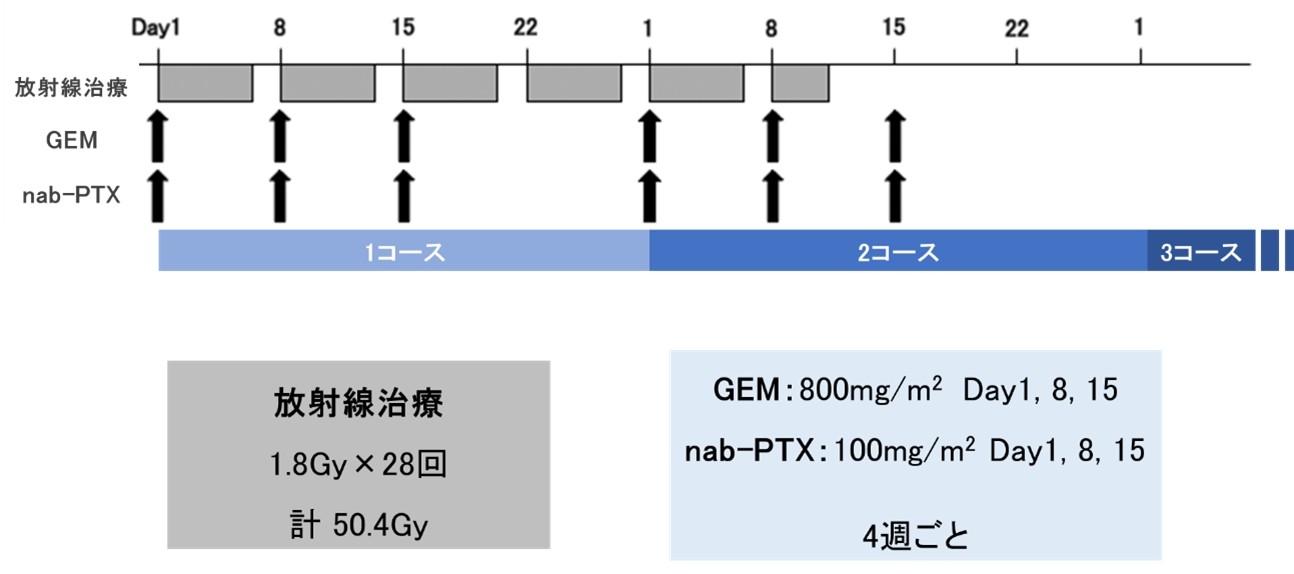
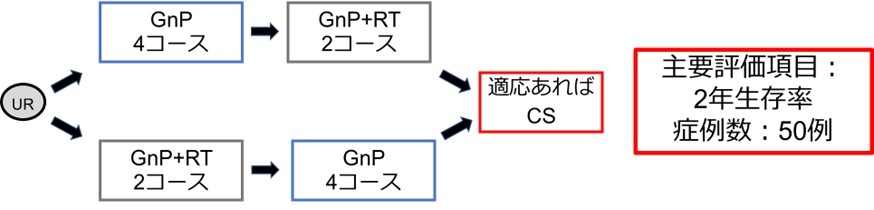
6. 局所進行切除不能膵がんに対するGemcitabine+nab-Paclitaxel併用化学放射線療法の第I相臨床試験(NUPAT-02):遠隔転移のない局所進行膵がんに対して、近年注目されているゲムシタビン・ナブパクリタキセル療法に、放射線治療を組み合わせる化学放射線治療(GnP-CRT)に関する医師主導第I相治験を行い、この推奨治療用量を決定しました。
Yamada S, Fujii T, Yokoyama Y, Kawashima H, Maeda O, Suzuki K, Okada T, Ono E, Yamaguchi J, Takano N, Takami H, Hayashi M, Niwa Y, Hirooka Y, Ito Y, Naganawa S, Ando Y, Nagino M, Goto H, Kodera Y. Phase I study of chemoradiotherapy using gemcitabine plus nab-paclitaxel for unresectable locally advanced pancreatic cancer. Cancer Chemother Pharmacol. 2018;81:815-821.
7. 局所進行切除不能膵がんに対するGemcitabine+nab-Paclitaxel併用化学放射線療法の第II相臨床試験(NUPAT-05):遠隔転移のない局所進行膵がんに対して、近年注目されているゲムシタビン・ナブパクリタキセル療法に、放射線治療を組み合わせることで治療効果の向上を目指し、さらにはコンバージョン手術を検討することで、治療成績の向上を目指す臨床試験を行いました。現在はこの治療成績をまとめ、学術雑誌へ公表する準備段階です。
Phase II study of chemoradiotherapy combined with gemcitabine and nab-paclitaxel for unresectable locally advanced pancreatic cancer.
8. 切除可能境界膵がんに対するnab-PTX+GEM療法±放射線療法併用による術前治療の無作為化比較第Ⅱ相臨床試験 Nagoya University Pancreatic Tumor Board trial 07 (NUPAT-07):外科的切除実施の難易度が高い膵がん(切除可能境界膵がん)に対して、ゲムシタビン・ナブパクリタキセル療法を行っている施設が広く使われています。これに、放射線治療を組み合わせるかどうかを無作為で決め(ランダム化し)、これにつづいて手術を行うことで、放射線治療の上乗せ効果を調べる臨床試験を行っています。
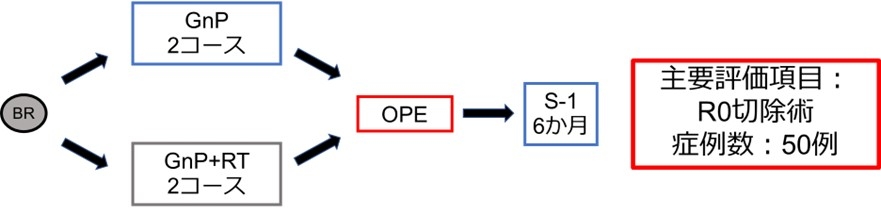
9. 局所進行膵がんに対する放射線療法導入タイミングに関する無作為化比較第Ⅱ相臨床試験 Nagoya University Pancreatic Tumor Board trial 08 (NUPAT-08):外科的切除実施の難易度が高い膵がん(切除可能境界膵がん)に対して、上述のようにゲムシタビン・ナブパクリタキセル療法に放射線治療を組み合わせる臨床試験としてNUPAT-05試験を行い、期待できる治療成績を得ました。しかし、放射線治療後から手術まで時間がたつことで手術自体が困難になる可能性が指摘されています。そこで、NUPAT-05で用いた治療法と、この放射線治療のタイミングを後にする治療法とを比較しすることで、最適な集学的治療戦略を検討する臨床試験を行っています。
5. 大腸グループ
● 大腸癌(Colorectal Cancer)
1.進行・再発大腸癌に対する化学療法の最適化
Phase II study of FOLFIRI with low-dose irinotecan plus ramucirumab as second-line treatment in Japanese patients with metastatic colorectal cancer (RINDO study)
進行再発大腸癌の二次治療として、イリノテカン日本標準量(150 mg/m²)を用いたFOLFIRI+ラムシルマブ療法の有効性・安全性を検証し、論文化した。• Jpn J Clin Oncol. 2025 Dec 8; hyaf198.PMID: 41359440
2.高リスクStage II/Stage III大腸癌における術後補助療法の最適化(CCOG1302)
高リスクStage II/Stage III大腸癌を対象としたCAPOX療法において、オキサリプラチン間欠投与と継続投与を比較する無作為化第II相試験(CCOG1302)の高齢者サブグループ解析を実施。高齢者では継続投与群で末梢神経障害の遺残が有意に多いことを明らかにした。
- Int J Clin Oncol. 2025;30(6):1174–1182.
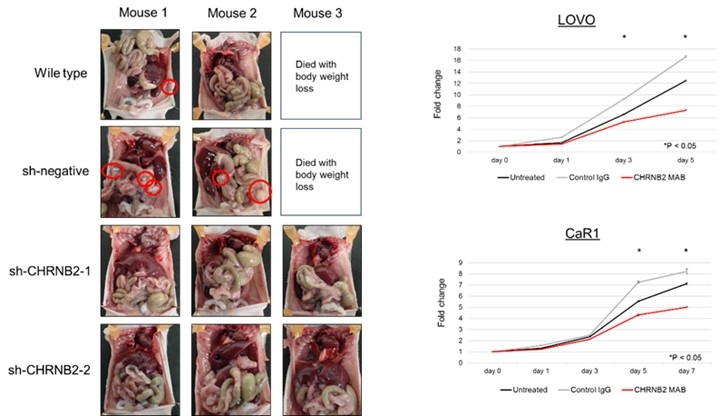
3.腹膜播種関連分子 CHRNB2 の同定と機能解析
大腸癌切除検体を用いた解析により、CHRNB2高発現症例では腹膜播種が特異的に多いことを示した。さらに細胞株およびマウス腹膜播種モデルを用いて、CHRNB2抑制や抗体投与により腹膜播種および腫瘍増殖が抑制されることを明らかにし、治療標的としての可能性を示した。
- Cancers (Basel). 2025;17(15):2485.
4.大腸癌における新規予後予測バイオマーカー探索(進行中)
大腸癌切除検体および細胞株を用いた解析により、GABRD、SLC7A9、FTCD、TTYH1 が大腸癌の予後と相関する可能性を見出しており、現在機能解析および臨床的意義の検証を進めている。
● 炎症性腸疾患(IBD)
1.IBD術後における門脈血栓症の発生頻度と危険因子解析(進行中)
潰瘍性大腸炎およびクローン病術後1週間で造影CTを施行し、門脈血栓症を含む静脈血栓塞栓症の発生率および危険因子を同定する前向き観察研究を実施している。
2.肛門周囲瘻孔を有するクローン病に対するグセルクマブ第III相試験
クローン病痔瘻患者を対象として、グセルクマブの有効性・安全性を評価する多施設共同第III相臨床試験に参加している。
3.クローン病腸管切除例に対する三角吻合法の検証(CCOG2503)
クローン病の腸管吻合において、自動縫合器を用いた端々三角吻合法が縫合不全を減少させ、術後内視鏡通過性を改善するという仮説のもと、前向き研究を実施中である。
4.潰瘍性大腸炎術後一時的回腸人工肛門患者に対する柴苓湯のHOS予防効果検証
大腸癌のカバリングイレオストミーにおいて有用性が報告されている漢方薬・柴苓湯について、潰瘍性大腸炎術後一時的回腸人工肛門患者におけるHigh-output stoma(HOS)予防効果を検証する臨床試験を進めている。
5.潰瘍性大腸炎における薬剤耐性および癌化関連遺伝子の網羅的解析(進行中)
潰瘍性大腸炎切除検体を用い、
- インフリキシマブ抵抗性粘膜
- colitic cancer(癌部・非癌部)
- sporadic cancer(癌部・非癌部)
各10症例の大腸粘膜について網羅的mRNA発現解析を行い、潰瘍性大腸炎における薬剤抵抗性および癌化に関与する遺伝子の同定を目指している。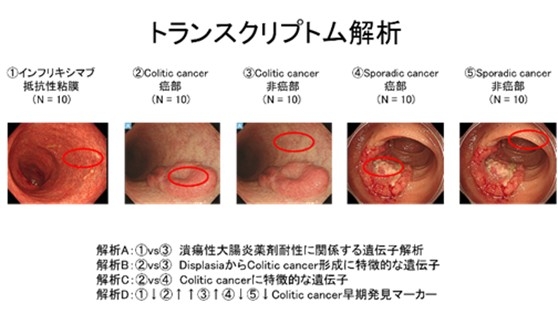
BIBLIOGRAPHY
2025 (Clinical)
- Tanaka H, Sakai A, Suenaga M, Hayashi M, Otsu T, Nakagawa N, Kurimoto K, Fukasawa M, Shibuya K, Watanabe N, Sunagawa M, Yamaguchi J, Mizuno T, Kokuryo T, Takami H, Ebata T, Fujii T, Kodera Y.
FUT2 and FUT3-specific normalization of DUPAN-2 and carbohydrate antigen 19-9 in preoperative therapy for pancreatic cancer: multicentre retrospective study (GEMINI-PC-01).
The British Journal of Surgery. 2025 Mar 28; 112(4): znaf049. - Kawakami H, Nakanishi K, Makiyama A, Konishi H, Morita S, Narita Y, Sugimoto N, Minashi K, Imano M, Inamoto R, Kodera Y, Kume H, Yamaguchi K, Hashimoto W, Muro K; EN-DEAVOR Study Group.
Real-world effectiveness and safety of trastuzumab-deruxtecan in Japanese patients with HER2-positive advanced gastric cancer (EN-DEAVOR study).
Gastric Cancer. 2025 Jan; 28(1): 51-61. - Mori K, Tanaka H, Kimura N, Fukasawa M, Itoh A, Shirai Y, Shibuya K, Nagaoka K, Yamamoto Y, Fujii T.
Significance of Self-Expandable Metallic Stent for Postoperative Intra-Abdominal Infection After Pancreatoduodenectomy in Patients With a Hard Pancreas.
https://doi.org/10.1002/ags3.70150 - Umeda S, Nakayama G, Kishida T, Hattori N, Nakanishi K, Tanaka H, Shimizu D, Takami H, Hayashi M, Kanda M, Tanaka C, Kodera Y.
Efficacy and safety of postoperative adjuvant chemotherapy with oxaliplatin for elderly patients: results from the CCOG-1302 study.
International Journal of Clinical Oncology. 2025 Jun;30(6): 1174-1182. - Hoshino N, Kanda M, Oba K, Aoyama T, Honda M, Kashiwabara K, Maeda H, Mayanagi S, Muto M, Tanaka K, Yamagishi H, Sakamoto J, Obama K, Yoshikawa T.
Efficacy and safety of oral 5-FU-based adjuvant chemotherapy for geriatric patients with colorectal cancer: Integrated analysis of seven clinical trials conducted at the Japanese Foundation for Multidisciplinary Treatment of Cancer.
Colorectal Disease. 2025 Nov; 27(11): e70317.
2025 (Experimental)
- Tanaka H, Fukasawa M, Kimura N, Mori K, Matsui K, Itoh A, Hirano K, Watanabe T, Shirai Y, Nagaoka K, Shibuya K, Yoshioka I, Yamamoto Y, Niimi H, Fujii T.
A novel melting temperature mapping method may improve the prediction of postoperative intra-abdominal infection after pancreatoduodenectomy.
British Journal of Surgery 2025 Oct 3; 112(10): znaf222. - Umeda S, Tanaka K, Kishida T, Hattori N, Tanaka H, Shimizu D, Takami H, Hayashi M, Tanaka C, Nakayama G, Kanda M.
Cholinergic Receptor Nicotinic Beta 2 Subunit Promotes the Peritoneal Disseminating Metastasis of Colorectal Cancer.
Cancers (Basel). 2025 Jul 28; 17(15): 2485. - Ito Y, Kanda M, Tanaka H, Nakamura K, Mizuno M, Hori M, Kajiyama H, Kodera Y.
Antitumor effects of plasma-activated sodium acetate solution on gastric cancer cells.
Scientific Reports. 2025 Jun 5; 15(1): 19807. - Iizuka A, Kanda M, Sato Y, Shimizu D, Umeda S, Tanaka H, Hattori N, Hayashi M, Tanaka C, Kodera Y.
Association of NR0B1 with Malignant Phenotypes in Esophageal Squamous Cell Carcinoma Through Modulation of p53-Independent Cell-Cycle Regulation.
Annals of Surgical Oncology. 2025 Jun;32(6):4464-4475. - Agatsuma Y, Shimizu D, Umeda S, Tanaka H, Hattori N, Hayashi M, Kanda M, Tanaka C, Nakayama G, Fujiwara M, Kodera Y.
FAM32A Suppression Decreases 5-Fluorouracil-induced Apoptosis and Is Associated With Poor Prognosis in Gastric Cancer.
Cancer Genomics Proteomics. 2025 Jan-Feb; 22(1): 55-69. - Bayasgalan T, Kanda M, Sato Y, Zhu H, Hamrah MH, Martinez FEG, Shinozuka T, Ito Y, Sasahara M, Shimizu D, Umeda S, Inokawa Y, Hattori N, Hayashi M, Tanaka C, Kodera Y.
SPOCD1 Enhances Cancer Cell Activities and Serves as a Prognosticator in Esophageal Squamous Cell Carcinoma.
Cancer Genomics Proteomics. 2025 Mar-Apr; 22(2): 306-325.
2024 (Clinical)
- Nakanishi K, Kanda M, Ito S, Mochizuki Y, Teramoto H, Ishigure K, Murai T, Asada T, Ishiyama A, Matsushita H, Shimizu D, Tanaka C, Fujiwara M, Murotani K, Kodera Y.
Oncological similarities between large type 3 and type 4 tumors in. patients with resectable gastric cancer: a propensity score-matched analysis of a multi-institutional dataset.
Gastric Cancer. 2024 Nov; 27(6): 1331-1341. - Kawakami H, Nakanishi K, Makiyama A, Konishi H, Morita S, Narita Y, Sugimoto N, Minashi K, Imano M, Inamoto R, Kodera Y, Kume H, Yamaguchi K, Hashimoto W, Muro K.
Real-world effectiveness and safety of trastuzumab-deruxtecan in. Japanese patients with HER2-positive advanced gastric cancer (EN-DEAVOR. study).
Gastric Cancer. 2025 Jan; 28(1): 51-61. - Kodera Y.
The Magic Flute is a Singspiel, not an opera? My thoughts about the. German, Austrian and Swiss Guidelines for Systemic Treatment of Gastric Cancer.
Gastric Cancer. 2024 Jan; 27(1): 1-2. - Kobayashi D, Kodera Y, Fukushima R, Morita M,. Fushida S, Yamashita N, Yoshikawa K, Ueda S, Yabusaki H, Kusumoto T, Arigami T, Hidemura A, Omori T, Yamaguchi H, Hirono Y, Tsuji Y, Moon JH, Tomita T, Imamura H, Nakanishi K, Shimizu D, Hirakawa A, Ishigami H, Kitayama J.
Phase II Study of Intraperitoneal Administration of Paclitaxel Combined with S-1 and Cisplatin for Gastric Cancer with Peritoneal Metastasis.
Annals of Surgical Oncology. 2024 Feb; 31(2): 735-743. - Sugiyama F, Kanda M, Shimiz, D,. Umeda S, Inokawa Y, Hattori N, Hayashi M,. Tanaka C, Nakayama G, Kodera Y.
Absence of Hypercoagulation Status after Neoadjuvant Treatment is. Associated with Favorable Prognosis in Patients Undergoing Subtotal Esophagectomy for Esophageal Squamous Cell Carcinoma.
Annals of Surgical Oncology. 2024 May; 31(5): 3417-3425.
2024 (Experimental)
- Kanda, M. Kasahara, Y. Shimizu, D. Shinozuka, T. Sasahara, M. Nakamura, S. Iguchi, Y. Katsuno, M. Kodera, Y. Obika, S.
Dual-modified antisense oligonucleotides targeting oncogenic. protocadherin to treat gastric cancer.
British Journal of Cancer, 2024 Nov; 131(9): 1555-1566. - Ito, Y. Kanda, M. Sasahara, M. Tanaka, C. Shimizu, D. Umeda, S. Inokawa, Y. Hattori, N. Hayashi, M. Nakayama, G. Kodera, Y.
Killer cell lectin-like receptor G2 facilitates aggressive phenotypes of. gastric cancer cells via dual activation of the ERK1/2 and JAK/STAT. pathways.
Gastric Cancer. 2024 May; 27(3): 506-518. - Kanda, M. Takano, N. Miyauchi, H. Ueda, K. Mizuno, M. Kasahara, Y. Kodera, Y. Obika, S.
Preclinical toxicological assessment of amido-bridged nucleic. acid-modified antisense oligonucleotides targeting synaptotagmin XIII. for intra-abdominal treatment of peritoneal metastasis of gastric cancer.
Gastric Cancer. 2024 Nov; 27(6): 1229-1241. - Sasahara, M. Kanda, M. Tanaka, C. Shimizu, D. Umeda, S. Takami, H. Inokawa, Y. Hattori, N. Hayashi, M. Nakayama, G. Kodera, Y.
Therapeutic antibody targeting natriuretic peptide receptor 1 inhibits. gastric cancer growth via BCL-2-mediated intrinsic apoptosis.
International Journal of Cancer. 2024 Apr 1; 154(7): 1272-1284. - Shinozuka, T. Kanda, M. Sato, Y. Shimizu, D. Umeda, S. Takami, H. Hattori, N. Hayashi, M. Tanaka, C. Kodera, Y.
Therapeutic Potential of Antibody Targeting Neuronal Pentraxin Receptor. in Esophageal Squamous Cell Carcinoma.
Annals of Surgical Oncology. 2024 Sep; 31(9): 5674-5682.

