産婦人科学
KEYWORDS
- エクソソーム
- 妊娠合併症
- 子宮内膜症
- 絨毛癌
- 腹膜中皮
- プラズマ
- 癒着胎盤
- RPOC
- PCOS
- 生殖中枢
HEAD

LAB MEMBER
| 構成員名 | 役職 | 研究者総覧 |
|---|---|---|
| 中村 智子 | 診療教授 | 研究者総覧 |
| 牛田 貴文 | 准教授 | 研究者総覧 |
| 新美 薫 | 准教授 | 研究者総覧 |
| 芳川 修久 | 講師 | 研究者総覧 |
| 横井 暁 | 講師 | 研究者総覧 |
| 村岡 彩子 | 講師 | 研究者総覧 |
| 玉内 学志 | 病院講師 | 研究者総覧 |
| 吉原 雅人 | 病院講師 | 研究者総覧 |
| 三宅 菜月 | 助教 | 研究者総覧 |
| 田野 翔 | 助教 | 研究者総覧 |
| 曾根原 玲菜 | 助教 | 研究者総覧 |
| 長尾 有佳里 | 助教 | 研究者総覧 |
| 甲木 聡 | 助教 | 研究者総覧 |
| 吉田 康将 | 病院助教 | 研究者総覧 |
| 松尾 聖子 | 病院助教 | 研究者総覧 |
| 夫馬 和也 | 病院助教 | 研究者総覧 |
| 関 友望 | 特任助教 | 研究者総覧 |
| 茂木 一将 | 病院助教 | 研究者総覧 |
| 伊吉 祥平 | 特任助教 | 研究者総覧 |
CONTACT
| ob-gy◎med.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | 産婦人科学 独自ホームページ |
OUTLINE
名古屋大学 医学部 産婦人科は、「婦人科腫瘍」、「内分泌・腫瘍」、「周産期」、「不妊・生殖」の4つのグループに分かれて研究を行っています。
RESEARCH PROJECTS
研究内容 - 腫瘍
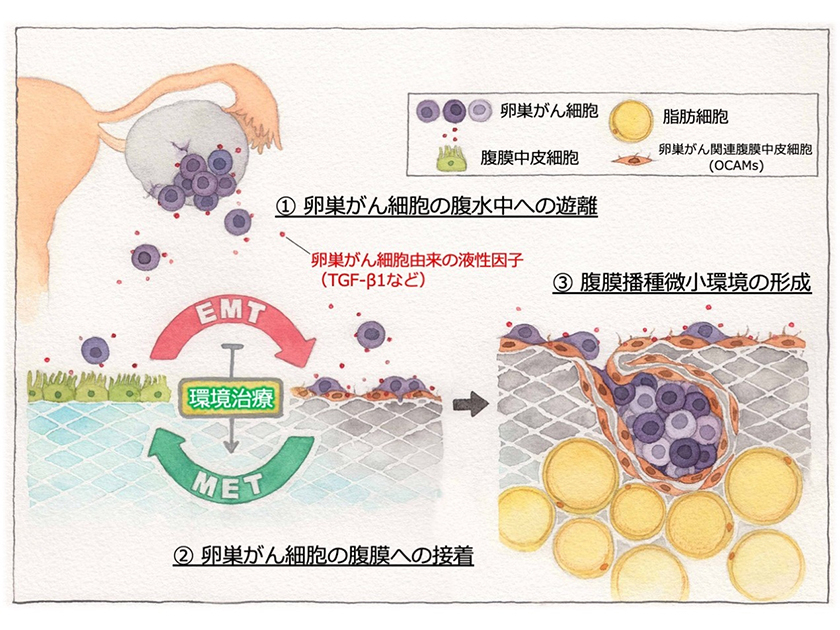
卵巣がん関連腹膜中皮細胞に着目した腹膜播種形成の病態解明と新規治療戦略
卵巣がん細胞が腹膜播種を起こすホスト細胞としては、腹膜中皮細胞が挙がりますが、もともと腹膜中皮細胞は通常、敷石状形態をとり、臓側あるいは壁側腹膜の表層を覆うことで、腸管などとの摩擦の緩衝、様々な生理活性物質の生成・分泌、そして腹腔内の創傷治癒に関与していることが知られています。ここで1つの疑問が生じますが、卵巣がんが播種する際、腹膜中皮細胞が、“防御的”に機能するのか、それともがん細胞の“initial contact”の足場としてがんの進展を“助ける”ものであるのか?ということです。近年、がん微小環境を構成する様々な細胞が、多様な増殖因子や生理活性物質を産生することで、治療抵抗性の維持やがん細胞の増殖、浸潤転移などを制御していることが判明しています。それら主要な細胞集団の1つに、がん関連線維芽細胞(CAFs)と呼ばれる細胞集団の存在が指摘されています。私たちはこれまでに、卵巣がん側の因子によって、本来防御的な腹膜中皮細胞が変貌を遂げ、α-SMAを高発現する卵巣がん関連腹膜中皮細胞(ovarian cancer-associated mesothelial cells:OCAMs)に変化することを見いだしました。OCAMsの本質は腹膜中皮細胞の上皮間葉転換であり、実際にOCAMsが基底膜の下、約90μmの範囲に広がる毛細リンパ管や毛細血管網から構成される血液腹膜関門を破壊し、それらの透過性を著しく高め、多量の腹水生成に寄与すること、そして、それらを標的とすることによって腹水量を減少に導き、がん性腹膜炎状態の改善に寄与できることを解明しました(Fujikake K et al, Oncol Rep. 2018)。さらに卵巣がんを助長する腹腔内因子として免疫細胞や脂肪細胞の影響が考えられ、それらが一体となって腹膜環境の生態系を構築し、がん性腹膜炎の形成に大きな役割を担っていることが解明されつつあります。これらのステップで重要な点は、腫瘍細胞の間葉系形質の獲得とがん-腹膜の協調的細胞クロストークの開始と拡大にあります。実際にOCAMsへと変貌した腹膜中皮細胞では、一種のケモカインの分泌が亢進し、その受容体であるケモカインレセプターを高発現する卵巣がん細胞を能動的に腹膜側に誘導し、結果として“Seed & Soil”的に腫瘍が腹膜に引き寄せられ腹膜播種を増加させるメカニズムが判明しました(Peng Y, et al, Cancer Lett 2019, Yasui H, et al, Clin Exp Metastasis. 2020)。またOCAMsは間葉系形質を獲得した卵巣がん細胞と協調することによって、腹腔内における腫瘍のプラチナ耐性に深く関与することが判明しました(Yoshihara M, et al, Int J Cancer 2020)。こうした腹膜播種の攻略には、腹膜全体をターゲットとしたOCAMsを正常な腹膜中皮細胞へと改変させる戦略が不可欠であると考えます。こうした構想の中で、私たちはこれまでに、OCAMsを正常化させる薬物候補をすでに複数同定しており、「腹膜環境の正常化」によって、がん性腹膜炎を制御する新規治療戦略を目指しております。
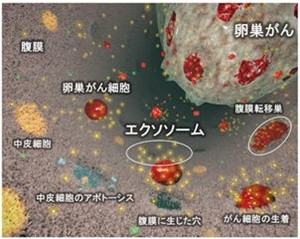
がん細胞外小胞エクソソームの婦人科悪性腫瘍における機能解析と臨床応用
あらゆる細胞が放出する直径100nm前後の小さな脂質二重膜小胞、エクソソームは、細胞間情報伝達手段の一つとして2007年頃より急速に注目を集めています。エクソソームは多様な細胞外小胞(Extracellular Vesicle: EV)の一つのサブタイプであり、EVは様々な生理活性物質を詰めこんだ複合体という特徴を有し、発がん・転移・悪性化に関わる重要な役割を持っており、ヒト体液中に豊富に含まれ、循環し、病態を反映してプロファイルが変化します。EVを対象とした研究は、世界的に今最も注目を集める研究分野の一つといって間違いなく、取り巻く市場も急激に拡大しています。我々の研究グループは、予後の悪い女性生殖器悪性腫瘍である卵巣がんを主な対象として、エクソソームの重要な役割について、これまで国立がん研究センターと共同で精力的に研究してきました。2017年に、卵巣がん細胞が放出するエクソソームがMMP1メッセンジャーRNAを内包し、腹膜中皮細胞を破壊し、腹膜播種性転移を促進するメカニズムを世界に先駆け解明しました(図:Yokoi A, et al., Nature Communications. 2017)。また、NEDO「体液中マイクロRNA測定技術基盤開発事業」の一環として、卵巣がん患者血液中の10種のエクソソームマイクロRNAを解析し、早期診断アルゴリズムを構築しました(Yokoi A, et al., Nature Communications. 2018)。さらに、米国テキサス大学MDアンダーソンがんセンターと共同で、卵巣がん細胞が分泌するエクソソームに含まれるDNAの生合成機構についての解析も行いました(Yokoi A, et al., Science Advances. 2019)。我々は、EVおよびエクソソームに内包される様々核酸の研究を通して、がん悪性化病態解明へのEVの強い関与や、がん臨床バイオマーカーとして、また新しい治療応用としての可能性を確信し、現在も国内有数の医療機関・研究施設と共同研究を遂行しています。また、次世代シーケンサーによるマイクロRNA網羅解析を軸とした、疾患機構解明にも取り組んでおり、産婦人科教室でしか経験できないような疾患を対象とした、ユニークなトランスレーショナル研究も展開しています (Yoshida, et al. Carcinogenesis. 2019, Yoshida, et. al. Oncogene. 2021)。さらに、文部科学省研究大学強化促進事業の支援を受け、名古屋大学高等研究院「ナノテクノロジーによるがん細胞外小胞研究ユニット」を設立し (http://www.aip.nagoya-u.ac.jp/ru/menu_b/post-36.html)、工学分野との共同研究や、内閣府AMED革新的がん医療実用化研究事業による支援などの下、社会還元へ繋がるような、EVの臨床応用を目指して最先端の研究を行っています。
非平衡大気圧プラズマの卵巣癌治療応用を目指した基礎研究
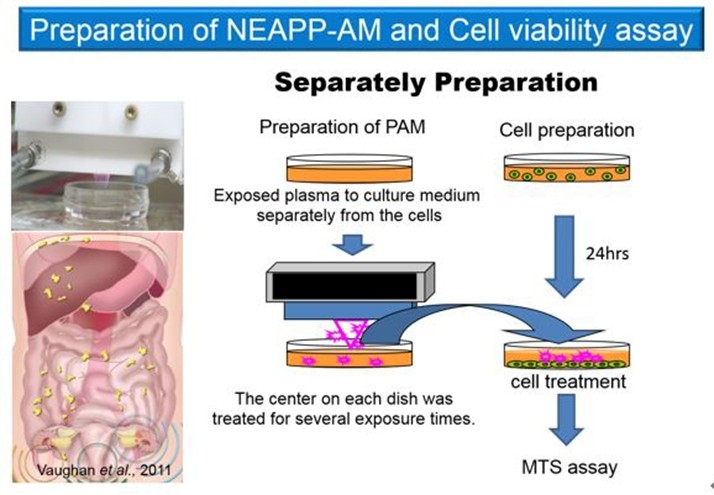
大気圧プラズマを人体に照射して、病気や怪我を治す「プラズマ医療」の研究が近年世界中で盛んに進められている。大気圧プラズマの応用といえば、環境汚染ガス処理、水処理、表面処理、殺菌などが思い浮かぶが、これを止血、創傷治癒、そして癌治療にまで応用する研究である。プラズマ医療では、活性種が癌細胞を攻撃したり、けがをした部分の細胞を適度に刺激して治癒を早める、といった治療原理が考えられている.細胞レベルではすでに著しい効果が多数報告されており、動物実験もいくつか始められている。
この10年間にわたって正常細胞のみならず、脳腫瘍、大腸癌、皮膚がん、肺癌、膵癌および卵巣癌などにおいてプラズマ照射がアポトーシスによる細胞死を誘導することが示されてきた。このプラズマのもたらすアポトーシスの作用は、プラズマから発せられるフリーラジカルを含む活性酸素種(ROS)などによる細胞の酸化還元平衡の障害に起因するDNAの損傷によるものであると考えられている。これまでのいくつかの報告からプラズマの細胞増殖抑制作用は正常細胞に比して腫瘍細胞で強いという一定の細胞選択性があることが示唆されてきている。この選択制は癌細胞の高い増殖活性に基づく細胞内ROSレベルの相違に起因すると考えられている。
以上の背景をもとに我々は、主に卵巣癌の腹腔内播種という進行形態の効果的な抑制方法として、大気圧プラズマを培養液に照射し(PAM; Plasma activated-medium)その溶液を投与するという腹腔内投与が可能な間接照射を利用したプラズマ癌治療を探求している。また、プラズマの持つ抗腫瘍効果の分子学的な解明やプラズマが卵巣癌の播種に促進的に働く上皮間葉形態転換現象(EMT: Epithelial-Mesenchymal Transition)に与える影響を調査している。
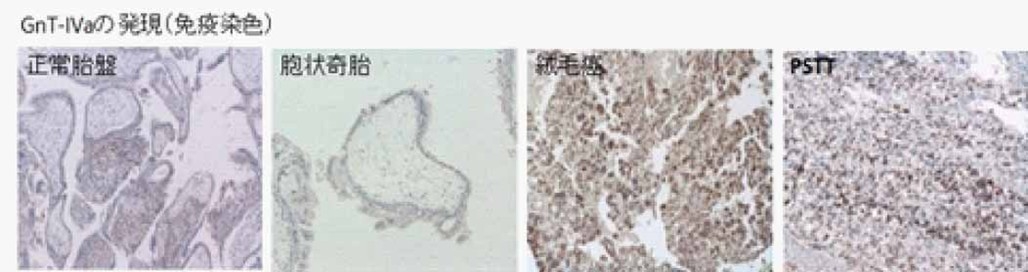
絨毛癌における糖転移酵素GnT-IVaおよびC2GnTの発現と機能解析
胞状奇胎から侵入奇胎をへて絨毛癌へと癌化することが知られていますが、そのメカニズムは解明されていません。すべての絨毛性疾患および胎盤の栄養膜細胞から分泌されるhCGは、腫瘍マーカーとしても用いられますが、アスパラギン結合糖鎖は4カ所、セリン結合糖鎖は4カ所結合できる部位をもっています。正常妊娠や胞状奇胎に比べると、侵入奇胎、さらに絨毛癌では過剰糖鎖付加hCGが顕著に増加することが明らかになっています。絨毛細胞の悪性化に伴い分泌される過剰糖鎖付加hCGの原因となる糖転移酵素N-acetylglucosaminyltransferase IV (GnT-IV) (Niimi K, et al. Br J Cancer. 2012)やCore-2 N-acetylglucosaminyltransferase (C2GnT)-1に注目した研究を行っています。
絨毛性腫瘍の責任妊娠の解明
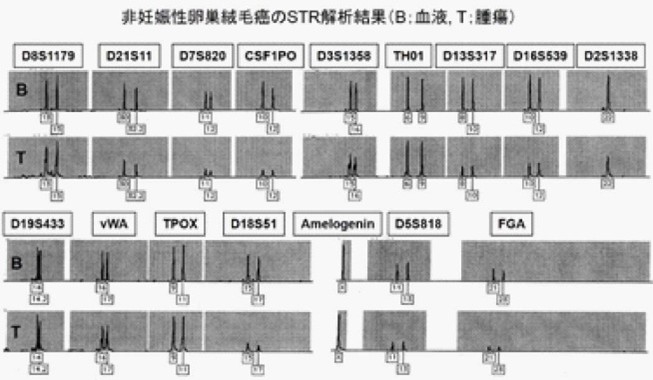
絨毛性腫瘍には、侵入奇胎、絨毛癌、胎盤部トロホブラスト腫瘍(PSTT)、および上皮性トロホブラスト腫瘍(ETT)があります。侵入奇胎は胞状奇胎を由来として発症しますが、その他の絨毛性腫瘍の場合には腫瘍の由来となる責任妊娠は先行妊娠(直前の妊娠)とは限りません。DNA解析を用いて絨毛性腫瘍の責任妊娠を調べています(Yamamoto E, et al. Gynecol Oncol Case Rep. 2014)。非妊娠性絨毛癌もDNA解析により診断することができます。
周産期
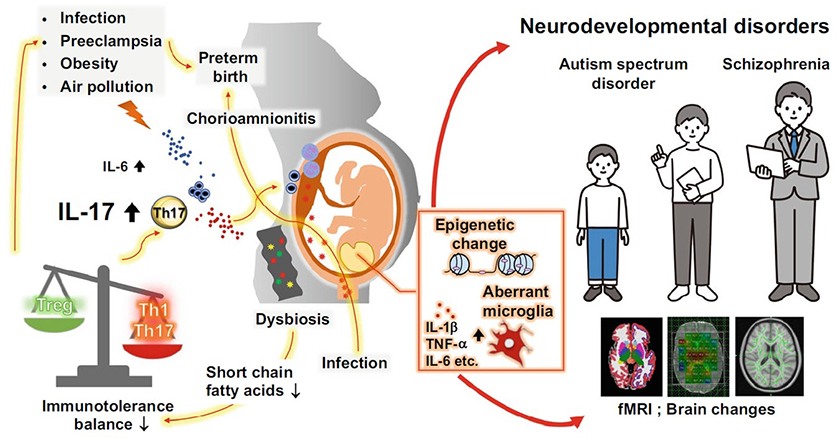
1. 妊娠高血圧症候群や妊娠中の環境が児の発達に与える影響
妊娠中の高血圧や、炎症、投薬、栄養などは、胎児の臓器や脳の発達に長期的な影響を及ぼしている可能性があります。本研究室では同意の得られた妊婦から臨床検体(母体血、臍帯血、羊水、胎盤、臍帯)を採取・保管し、解析に用いています。また、小児科との共同研究で新生児の頭部MRIを解析し、妊娠高血圧症候群、絨毛膜羊膜炎、ステロイドが新生児期の脳に影響を及ぼしている可能性を明らかにしました(Ushida et al. Pregnancy Hypertens. 2021, Katsuki et al. Early Hum Dev. 2021, Nosaka et al. Arch Gynecol Obstet. 2024, Fuma et al. Eur J Obstet Gynecol Reprod Biol. 2024)。動物実験では妊娠高血圧モデルマウス、母体炎症モデルマウス等を用いて、母獣の環境が仔の脳に与える影響を研究しています(Imai et al. Free Radic Biol Med. 2016, Fuma et al. Commun Biol. 2025)。
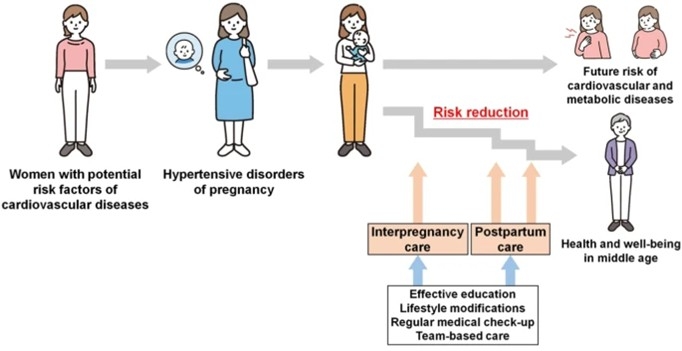
2. 妊娠前・妊娠中の生活の改善による妊娠合併症の予防
体重増加、食事、運動、睡眠など、生活を改善することで妊娠高血圧症候群に代表されるような妊娠合併症を予防できないか研究しています。地域の各施設から収集した臨床データや、IoTから得られたリアルワールドデータを用いて、患者教育を含めた疾患予防アルゴリズムを構築し、当科のインターコンセプション外来での情報提供に還元しています(Ushida et al. Hypertens Res. 2024, Tano et al. Hypertens Res. 2024)。
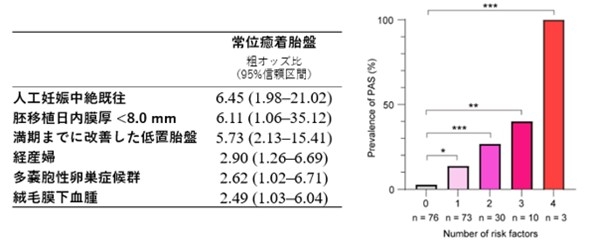
3. 生殖補助医療における癒着胎盤症候群の関連因子の同定
生殖補助医療、特にホルモン補充周期凍結胚移植において癒着胎盤症候群の頻度が増加することが報告されています。癒着胎盤症候群では分娩後に胎盤剥離が困難となり、分娩後大量出血のリスクとなります。分娩前に癒着胎盤症候群を予測することは難しいため、臨床研究により癒着胎盤症候群に関連する因子を同定しました(Matsuo et al. Reprod Med Biol. 2024)。現在ホルモン補充周期凍結胚移植における癒着胎盤症候群の病態生理に関する基礎研究もはじめています。
4. 周産期予後改善を目的とした細胞外小胞に着目した包括的アプローチ
あらゆる生細胞が放出する細胞外小胞は、内部にタンパク質、核酸、脂質等を含み細胞間の情報伝達を担っていることが報告されています。今までに、先天性横隔膜ヘルニアという出生後に呼吸障害で亡くなる可能性がある重症な疾患の予後を羊水中細胞外小胞を用いて高精度に予測できることを報告しました(Matsuo et al. J Extracell Biol. 2024)。現在は妊娠高血圧腎症に関する研究もはじめています。
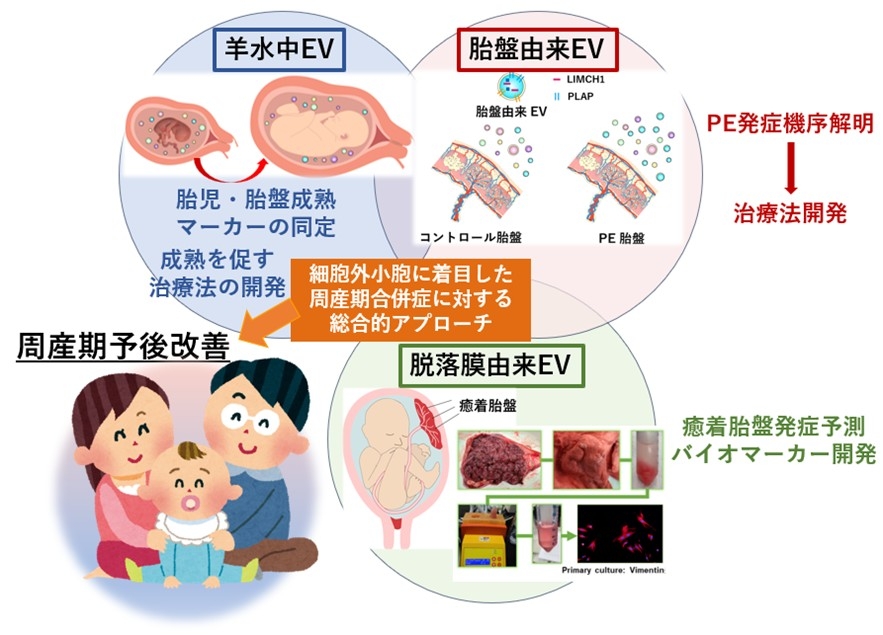
子宮内膜症の病態解明と新規治療法の確立
子宮内膜症は、エストロゲン依存性に増悪する慢性炎症性疾患であり、ホルモン療法が治療の主軸となっています。ホルモン療法はいずれも排卵を抑制するため、現在の挙児希望とは両立できないという問題点があります。また、ホルモン療法中に病変が増大したり、疼痛が改善しない症例もあり、ホルモン療法によりすべての子宮内膜症が解決するわけではありません。一方、卵巣子宮内膜症性嚢胞摘出術では、術後に卵巣予備能の指標であるAMH(Anti-Müllerian Hormone)が低下することが示されており、卵巣にダメージを及ぼします。当教室では、これら子宮内膜症治療の問題点の解決を目指し、卵巣機能維持と両立できる非ホルモン療法につながる研究に取り組んでいます。我々は、世界で初めて卵巣子宮内膜症(OE)モデルマウスの確立に成功しました(Hayashi S, et al. Redox Biol. 2020)。このマウスモデルを用いて、NLRP3インフラマソームに着目し、正所性子宮内膜に影響を及ぼさない非ホルモン療法について報告しました(Murakami, et al. Reprod Biol Endocrinol. 2022)。また、子宮内膜症の新たな特性である細胞老化に着目し、老化細胞をターゲットにした薬物治療が新規治療戦略となる可能性について探究しております。さらに、子宮内膜症性病変の治療についての検討だけではなく、子宮内膜症成立の根本的な要因についても解明すべく、逆流説に基づく子宮内膜症の発生において、子宮内膜の細菌感染が成因となっていること、感染子宮内膜への抗菌薬治療が、子宮内膜症の発生を抑制する可能性を報告しました (Muraoka A, et al. Sci Transl Med. 2023)。
プレコンセプションケアを見据えた多嚢胞性卵巣症候群 (PCOS)の診断と薬物療法の探求
PCOS (polycystic ovary syndrome) は、排卵障害による不妊症に加え、周産期合併症の増加や肥満・糖尿病・高脂血症などの代謝異常も来し、女性の生殖および代謝機能に重大な影響を及ぼすため、女性の健康を生涯にわたって害する疾患です。性成熟期女性の5-10%程度に認められるありふれた疾患であるにもかかわらず、根本的な病因は不明であり、治療法は排卵障害に対する排卵誘剤など、対症療法のみになります。日本産科婦人科学会では2024年にPCOSの診断基準を改訂し、卵巣予備能のマーカーである血清AMH値を診断に用いることが可能となりました。しかし、思春期~若年の女性ではPCOSの診断方法が未だ一定していないのが現状です。PCOSの可能性を簡便に把握できることは将来の妊娠を希望する若年女性にとって非常に重要です。当グループでは数百人の女子大学生の検体を用いて血清AMH値と月経不順との関係、PCOSリスクとの関係を検討しました(Miyake N, et al. Reprod Med Biol. 2024)。また、PCOSは前述のように、特徴的な病態を多臓器で示す全身性疾患であるため、病因は単一でないと考えられており、病態の解明には複数臓器での解析が必須になります。しかし、ヒトの複数臓器から検体を一度に採取することは困難であるため、PCOS の病態解明および根治的な治療法の開発には、適切な動物モデルの作製が極めて重要といえます。当グル―プでは、胎生期に経母体的にアンドロゲンを投与することで、ヒトPCOSに近い疾患モデルの作成に成功、さらに、高ゴナドトロピン (LH) 値の要因として、GnRH/ LH 分泌をさらに上位から制御することが近年明らかになってきた視床下部神経ペプチドであるキスペプチンの発現異常について報告しました(Osuka S, et al. Endocrinology. 2017)。現在は、このモデルを用い、企業との共同研究によって薬剤による治療効果の検討を行っています(Muraoka A, et al. Sci Transl Med. 2023) 。
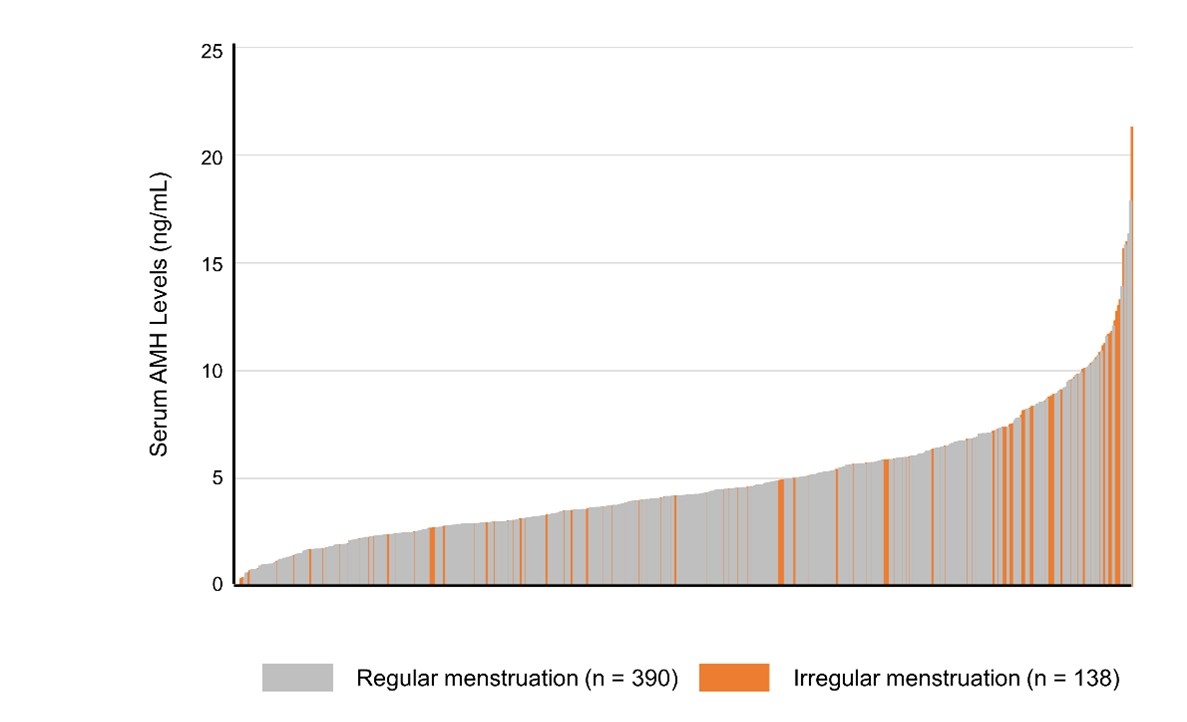
月経不順あり:オレンジ、月経不順なし:灰色 (文献1より)
女子大生における血清AMH値と月経不順の有無
Retained Products of Conception (RPOC)における多量出血予測因子
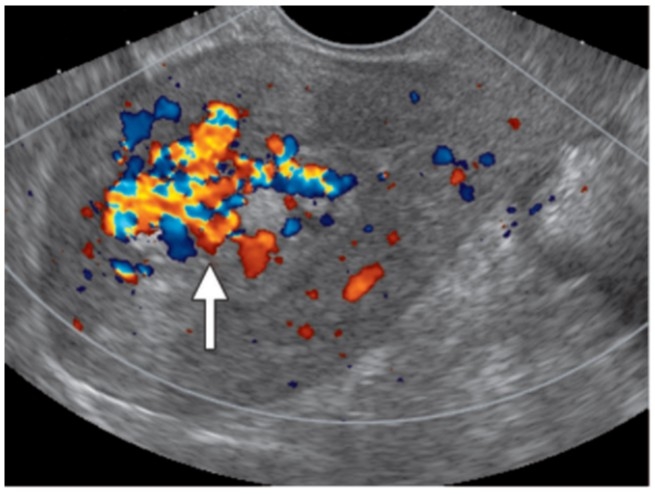
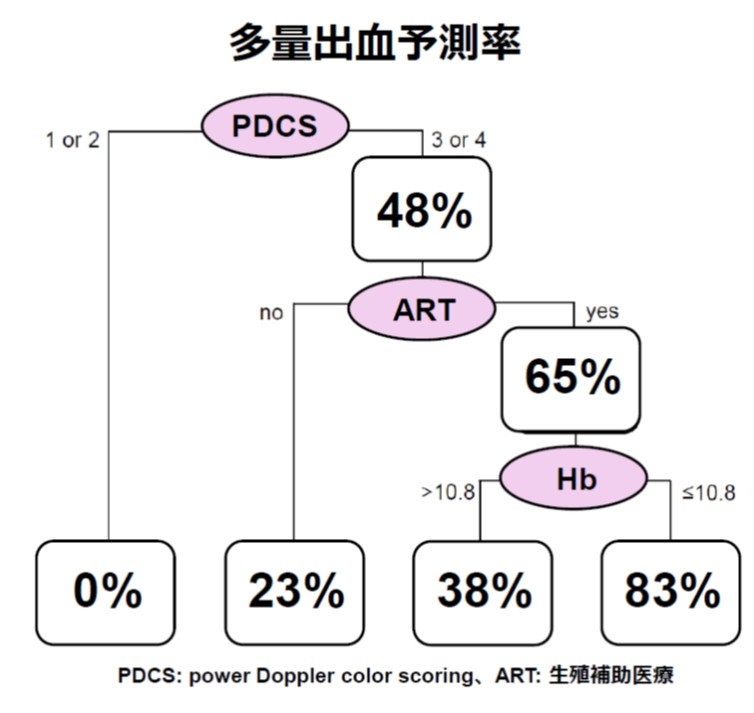
(文献8より一部改変)
RPOCとは妊娠終了後に子宮内に残存した絨毛由来の組織が腫瘤を形成したもので、時に生命を脅かすほどの出血を呈しますが、現在確立された治療プロトコールは存在しません。子宮動脈塞栓術や子宮鏡手術など治療介入を要す症例をより的確に抽出するためのプロトコールの確立が望まれます。当教室ではRPOCの多量出血予測因子を同定し報告しました (Sonehara R, et al. Sci Rep. 2022)。現在は、出血予測のスコアリングシステム構築を目指し、多施設共同研究を行っております。
その他、早発卵巣不全 (POI) の診断バイオマーカー、ヒト顆粒膜細胞株を用いた卵胞発育制御機構の解明、などをテーマにした研究も行っております。さまざまな分野の基礎研究室との共同研究も行っています。
BIBLIOGRAPHY
不明
- Yoshita S, Osuka S, Shimizu T, Fujitsuka N, Matsumoto C, Bayasula, Miyake N, Muraoka A, Nakanishi N, Nakamura T, Goto M, Kajiyama H. Unkeito promotes follicle development by restoring reduced follicle-stimulating hormone responsiveness in rats with polycystic ovary syndrome. [Journal name pending PubMed confirmation].
2025
- Muraoka A, Yokoi A, Yoshida K, Kitagawa M, Bayasula, Murakami M, Miyake N, Sonehara R, Nakamura T, Osuka S, Kajiyama H. Serum-derived small extracellular vesicles as biomarkers for predicting pregnancy and delivery in assisted reproductive technology in patients with endometriosis. Front Endocrinol (Lausanne). 2025;15:1442684.
- Fuma K, Iitani Y, Imai K, Ushida T, Tano S, Yoshida K, Yokoi A, Miki R, Kidokoro H, Sato Y, Hara Y, Ogi T, Nomaki K, Tsuda M, Komine O, Yamanaka K, Kajiyama H, Kotani T. Prenatal inflammation impairs early CD11c-positive microglia induction and delays myelination in neurodevelopmental disorders. Commun Biol. 2025 Jan 17;8(1):75. doi: 10.1038/s42003-025-07511-3.
- Tano S, Kotani T, Ushida T, Matsuo S, Yoshihara M, Imai K, Kinoshita F, Moriyama Y, Nomoto M, Yoshida S, Yamashita M, Kishigami Y, Oguchi H, Kajiyama H. Visualizing risk modification of hypertensive disorders of pregnancy: development and validation of prediction model for personalized interpregnancy weight management. Hypertens Res. 2025 Mar;48(3):884-893.
2024
- Yabuki A, Muraoka A, Tamauchi S, Seki T, Takeda T, Sonehara R, Miyake N, Nakamura T, Osuka S, Kajiyama H. The influence of radical trachelectomy on endometrial thickness in in vitro fertilization–embryo transfer. J Obstet Gynaecol Res. 2024;50(2):218–224.
- Yabuki A, Muraoka A, Osuka S, Yokoi A, Yoshida K, Kitagawa M, Bayasula, Sonehara R, Miyake N, Nakanishi N, Nakamura T, Iwase A, Kajiyama H. Serum miRNA as a predictive biomarker for ovarian reserve after endometrioma cystectomy. Reprod Biol. 2024;24(1):100821.
- Nosaka R, Ushida T, Kidokoro H, Kawaguchi M, Shiraki A, Iitani Y, Imai K, Nakamura N, Sato Y, Hayakawa M, Natsume J, Kajiyama H, Kotani T. Intrauterine exposure to chorioamnionitis and neuroanatomical alterations at term-equivalent age in preterm infants. Arch Gynecol Obstet. 2024 May;309(5):1909-1918.
- Fuma K, Ushida T, Kawaguchi M, Nosaka R, Kidokoro H, Tano S, Imai K, Sato Y, Hayakawa M, Kajiyama H, Kotani T. Impact of antenatal corticosteroids on subcortical volumes in preterm infants at term-equivalent age: A retrospective observational study. Eur J Obstet Gynecol Reprod Biol. 2024 Nov;302:7-14.
- Ushida T, Tano S, Imai K, Matsuo S, Kajiyama H, Kotani T. Postpartum and interpregnancy care of women with a history of hypertensive disorders of pregnancy. Hypertens Res. 2024 Jun;47(6):1457-1469.
- Miyake N, Osuka S, Ohsawa I, Tonoike T, Uno T, Tsuzuki K, Bayasula, Sonehara R, Muraoka A, Nakamura T, Goto M, Iwase A, Kajiyama H. Association between anti-Müllerian hormone levels and polycystic ovary syndrome in a general cohort of young women in Japan. Reprod Med Biol. 2024;23(1):e12615.
2023
- Muraoka A, Suzuki M, Hamaguchi T, Watanabe S, Iijima K, Murofushi Y, Shinjo K, Osuka S, Hariyama Y, Ito M, Ohno K, Kiyono T, Kyo S, Iwase A, Kikkawa F, Kajiyama H, Kondo Y. Fusobacterium infection facilitates the development of endometriosis through the phenotypic transition of endometrial fibroblasts. Sci Transl Med. 2023;15(700):eadd1531.
- Nakanishi N, Osuka S, Kono T, Kobayashi H, Ikeda S, Bayasula, Sonehara R, Murakami M, Yoshita S, Miyake N, Muraoka A, Kasahara Y, Murase T, Nakamura T, Goto M, Iwase A, Kajiyama H. Upregulated ribosomal pathway impairs follicle development in a polycystic ovary syndrome mouse model: differential gene expression analysis of oocytes. Reprod Sci. 2023;30(4):1306–1315.
2022
- Miyake N, Nagai T, Suga H, Osuka S, Kasai T, Sakakibara M, Soen M, Ozaki H, Miwata T, Asano T, Kano M, Muraoka A, Nakanishi N, Nakamura T, Goto M, Yasuda Y, Kawaguchi Y, Miyata T, Kobayashi T, Sugiyama M, Onoue T, Hagiwara D, Iwama S, Iwase A, Inoshita N, Arima H, Kajiyama H. Functional lactotrophs in induced adenohypophysis differentiated from human iPS cells. Endocrinology. 2022;163(3):bqac004.
- Wei W, Komatsu K, Osuka S, Murase T, Bayasula, Nakanishi N, Nakamura T, Goto M, Iwase A, Masubuchi S, Kajiyama H. Tamoxifen activates dormant primordial follicles in mouse ovaries. Reprod Sci. 2022;29(12):3404–3412.
- Murakami M, Osuka S, Muraoka A, Hayashi S, Bayasula, Kasahara Y, Sonehara R, Hariyama Y, Shinjo K, Tanaka H, Miyake N, Yoshita S, Nakanishi N, Nakamura T, Goto M, Kajiyama H. Effectiveness of NLRP3 inhibitor as a non-hormonal treatment for ovarian endometriosis. Reprod Biol Endocrinol. 2022;20(1):58.
- Sonehara R, Nakamura T, Iwase A, Nishida K, Takikawa S, Murakami M, Yoshita S, Muraoka A, Miyake N, Nakanishi N, Osuka S, Goto M, Kajiyama H. Predictive factors for massive hemorrhage in women with retained products of conception: a prospective study. Sci Rep. 2022;12(1):11859.
2021
- Yoshida K, Yokoi A, Sugiyama M, Oda S, Kitami K, Tamauchi S, Ikeda Y, Yoshikawa N, Nishino K, Niimi K, Suzuki S, Kikkawa F, Yokoi T, Kajiyama H. Expression of the chrXq27.3 miRNA cluster in recurrent ovarian clear cell carcinoma and its impact on cisplatin resistance. Oncogene. 2021 Feb;40(7):1255-1268.
- Ushida T, Kidokoro H, Nakamura N, Katsuki S, Imai K, Nakano-Kobayashi T, Moriyama Y, Sato Y, Hayakawa M, Natsume J, Kajiyama H, Kotani T. Impact of maternal hypertensive disorders of pregnancy on brain volumes at term-equivalent age in preterm infants: A voxel-based morphometry study. Pregnancy Hypertens. 2021 Aug;25:143-149. doi: 10.1016/j.preghy.2021.06.003. Epub 2021 Jun 9. PMID: 34139669.
- Katsuki S, Ushida T, Kidokoro H, Nakamura N, Iitani Y, Fuma K, Imai K, Nakano-Kobayashi T, Sato Y, Hayakawa M, Natsume J, Kajiyama H, Kotani T. Hypertensive disorders of pregnancy and alterations in brain metabolites in preterm infants: A multi-voxel proton MR spectroscopy study. Early Hum Dev. 2021 Dec;163:105479.
- Kasahara Y, Osuka S, Takasaki N, Bayasula, Koya Y, Nakanishi N, Murase T, Nakamura T, Goto M, Iwase A, Kajiyama H. Primate-specific POTE-actin gene could play a role in human folliculogenesis by controlling the proliferation of granulosa cells. Cell Death Discov. 2021;7(1):186.
- Muraoka A, Osuka S, Yabuki A, Bayasula, Yoshihara M, Tanaka H, Sonehara R, Miyake N, Murakami M, Yoshita S, Nakanishi N, Nakamura T, Goto M, Iwase A, Kajiyama H. Impact of perioperative use of GnRH agonist or dienogest on ovarian reserve after cystectomy for endometriomas: a randomized controlled trial. Reprod Biol Endocrinol. 2021;19(1):179.
2020
- Yasui H, Kajiyama H, Tamauchi S, Suzuki S, Peng Y, Yoshikawa N, Sugiyama M, Nakamura K, Kikkawa F. CCL2 secreted from cancer-associated mesothelial cells promotes peritoneal metastasis of ovarian cancer cells through the P38-MAPK pathway. Clin Exp Metastasis. 2020 Feb;37(1):145-158.
- Yoshihara M, Kajiyama H, Yokoi A, Sugiyama M, Koya Y, Yamakita Y, Liu W, Nakamura K, Moriyama Y, Yasui H, Suzuki S, Yamamoto Y, Ricciardelli C, Nawa A, Shibata K, Kikkawa F. Ovarian cancer-associated mesothelial cells induce acquired platinum-resistance in peritoneal metastasis via the FN1/Akt signaling pathway. Int J Cancer. 2020 Apr 15;146(8):2268-2280.
- Hayashi S, Nakamura T, Motooka Y, Ito F, Jiang L, Akatsuka S, Iwase A, Kajiyama H, Kikkawa F, Toyokuni S. Novel ovarian endometriosis model causes infertility via iron-mediated oxidative stress in mice. Redox Biol. 2020;37:101726.
- Muraoka A, Osuka S, Kiyono T, Suzuki M, Yokoi A, Murase T, Nishino K, Niimi K, Nakamura T, Goto M, Kajiyama H, Kondo Y, Kikkawa F. Establishment and characterization of cell lines from human endometrial epithelial and mesenchymal cells from patients with endometriosis. FS Sci. 2020;1(2):195–205.
2019
- Peng Y, Kajiyama H, Yuan H, Nakamura K, Yoshihara M, Yokoi A, Fujikake K, Yasui H, Yoshikawa N, Suzuki S, Senga T, Shibata K, Kikkawa F. PAI-1 secreted from metastatic ovarian cancer cells triggers the tumor-promoting role of the mesothelium in a feedback loop to accelerate peritoneal dissemination. Cancer Lett. 2019 Feb 1;442:181-192.
- Yokoi A, Villar-Prados A, Oliphint PA, Zhang J, Song X, De Hoff P, Morey R, Liu J, Roszik J, Clise-Dwyer K, Burks JK, O'Halloran TJ, Laurent LC, Sood AK. Mechanisms of nuclear content loading to exosomes. Sci Adv. 2019 Nov 20;5(11):eaax8849.
- Yoshida K, Yokoi A, Kagawa T, Oda S, Hattori S, Tamauchi S, Ikeda Y, Yoshikawa N, Nishino K, Utsumi F, Niimi K, Suzuki S, Shibata K, Kajiyama H, Yokoi T, Kikkawa F. Unique miRNA profiling of squamous cell carcinoma arising from ovarian mature teratoma: comprehensive miRNA sequence analysis of its molecular background. Carcinogenesis. 2019 Dec 31;40(12):1435-1444.
2018
- Fujikake K, Kajiyama H, Yoshihara M, Nishino K, Yoshikawa N, Utsumi F, Suzuki S, Niimi K, Sakata J, Mitsui H, Shibata K, Senga T, Kikkawa F. A novel mechanism of neovascularization in peritoneal dissemination via cancer-associated mesothelial cells affected by TGF-β derived from ovarian cancer. Oncol Rep. 2018 Jan;39(1):193-200.
2017
- Yokoi A, Yoshioka Y, Yamamoto Y, Ishikawa M, Ikeda SI, Kato T, Kiyono T, Takeshita F, Kajiyama H, Kikkawa F, Ochiya T. Malignant extracellular vesicles carrying MMP1 mRNA facilitate peritoneal dissemination in ovarian cancer. Nat Commun. 2017 Mar 6;8:14470.
- Osuka S, Iwase A, Nakahara T, Kondo M, Saito A, Bayasula, Nakamura T, Takikawa S, Goto M, Kotani T, Kikkawa F. Kisspeptin in the hypothalamus of two rat models of polycystic ovary syndrome. Endocrinology. 2017;158(2):367–377.
2016
- Imai K, Kotani T, Tsuda H, Mano Y, Nakano T, Ushida T, Li H, Miki R, Sumigama S, Iwase A, Hirakawa A, Ohno K, Toyokuni S, Takeuchi H, Mizuno T, Suzumura A, Kikkawa F. Neuroprotective potential of molecular hydrogen against perinatal brain injury via suppression of activated microglia. Free Radic Biol Med. 2016 Feb;91:154-63.
2014
- Yamamoto E, Niimi K, Shinjo K, Yamamoto T, Fukunaga M, Kikkawa F. Identification of causative pregnancy of gestational trophoblastic neoplasia diagnosed during pregnancy by short tandem repeat analysis. Gynecol Oncol Case Rep. 2014;9:3–6.
2012
- Niimi K, Yamamoto E, Fujiwara S, Shinjo K, Kotani T, Umezu T, Kajiyama H, Shibata K, Ino K, Kikkawa F. High expression of N-acetylglucosaminyltransferase IVa promotes invasion of choriocarcinoma. Br J Cancer. 2012;107(12):1969–1977.
MESSAGE
大学院入学案内
産婦人科学/生殖器腫瘍制御学講座では、「婦人科腫瘍」、「内分泌・腫瘍」、「周産期」、「不妊・生殖」の4つのグループに分かれて、それぞれが高度で専門的な治療と研究に積極的に取り組んでいます。
すべての専門分野を網羅し、基礎研究・臨床研究の両面において、希望の専門分野の研究が可能です。また、積極的に国内外への留学も奨励しており、海外や国内の研究施設で共同研究を行なっています。
産婦人科は、生命の誕生にもっとも深く関わり、思春期・性成熟期・老年期の女性のケアを行い、 そして婦人科腫瘍の手術を中心とした集学的治療とあらゆる年齢層の女性をターゲットとする幅広い診療分野です。
産婦人科学/生殖器腫瘍制御学講座では、多くの研修関連施設と協力しながら東海地域の産婦人科医療を担っています。 また、大学院大学としての学部学生の教育のみならず、大学院生に対する医学研究に力を注いでいます。 生命の誕生から死まで、女性のトータルサポートを行う女性総合診療科として、臨床・研究にともに取り組んでいく仲間を心から歓迎いたします。

