統合生理学
KEYWORDS
- 体温調節
- 発熱
- ストレス
- 肥満
- 中枢神経回路
- 自律神経
- 交感神経
- 褐色脂肪
- 恒常性
- プロスタグランジン
- 一次繊毛
- オキシトシン
- 1分子イメージング
- 機械受容チャネル
HEAD

LAB MEMBER
| 構成員名 | 役職 | 研究者総覧 |
|---|---|---|
| 小林 剛 | 講師 | 研究者総覧 |
| 中村 佳子 | 講師 | 研究者総覧 |
| 片岡 直也 | 特任講師 | 研究者総覧 |
| 福島 章紘 | 特任講師 | 研究者総覧 |
| 大屋 愛実 | 特任講師(JSTさきがけ研究者) | 研究者総覧 |
| 鈴木 佑治 | 助教 | 研究者総覧 |
| 北川 悠梨 | 助教 | 研究者総覧 |
| 竹本 弥佐子 | 技術補佐員 | |
| 平田 絢子 | 技術補佐員 | |
| 渡邉 佳代子 | 技術補佐員 | |
| 若林 弘子 | 秘書 |
CONTACT
| kazu◎med.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | 統合生理学 独自ホームページ |
OUTLINE
目まぐるしく変化する多様な環境でも私達が生命を維持し、活動することができるのは、体内の恒常性を自律的に維持する仕組みを備えているおかげです。この恒常性維持システムに不調をきたすと、すぐさま臨床医学的な問題(つまり疾患)が生じ、生命を脅かす事態にもつながります。本講座では、個体レベルの生理学や解剖学の手法を駆使し、恒常性維持システムの中でも体温や代謝の調節をつかさどる脳内の神経回路に焦点を当てて、その核心メカニズムを解明すべく研究を行っています。
特に最近では、心理ストレスが体温を上昇させる「心因性発熱」を起こす神経回路、飢餓の時にエネルギー消費を減らすと同時に摂食行動を促進する神経回路、快適な温度環境を探す体温調節行動の神経回路、「愛情ホルモン」オキシトシンが脂肪を燃焼させる神経路、加齢による肥満が起こる分子・細胞メカニズムの研究などにも取り組み、成果を挙げています。
また、本講座では伸展・ずり応力・圧力・重力といった力学的な刺激に対する細胞の感知/応答機構の解明にも取り組んでいます。この研究では、細胞シグナルの変換・伝達の一分子イメージング解析などのアプローチをとり研究を進めています。
研究内容については、ウェブサイトならびに研究室紹介動画もご覧ください。
RESEARCH PROJECTS
1. 恒常性維持の中枢神経回路メカニズム
これまでに私達は、体温調節の反応をコントロールしたり、感染あるいは心理ストレスを受けたときに発熱を起こしたり、飢餓のときに代謝を減らして摂食を促進する、脳の中の神経回路メカニズムを研究し、その根本的な仕組みを解明することで成果を挙げてきました(これまでに出版した代表的な総説:Am. J. Physiol., 2011; Temperature, 2015; Pflügers Arch., 2018; BioEssays, 2018; Nature Rev. Neurosci., 2022; Auton. Neurosci., 2022; 生体の科学, 2010;日本臨牀, 2012; Brain and Nerve, 2022; 生化学, 2024など)。
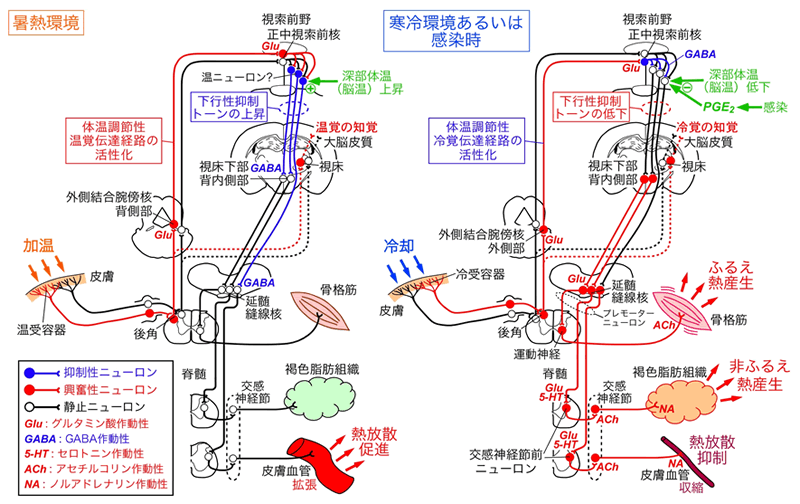
これまでに明らかになった体温調節と発熱の神経回路(K. Nakamura, Am. J. Physiol., 2011、中村和弘, 日本臨牀, 2012より)
私達は、これまでの研究成果をさらに発展させ、生体の恒常性維持(つまり生命維持)に必須の、下記の神経回路メカニズムの解明に取り組んでいます。特に、光遺伝学や薬理遺伝学など、最新の分子生物学的な研究手法を生理学や解剖学実験に取り入れることで、これまでに明らかにすることができなかった本質的な仕組みの解明を目指しています。
i) 自律的な体温調節と感染性発熱の脳内神経回路(K. Nakamura et al., J. Neurosci., 2002; J. Neurosci., 2004; Nature Neurosci., 2008; PNAS, 2010; Y. Nakamura et al., Sci. Adv., 2022など)
ii) 心理ストレスによる体温上昇(心因性発熱)や交感神経反応(頻脈など)を生み出す脳の神経回路(Kataoka et al., Cell Metab., 2014; Science, 2020など)
iii) 飢餓を生き延びるためにエネルギー消費を減らすと同時に摂食行動を促進する神経回路(Y. Nakamura et al., Cell Metab., 2017など)
iv) 快適な温度環境を探す体温調節行動の神経回路(Yahiro et al., Sci. Rep., 2017; J. Neurosci., 2023; J. Physiol., 2026)
v) 「愛情ホルモン」オキシトシンが脂肪を燃焼させる脳の神経路(Fukushima et al., Cell Rep., 2022)
vi) 加齢による肥満(中年太り)が起こる分子・細胞メカニズム(Oya et al., Cell Metab., 2024)
くわしくは独自ウェブサイトの研究内容をご覧ください。
2. 力学的な刺激に対する細胞の感知/応答メカニズム
伸展・ずり応力・圧力・重力といった力学的な刺激に対する細胞の感知/応答機構の解明にも取り組んでいます。この研究では、細胞シグナルの変換・伝達の一分子イメージング解析などのアプローチをとり研究を進めています。
BIBLIOGRAPHY
2026
- Yahiro T, Nakamura Y, Nakamura K*. The pyrogenic mediator prostaglandin E2 elicits warmth seeking via EP3 receptor-expressing parabrachial neurons: a potential mechanism of chills. J Physiol, 2026; 604(5):2110-2130.
- 片岡直也, 中村和弘. 社会的ストレスに対する自律生理反応と行動反応の社会的基盤. 週刊 医学のあゆみ, 2026; 296 (9):816-820.
- 中村和弘. 発熱の生理的意義と自律性・行動性メカニズム. 日本臨牀 2026; 84(3):346-352.
- 中村和弘. 体温調節の生理学① 体温調節の身体機構. 産業医学ジャーナル 2026; 49(2):176-181.
2025
- Xun Y, Jiang Y, Xu B, Tang M, Ludwig S, Nakamura K, Mukhopadhyay S, Liu C, Beutler B, Zhang Z. GPR45 modulates Gαs at primary cilia of the paraventricular hypothalamus to control food intake. Science, 2025; 388(6751): eadp3989.
- Pauza AG, Thakkar P, Shen X, Felippe ISA, Roßmann K, Oya M, McBryde FD, Nakamura K, Broichhagen J, Hodson DJ, Pauza DH, Murphy D, Paton JFR. Melanocortin system activates carotid body arterial chemoreceptors in hypertension. Circ Res, 2025; 137(7):967-982.
- 中村和弘. 精神的ストレスによる循環器疾患の発症機序の理解に向けて. 週刊 医学のあゆみ, 2025; 295 (9):825-829.
- 中村和弘. 脳から考える中年太りのメカニズム―過食の本当の問題. 臨床栄養, 2025; 147 (2):157-159.
- 【教科書】中村和弘. 第59章 体温とその調節 “標準生理学 第10版”(大森治紀、大橋俊夫、河合康明、黒澤美枝子 監修; 医学書院, 東京)”, 2025; 449-470.
- 【教科書】中村和弘. 第16章 体温の調節 “精解 生理学(桑名俊一 編著; 理工図書, 東京)”, 2025; 449-470.
2024
- Oya M, Miyasaka Y, Nakamura Y, Tanaka M, Suganami T, Mashimo T, Nakamura K*. Age-related ciliopathy: Obesogenic shortening of melanocortin-4 receptor-bearing neuronal primary cilia. Cell Metab, 2024; 36(5): 1044-1058.
- 中村和弘. 体温調節の中枢機構. 生化学, 2024; 96(1):12-27.
- 福島章紘, 中村和弘. 体温調節の中枢神経回路とその多様な生理的役割. Medical Science Digest, 2024; 50 (1):14-17.
- 大屋愛実, 中村和弘. 中年太りは神経細胞の一次繊毛の加齢に伴う退縮によって起こる. 実験医学, 2024; 42 (13):2075-2078.
- 【著書】Nakamura K*. Central mechanisms of thermoregulation and fever in mammals. In: Thermal Biology, ed. by Tominaga M, Takagi M: Elsevier, Advances in Experimental Medicine and Biology Vol. 1461, Pages 141-159, 2024.
- 【著書】中村和弘, 中村佳子. 体温調節と発熱の中枢司令の基本原理 “別冊 医学のあゆみ「自律神経のサイエンス」(荒木信夫 編集; 医歯薬出版)”, 2024; 22-27.
- 【著書】中村佳子, 中村和弘. 体温調節と発熱惹起を担う視索前野ニューロン “Annual Review 神経 2024(鈴木則宏、荒木信夫、宇川義一 、桑原 聡、塩川芳昭 編集; 中外医学社)”, 2024; 236-242.
- 【教科書】中村和弘. 第16章 体温の調節 “看護生理学(桑名俊一 編著; 理工図書, 東京)”, 2024; 443-466.
- 【辞典】中村和弘(共同執筆者). “生理学用語ハンドブック(日本生理学会 監修; 丸善出版)”, 2024.
2023
- Yahiro T, Kataoka N, Nakamura K*. Two ascending thermosensory pathways from the lateral parabrachial nucleus that mediate behavioral and autonomous thermoregulation. J Neurosci, 2023; 43: 5221-5240.
- Garami A, Steiner AA, Pakai E, Wanner SP, Almeida MC, Keringer P, Oliveira DL, Nakamura K, Morrison SF, Romanovsky AA. The neural pathway of the hyperthermic response to antagonists of the transient receptor potential vanilloid-1 channel. Temperature, 2023; 10: 121-135.
- Tsuji S, Brace CS, Yao R, Tanie Y, Tada H, Rensing N, Mizuno S, Almunia J, Kong Y, Nakamura K, Furukawa T, Ogiso N, Toyokuni S, Takahashi S, Wong M, Imai SI, Satoh A. Sleep-wake patterns are altered with age, Prdm13 signaling in the DMH, and diet restriction in mice. Life Sci Alliance, 2023; 6: e202301992.
- 中村和弘, 中村佳子. 体温調節と発熱の中枢司令の基本原理. 医学のあゆみ, 2023; 285(6):534-539.
- 中村和弘. 体温と代謝の中枢調節メカニズム:肥満発症機序の理解に向けて. 生体の科学, 2023; 74 (5):428-429.
- 中村和弘. 中枢神経系を介した褐色脂肪熱産生調節. 実験医学増刊, 2023; 41 (20):22-28.
- 【著書】中村和弘. 多様な環境ストレスから生命を守る脳の交感神経制御メカニズム “Annual Review 神経 2023(鈴木則宏、荒木信夫、宇川義一 、桑原 聡、塩川芳昭 編集; 中外医学社)”, 2023; 275-281.
- 【高校副読本】中村和弘. 体温調節行動を生み出す脳の感覚メカニズム “改訂版 フォトサイエンス生物図録(数研出版)”, 2023; 202-203.
2022
- Nakamura Y, Yahiro T, Fukushima A, Kataoka N, Hioki H, Nakamura K*. Prostaglandin EP3 receptor–expressing preoptic neurons bidirectionally control body temperature via tonic GABAergic signaling. Sci Adv, 2022; 8: eadd5463.
- Fukushima A, Kataoka N, Nakamura K*. An oxytocinergic neural pathway that stimulates thermogenic and cardiac sympathetic outflow. Cell Rep, 2022; 40: 111380.
- Nakamura K*, Nakamura Y, Kataoka N. A hypothalamomedullary network for physiological responses to environmental stresses. Nature Rev Neurosci, 2022; 23: 35-52.
- Nakamura K*, Morrison SF. Central sympathetic network for thermoregulatory responses to psychological stress. Auton Neurosci, 2022; 237: 102918.
- Morrison SF, Nakamura K, Tupone D. Thermoregulation in mice: The road to understanding torpor hypothermia and the shortcomings of a circuit for generating fever. Temperature, 2022; 9 (1): 8-11.
- Koba S, Kumada N, Narai E, Kataoka N, Nakamura K, Watanabe T. A brainstem monosynaptic excitatory pathway that drives locomotor activities and sympathetic cardiovascular responses. Nat Commun, 2022; 13: 5079.
- Hayashi Y, Shimizu I, Yoshida Y, Ikegami R, Suda M, Katsuumi G, Fujiki S, Ozaki K, Abe M, Sakimura K, Okuda S, Hayano T, Nakamura K, Walsh K, Jespersen NZ, Nielsen S, Scheele C, Minamino T. Coagulation factors promote brown adipose tissue dysfunction and abnormal systemic metabolism in obesity. iScience, 2022; 25 (7): 104547.
- 中村和弘. 心理ストレスによる交感神経反応を生み出す脳の神経回路. 循環器内科, 2022; 92(6): 656-661.
- 片岡直也, 中村和弘. 体温調節とストレス性交感神経反応の脳内メカニズム. 実験医学, 2022; 40(19): 3078-3084.
- 中村和弘. 心理ストレスによる褐色脂肪熱産生と体温上昇の中枢神経回路. 医学のあゆみ 2022; 280 (11): 1139-1143.
- 中村和弘. 環境ストレスに応じた体温調節の中枢神経ネットワーク. Brain and Nerve 2022; 74 (2): 143-150.
- 【著書】中村和弘. II章–6. 体温の調節機構 “自律神経:初めて学ぶ方のためのマニュアル(榊原隆次、内田さえ 編著; 中外医学社)”, 2022; 125-133.
2021
- Yoneshiro T, Kataoka N, Walejko JM, Ikeda K, Brown Z, Yoneshiro M, Crown SB, Osawa T, Sakai J, McGarrah RW, White PJ, Nakamura K, Kajimura S. Metabolic flexibility via mitochondrial BCAA carrier SLC25A44 is required for optimal fever. eLife, 2021; 10: e66865.
- Horie T, Nakao T, Miyasaka Y, Nishino T, Matsumura S, Nakazeki F, Ide Y, Kimura M, Tsuji S, Rodriguez RR, Watanabe T, Yamasaki T, Xu S, Otani C, Miyagawa S, Matsushita K, Sowa N, Omori A, Tanaka J, Nishimura C, Nishiga M, Kuwabara Y, Baba O, Watanabe S, Nishi H, Nakashima Y, Picciotto MR, Inoue H, Watanabe D, Nakamura K, Sasaki T, Kimura T, Ono K. microRNA-33 maintains adaptive thermogenesis via enhanced sympathetic nerve activity. Nat Commun, 2021; 12: 843.
- Yoshimi K, Oka Y, Miyasaka Y, Kotani Y, Yasumura M, Uno Y, Hattori K, Tanigawa A, Sato M, Oya M, Nakamura K, Matsushita N, Kobayashi K, Mashimo T. Combi-CRISPR: combination of NHEJ and HDR provides efficient and precise plasmid-based knock-ins in mice and rats. Hum Genet, 2021; 140: 277-287.
- 中村和弘. 心理ストレスによる体温上昇の中枢神経回路メカニズム. Clinical Neuroscience, 2021; 39: 724-726.
- 中村和弘. 環境ストレスを生き抜くための体温の動的制御. 月刊「細胞」, 2021; 53: 11-14.
- 片岡直也, 中村和弘. 心理ストレスに対する交感神経反応と行動反応の中枢神経メカニズム. 自律神経, 2021; 58(1): 133-138.
- 【著書】Takahashi M, Ishida Y, Kataoka N, Nakamura K, Hioki H. Efficient labeling of neurons and identification of postsynaptic sites using adeno-associated virus vector. In: Receptor and Ion Channel Detection in the Brain (2nd Ed)., ed. by Lujan R, Ciruela F: Humana, Neuromethods Vol. 169, Pages 323-341, 2021.
- 【著書】中村和弘. 多様な心理ストレス反応を制御する脳神経回路:心身相関メカニズムの理解へ “Annual Review 神経 2021(鈴木則宏、荒木信夫、宇川義一 、桑原 聡、塩川芳昭 編集; 中外医学社)”, 2021; 329-336.
2020
- Kataoka N, Shima Y, Nakajima K, Nakamura K.* A central master driver of psychosocial stress responses in the rat. Science, 2020; 367: 1105-1112.
- Kataoka N, Nakamura K. Where mind meets body: a master brain circuit for stress responses. TheScienceBreaker, 2020; doi: 10.25250/thescbr.brk404.
- 中村和弘. ストレス性体温上昇の神経機序-感染性発熱との比較から-. 心身医学, 2020; 60: 203-209.
- 片岡直也, 中村和弘. 心理ストレス反応を駆動する大脳皮質から視床下部への心身相関メカニズム. 実験医学, 2020; 38 (14): 2367-2370.
2019
- Morrison SF, Nakamura K. Central Mechanisms for Thermoregulation. Annu Rev Physiol, 2019; 81: 285-308.
- Ota W, Nakane Y, Kashio M, Suzuki Y, Nakamura K, Mori Y, Tominaga M, Yoshimura T. Involvement of TRPM2 and TRPM8 in temperature-dependent masking behavior. Sci Rep, 2019; 9: 3706.
- 中村和弘, 中村佳子. 飢餓から生命を守るための脳の仕組み. 脳神経内科, 2019; 90: 618–626.
- 中村佳子. 飢餓を生き抜く脳の仕組み. 自律神経, 2019; 56: 257–263.
- 佐藤亜希子, 中村和弘. 睡眠と体温調節能の老化変容における視床下部神経回路の役割. 基礎老化研究, 2019; 43: 23–28.
- 【著書】中村和弘. 心理や情動による交感神経反応の神経回路メカニズム:ストレスで心臓がドキドキするしくみ. “実験医学増刊号「臓器連環による生体恒常性の破綻と疾患」(春日雅人 編集; 羊土社, 東京)”, 2019; 37(7): 167-173.
2018
- Nakamura K*, Nakamura Y. Hunger and satiety signaling: Modeling two hypothalamomedullary pathways for energy homeostasis. BioEssays, 2018; 40: 1700252.
- Nakamura Y, Nakamura K.* Central regulation of brown adipose tissue thermogenesis and energy homeostasis dependent on food availability. Pflügers Arch–Eur J Physiol, 2018; 470: 823-837.
- Koba S, Hanai E, Kumada N, Kataoka N, Nakamura K, Watanabe T. Sympathoexcitation by hypothalamic paraventricular nucleus neurons projecting to the rostral ventrolateral medulla. J Physiol, 2018; 596: 4581-4595.
- 中村和弘. 多様な環境ストレスに応じた褐色脂肪熱産生調節の中枢メカニズム. 生化学, 2018; 90: 408-412.
- 中村和弘. 体温調節の行動とその神経回路メカニズム-快適な温度環境を選ぶための温度感覚とは? CLINICAL CALCIUM, 2018; 28: 65–72.
- 【著書】Nakamura K. Chapter 16 - Afferent pathways for autonomic and shivering thermoeffectors. In: Handbook of Clinical Neurology (Thermoregulation: From Basic Neuroscience to Clinical Neurology Part I), ed. by Romanovsky AA: Elsevier, Vol. 156, Pages 263-279, 2018.
- 【教科書翻訳】中村和弘. 第73章 エネルギー論と代謝速度、第74章 体温調節と発熱. “ガイトン生理学 原著第13版(石川義弘・岡村康司・尾仲達史・河野憲二 総監訳; エルゼビア, 東京)”, 2018; 823-842.
2017
- Yahiro T, Kataoka N, Nakamura Y, Nakamura K.* The lateral parabrachial nucleus, but not the thalamus, mediates thermosensory pathways for behavioural thermoregulation. Sci Rep, 2017; 7: 5031.
- Nakamura Y, Yanagawa Y, Morrison SF, Nakamura K.* Medullary reticular neurons mediate neuropeptide Y-induced metabolic inhibition and mastication. Cell Metab, 2017; 25: 322–334.
- 中村和弘, 中村佳子. 飢餓反応の中枢神経回路メカニズム. 肥満研究, 2017; 23: 161–168.
- 【著書】中村和弘. 心理ストレスによる自律生理反応を駆動する中枢神経回路機構. “ブレインサイエンス・レビュー2017(廣川信隆 編; クバプロ, 東京)”, 2017; 135-149.
2016
- Sohn J, Okamoto S, Kataoka N, Kaneko T, Nakamura K, Hioki H. Differential inputs to the perisomatic and distal-dendritic compartments of VIP-positive neurons in layer 2/3 of the mouse barrel cortex. Front Neuroanat, 2016; 10: 124.
- Chiba Y, Yamada T, Tsukita S, Takahashi K, Munakata Y, Shirai Y, Kodama S, Asai Y, Sugisawa T, Uno K, Sawada S, Imai J, Nakamura K, Katagiri H. Dapagliflozin, a sodium-glucose co-transporter 2 inhibitor, acutely reduces energy expenditure in BAT via neural signals in mice. PLoS One, 2016; 11: e0150756.
- 中村和弘. 体温を調節する中枢神経回路メカニズム. 日本神経精神薬理学雑誌, 2016; 36: 93–99.
- 中村和弘. 体温・代謝調節システムの研究から「温度生物学」への展開. 生物物理, 2016; 56: 149–153.
- 【著書】中村和弘. 体温の中枢制御機構. “Annual Review 2016 糖尿病・代謝・内分泌(寺内康夫, 伊藤 裕, 石橋 俊 編; 中外医学社, 東京)”, 2016; 80-86.
- 【教科書】中村和弘. 第15章 体温の調節. “コメディカル専門基礎科目シリーズ 生理学(桑名俊一, 荒田晶子 編; 理工図書, 東京)”, 2016; 357-378.
- 【教科書翻訳】樋口 隆, 中村和弘. 第39章 体温調節. “オックスフォード・生理学 原書4版(岡野栄之, 鯉淵典之, 植村慶一 監訳; 丸善, 東京)”, 2016; 823-836.
2015
- Nakamura K.* Neural circuit for psychological stress-induced hyperthermia. Temperature, 2015; 2: 352–361.
- 中村和弘. 心理ストレスと体温上昇. Brain and Nerve, 2015; 67: 1205–1214.
- 【著書】中村和弘. 褐色脂肪細胞の熱産生を制御する視床下部−延髄−交感神経回路. “糖尿病学2015(門脇 孝 編; 診断と治療社, 東京)”, 2015; 35–44.
2014
- Kataoka N, Hioki H, Kaneko T, Nakamura K.* Psychological stress activates a dorsomedial hypothalamus–medullary raphe circuit driving brown adipose tissue thermogenesis and hyperthermia. Cell Metab, 2014; 20: 346–358.
- Lkhagvasuren B, Oka T, Nakamura Y, Hayashi N, Sudo N, Nakamura K.* Distribution of Fos-immunoreactive cells in rat forebrain and midbrain following social defeat stress and diazepam treatment. Neuroscience, 2014; 272: 34–57.
- Hiraoka Y, Matsuoka T, Ohno M, Nakamura K, Saijo S, Matsumura S, Nishi K, Sakamoto J, Chen PM, Inoue K, Fushiki T, Kita T, Kimura T, Nishi E. Critical roles of nardilysin in the maintenance of body temperature homeostasis. Nature Commun, 2014; 5: 3224.
- 中村和弘. 体温調節機構とその異常. Clinical Neuroscience, 2014; 32: 1387–1390.
- 中村和弘. 体温調節に必要な環境温度情報の神経伝達機構. 自律神経, 2014; 51: 91–98.
- 中村和弘. 神経による褐色脂肪の機能調節. The Lipid, 2014; 25: 36–42.
- 【教科書翻訳】中村和弘. 第38章 温熱ストレスと発熱. “リッピンコットシリーズ イラストレイテッド生理学(鯉渕典之, 栗原 敏 監訳; 丸善, 東京)”, 2014; 544-552.
2013
- 【著書】中村和弘. 第3章 脳が調節する褐色脂肪組織の熱産生. “ここまでわかった 燃える褐色脂肪の不思議(斉藤昌之, 大野秀樹 編; ナップ, 東京)”, 2013; 57-77.
2012
- 近藤高史, 中村和弘. すぐき汁の味成分分析—かぶら汁との比較—. 日本味と匂学会誌, 2012; 19: 223–229.
- 中村和弘. 褐色脂肪熱産生を調節する中枢神経機構—寒冷、感染、ストレスを生き抜くために. 医学のあゆみ, 2012; 242: 913–917.
- 中村和弘. 体温調節の中枢神経機構. 日本臨牀, 2012; 70: 922-926.
2011
- Nakamura K.* Central circuitries for body temperature regulation and fever. Am J Physiol, 2011; 301: R1207–R1228.
- Lkhagvasuren B, Nakamura Y, Oka T, Sudo N, Nakamura K.* Social defeat stress induces hyperthermia through activation of thermoregulatory sympathetic premotor neurons in the medullary raphe region. Eur J Neurosci, 2011; 34: 1442–1452.
- Nakamura K*, Morrison SF. Central efferent pathways for cold-defensive and febrile shivering. J Physiol, 2011; 589: 3641–3658.
- Morrison SF, Nakamura, K. Central neural pathways for thermoregulation. Front Biosci, 2011; 16: 74-104.
- Zhang ZH, Yu Y, Wei SG, Nakamura Y, Nakamura K, Felder RB. EP3 receptors mediate PGE2-induced hypothalamic paraventricular nucleus excitation and sympathetic activation. Am J Physiol Heart Circ Physiol, 2011; 301: H1559-H1569.
- Wu S, Esumi S, Watanabe K, Chen J, Nakamura KC, Nakamura K, Kometani K, Minato N, Yanagawa Y, Akashi K, Sakimura K, Kaneko T, Tamamaki N. Tangential migration and proliferation of intermediate progenitors of GABAergic neurons in the mouse telencephalon. Development, 2011; 138: 2499–2509.
- 中村和弘. 褐色脂肪組織熱産生の中枢神経調節メカニズム. 肥満研究, 2011; 17: 87–95.
- 中村和弘. 視床下部からの交感神経遠心路. 分子精神医学,2011; 11: 23–29.
2010
- Nakamura K*, Morrison SF. A Thermosensory pathway mediating heat-defense responses. Proc Natl Acad Sci USA, 2010; 107: 8848–8853.
- 中村和弘. 体温調節のメカニズム. 自律神経, 2010; 47: 281–286.
- 中村和弘. 体温調節の中枢神経回路メカニズム. 生体の科学, 2010; 61: 276–285.
- 【著書】Garami A, Almeida MC, Nucci TB, Hew-Butler T, Soriano RN, Pakai E, Nakamura K, Morrison SF, Romanovsky AA. The TRPV1 channel in normal thermoregulation: What have we learned from experiments using different tools? In: Vanilloid Receptor TRPV1 in Drug Discovery: Targeting Pain and Other Pathological Disorders, ed. by Gomtsyan A, Faltynek CR: John Wiley & Sons, Hoboken, NJ, USA, 2010; 351-402.
2009
- Nakamura Y, Nakamura K*, Morrison SF. Different populations of prostaglandin EP3 receptor-expressing preoptic neurons project to two fever-mediating sympathoexcitatory brain regions. Neuroscience, 2009; 161: 614–620.
- Romanovsky AA, Almeida MC, Garami A, Steiner AA, Norman MH, Morrison SF, Nakamura K, Burmeister JJ, Nucci TB The transient receptor potential vanilloid-1 channel in thermoregulation: a thermosensor it is not. Pharmacol Rev, 2009; 61: 228–261.
- Manczak M, Mao P, Nakamura K, Bebbington C, Park B, Reddy PH. Neutralization of granulocyte macrophage colony-stimulating factor decreases amyloid beta 1-42 and suppresses microglial activity in a transgenic mouse model of Alzheimer's disease. Hum Mol Genet, 2009; 18: 3876–3893.
- Reddy PH, Manczak M, Zhao W, Nakamura K, Bebbington C, Yarranton G, Mao P. Granulocyte-macrophage colony-stimulating factor antibody suppresses microglial activity: implications for anti-inflammatory effects in Alzheimer's disease and multiple sclerosis. J Neurochem, 2009; 111: 1514–1528.
2008
- Nakamura K*, Morrison SF. Preoptic mechanism for cold-defensive responses to skin cooling. J Physiol, 2008; 586: 2611–2620.
- Nakamura K*, Morrison SF. A thermosensory pathway that controls body temperature. Nature Neurosci, 2008; 11: 62–71.
- Morrison SF, Nakamura K, Madden CJ. Central control of thermogenesis in mammals. Exp Physiol, 2008; 93: 773–797.
- Tsuchiya H, Oka T, Nakamura K, Ichikawa A, Saper CB, Sugimoto Y. Prostaglandin E2 attenuates preoptic expression of GABA(A) receptors via EP3 receptors. J Biol Chem, 2008; 283: 11064–11071.
2007
- Nakamura K*, Morrison SF. Central efferent pathways mediating skin cooling-evoked sympathetic thermogenesis in brown adipose tissue. Am J Physiol, 2007; 292: R127–R136.
2006
- Nakamura K*, Yamashita Y, Tamamaki N, Katoh H, Kaneko T, Negishi M. In vivo function of Rnd2 in the development of neocortical pyramidal neurons. Neurosci Res, 2006; 54: 149–153.
- 中村和弘. 発熱及び体温調節の交感神経経路. 自律神経, 2006; 43: 44–51.
2005
- Nakamura Y, Nakamura K*, Matsumura K, Kobayashi S, Kaneko T, Morrison SF. Direct pyrogenic input from prostaglandin EP3 receptor-expressing preoptic neurons to the dorsomedial hypothalamus. Eur J Neurosci, 2005; 22: 3137–3146.
- Nakamura K*, Matsumura K, Kobayashi S, Kaneko T. Sympathetic premotor neurons mediating thermoregulatory functions. Neurosci Res, 2005; 51: 1–8.
- Wu SX, Goebbels S, Nakamura Ko, Nakamura Ka, Kometani K, Minato N, Kaneko T, Nave KA, Tamamaki N. Pyramidal neurons of upper cortical layers generated by NEX-positive progenitor cells in the subventricular zone. Proc Natl Acad Sci USA, 2005; 102: 17172–17177.
2004
- Nakamura K*, Matsumura K, Hübschle T, Nakamura Y, Hioki H, Fujiyama F, Boldogköi Z, König M, Thiel HJ, Gerstberger R, Kobayashi S, Kaneko T. Identification of sympathetic premotor neurons in medullary raphe regions mediating fever and other thermoregulatory functions. J Neurosci, 2004; 24: 5370–5380.
- Nakamura K*, Wu SX, Fujiyama F, Okamoto K, Hioki H, Kaneko T. Independent inputs by VGLUT2- and VGLUT3-positive glutamatergic terminals onto rat sympathetic preganglionic neurons. NeuroReport, 2004; 15: 431–436.
- Nakamura K.* Fever-inducing sympathetic neural pathways. J Therm Biol, 2004; 29: 339–344.
- Kopp UC, Cicha MZ, Nakamura K, Nüsing RM, Smith LA, Hökfelt T. Activation of EP4 receptors contributes to prostaglandin E2 mediated stimulation of renal sensory nerves. Am J Physiol Renal Physiol, 2004; 287: F1269–F1282.
- Hioki H, Fujiyama F, Nakamura K, Wu SX, Matsuda W, Kaneko T. Chemically specific circuit composed of vesicular glutamate transporter 3- and preprotachykinin B-producing interneurons in the rat neocortex. Cereb. Cortex, 2004; 14: 1266–1275.
2003
- Yoshida K, Nakamura K, Matsumura K, Kanosue K, König M, Thiel HJ, Boldogköi Z, Toth I, Roth J, Gerstberger R, Hübschle T. Neurons of the rat preoptic area and the raphe pallidus nucleus innervating the brown adipose tissue express the prostaglandin E receptor subtype EP3. Eur J Neurosci, 2003; 18: 1848–1860.
2002
- Nakamura K*, Matsumura K, Kaneko T, Kobayashi S, Katoh H, Negishi M. The rostral raphe pallidus nucleus mediates pyrogenic transmission from the preoptic area. J Neurosci, 2002; 22: 4600–4610.
- Mouihate A, Clerget-Froidevaux MS, Nakamura K, Negishi M, Wallace JL, Pittman QJ. Suppression of fever at near term is associated with reduced COX-2 protein expression in rat hypothalamus. Am J Physiol Regul Integr Comp Physiol, 2002; 283: R800–R805.
- Ishikawa Y, Katoh H, Nakamura K, Mori K, Negishi M. Developmental changes in expression of small GTPase RhoG mRNA in the rat brain. Brain Res Mol Brain Res, 2002; 106 145–150.
- 【著書】中村和弘. Question 38 PG受容体およびTX受容体について概説してください. “これだけは知っておきたいアラキドン酸カスケードQ&A(室田誠逸 編; 医薬ジャーナル社, 大阪)”, 2002; 124–126.
2001
- Nakamura K*, Li YQ, Kaneko T, Katoh H, Negishi M. Prostaglandin EP3 receptor protein in serotonin and catecholamine cell groups: a double immunofluorescence study in the rat brain. Neuroscience, 2001; 103: 763–775.
2000
- Nakamura K*, Kaneko T, Yamashita Y, Hasegawa H, Katoh H, Negishi M. Immunohistochemical localization of prostaglandin EP3 receptor in the rat nervous system. J Comp Neurol, 2000; 421: 543–569.
- Yamaguchi Y, Katoh H, Yasui H, Aoki J, Nakamura K, Negishi M. Gα(12) and Gα(13) inhibit Ca(2+)-dependent exocytosis through Rho/Rho-associated kinase-dependent pathway. J Neurochem, 2000; 75: 708–717.
- Hasegawa H, Katoh H, Yamaguchi Y, Nakamura K, Futakawa S, Negishi M. Different membrane targeting of prostaglandin EP3 receptor isoforms dependent on their carboxy-terminal tail structures. FEBS Lett, 2000; 473: 76–80.
- Negishi M, Katoh H, Nakamura K, Aoki J, Fujita H. Molecular aspects of functions of prostaglandin E receptors in CNS. Recent Res Devel Endocrinol, 2000; 1: 133–143.
1999
- Nakamura K, Kaneko T, Yamashita Y, Hasegawa H, Katoh H, Ichikawa A, Negishi M. Immunocytochemical localization of prostaglandin EP3 receptor in the rat hypothalamus. Neurosci Lett, 1999; 260: 117–120.
- Hasegawa H, Fujita H, Katoh H, Aoki J, Nakamura K, Ichikawa A, Negishi M. Opposite regulation of transepithelial electrical resistance and paracellular permeability by Rho in Madin-Darby canine kidney cells. J Biol Chem, 1999; 274: 20982–20988.
- Aoki J, Katoh H, Yasui H, Yamaguchi Y, Nakamura K, Hasegawa H, Ichikawa A, Negishi M. Signal transduction pathway regulating prostaglandin EP3 receptor-induced neurite retraction: requirement for two different tyrosine kinases. Biochem J, 1999; 340: 365–369.
- Satoh S, Chang CS, Katoh H, Hasegawa H, Nakamura K, Aoki J, Fujita H, Ichikawa A, Negishi M. The key amino acid residue of prostaglandin EP3 receptor for governing G protein association and activation steps. Biochem Biophys Res Commun, 1999; 255: 164–168.
1998
- Nakamura K, Katoh H, Ichikawa A, Negishi M. Inhibition of dopamine release by prostaglandin EP3 receptor via pertussis toxin-sensitive and -insensitive pathways in PC12 cells. J Neurochem, 1998; 71: 646–652.
MESSAGE
当研究室は生体の恒常性を維持する仕組みの本質を解明することを目指しており、人材育成の観点では、世界で通用する生理学者・生命科学者の養成を使命としています。「生命がどのようにして成り立っているのか?」という医学・生物学の大きな問題に取り組みたいという意欲的な大学院生を募集します。医学部以外の学部の出身者も歓迎します。医学修士課程から入学し、博士課程に進学する道を経れば、じっくりと時間をかけて大きなプロジェクトに取り組むこともできます。
私達が得意とする実験は、in vivo生理実験、神経解剖学実験、行動解析実験などですが、これに加えて、最新の光遺伝学や遺伝薬理学などの分子生物学的手法を取り入れ、分子レベルと個体レベルの解析や知見をつなぐことで、これまでに誰も明らかにできなかった大きな問題に取り組んでいます。当研究室に入門した大学院生は、まず、こうした実験技術の習得を通じて、生命科学研究に必要な基礎的な知識や技術的なバックグラウンドに関して指導を受けます。大学院生の研究プロジェクトの進め方は、指導教官との頻繁なディスカッションやラボミーティングでの議論を通じて決定します。場合によっては、プロジェクトの推進に必要な技術を国内外の他研究室にて習得することもあります。独力で実験することができるようになったら、自主性を尊重した形でプロジェクトを進めてもらいます。国際学会での発表や国際誌への論文執筆などを通じて英語や論理的思考の能力を養い、また、国際的感覚を身につけます。
このような研究に興味を持ち、世界と渡り合う研究者を目指す学生は、まず、当研究室の責任者へご連絡ください。研究室見学を随時受け付けています。また、日本学術振興会特別研究員(博士課程学生あるいはポスドク)として申請し、受け入れることも可能ですので、ご相談ください。

