ウイルス学
KEYWORDS
- ウイルス病原性の分子基盤の解明
- ヘルペスウイルス
- Epstein-Barrウイルス
- RNAウイルス
HEAD

LAB MEMBER
CONTACT
| med◎t.mail.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | ウイルス学 独自ホームページ |
OUTLINE
ウイルスはヒトを初めとした宿主に様々な疾病をもたらします。ウイルスは健常人・免疫不全宿主に重篤な感染症を引き起こすのみならず、肝癌・子宮頚癌・白血病・悪性リンパ腫などの「がん」の原因にもなります。ヘルペスウイルス、インフルエンザウイルス、肝炎ウイルス、HIVなどのウイルスが引き起こす疾患を「制する」ことは、現代社会において極めて重要なチャレンジです。私たちの研究室では、Epstein-Barrウイルスや単純ヘルペスウイルスなどのヒトヘルペスウイルスやインフルエンザウイルスやコロナウイルスなどのRNAウイルスを中心に、ウイルス病原性の分子基盤の解明、ウイルス疾患の診断・制御・治療法の開発など先駆的な研究を行っています。
RESEARCH PROJECTS
EBV の腫瘍原性と宿主の生体応答/疾患発症メカニズムの解析
Epstein-Barr ウイルス(EBV) はほとんどの成人が感染しており、ときに慢性活動性EBV 感染症、悪性リンパ腫や上咽頭がん・胃がんなどの腫瘍性疾患を引き起こします。EBV がもつ約80 個の遺伝子は、感染細胞の増殖、タンパク質/DNA の産生や、免疫系からの回避、シグナル伝達や膜輸送系の制御など、自身の生存に重要な役割を担っていますが、その多くは分かっていません。本研究室では最先端の解析装置、実験手法を駆使し、EBV の増殖と宿主の生体応答/ 疾患の発症メカニズムを解析することで、EBV 疾患の克服と共生への道を目指しています。私たちは本研究分野において世界をリードすると同時に、積極的に多業界とのコラボレーションで新しい可能性を展開します。
1.身近なウイルスが「がん」を引き起こす仕組みの解明
目的: ごく一部のヒトにおいて、EBV はがんや、その他の難病を発症します。そのメカニズムを解明するために、患者の遺伝子とウイルスの遺伝子の両方を、次世代シーケンサーを用い、網羅的遺伝子解析します。
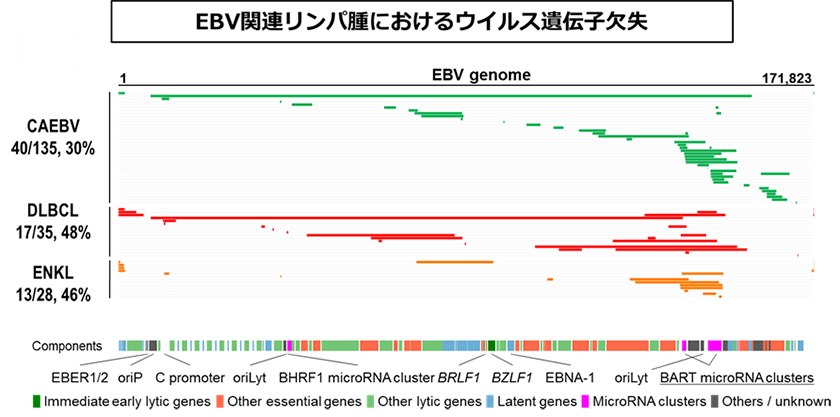
内容: 難治性のリンパ増殖性疾患である慢性活動性EBV 感染症に関わるEBV は、いくつかの重要な遺伝子を欠失していることを見出しました。また、このような欠失EBV は他のEBV 関連悪性リンパ腫でも見られること、欠失EBV はウイルス遺伝子発現を活性化させ、腫瘍化を促進していることを明らかにしました。( Okuno Y et al,. Nat Microbiol 2019 )。
期待される成果: 今回明らかになったウイルス発がんの仕組みに基づき、より良い治療法の開発が進むことが、今後、期待されます。
2.生命現象を利用し、細胞を乗っ取るEBV の生存を支えるタンパク質の研究
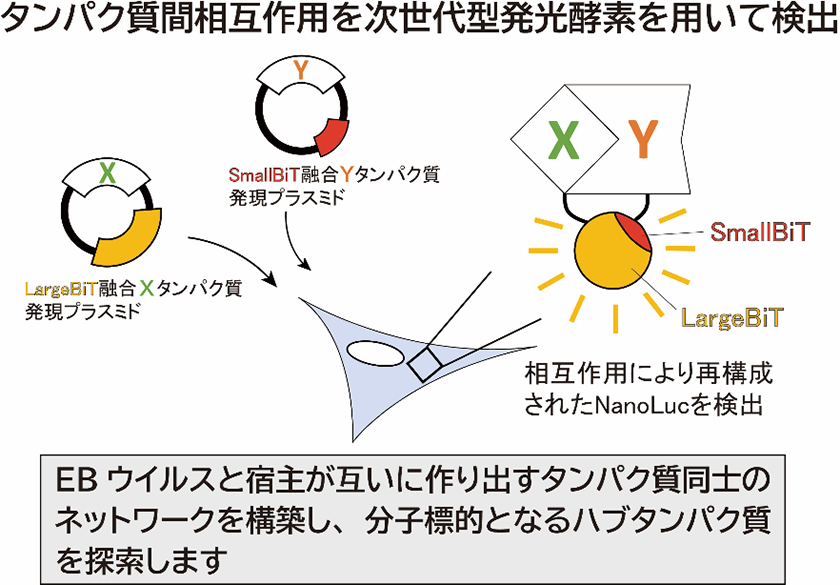
目的: EBVと宿主が互いに作り出すタンパク質同士のネットワークを明らかにし、ウイルスの生存に重要な「ハブタンパク質」を探索します。理論的計算科学分野における創発システム研究者と一体となり連携研究を行います。
内容: ヒト細胞内で起こるタンパク質間の相互作用を、次世代型発光テクノロジーを用いてリアルタイムかつ定量的に検出します。
期待される成果: 感染細胞で起こるタンパク質間相互作用についての動的理解と、ネットワークの「ハブタンパク質」としての素性を解明し、分子標的薬のクリエイトを目指します。
3.ウイルスはどうやって免疫反応から逃れている? ウイルスの免疫回避メカニズムを研究
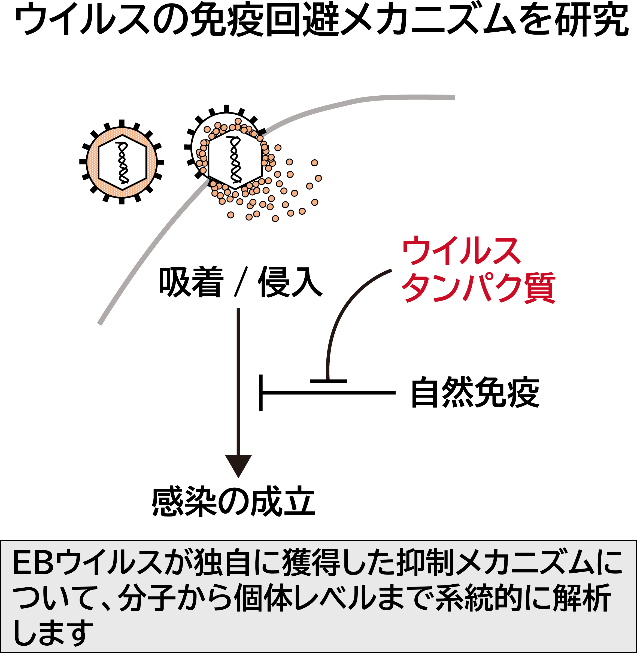
目的: ヒト細胞内では病原体の特異構造を認識し、免疫反応を誘導します。ヒトに病気を起こすウイルスの多くは、この免疫反応を抑制するシステムを進化的に獲得しています。感染から病気の発症の過程において、EBV が獲得したさまざまな免疫回避システムを実証します。
内容: 免疫応答の誘導のきっかけを作るさまざまな核酸センサー分子、シグナル伝達との関係についてウイルス学、免疫学、薬理学などさまざまな分野の実験手法により推進します ( Watanabe T et al.,J Virol 2015: Watanabe T et al.,Cancer Sci 2020 ) 。
期待される成果: ウイルス独自の強力な免疫抑制システムを分子レベルで理解することは、今後のワクチン開発に重要となるとともに、自己免疫疾患や新型コロナウイルス感染症によって引き起こされる過剰免疫反応を制御するための応用研究を創成します。
ウイルス感染に関わる宿主因子の包括的な探索
人類は常にウイルス感染に晒されています。病原性のないものから致死的なものまで様々なヒトに感染するウイルスが存在しますが、抗ウイルス薬が未だ存在しないウイルスがほとんどです。たとえ、抗ウイルス薬があったとしても、その大半はウイルス因子を標的としており、ウイルスの変異による薬剤耐性ウイルスが問題となります。ウイルスは自身単独では増殖出来ず、必ず宿主が必要になります。そのため、ウイルスが利用する宿主因子の同定およびその分子基盤の解明は、抗ウイルス薬の開発に非常重要な知見となります。
例えば、ヒト発癌ウイルスの一つであるEpstein-Barrウイルス(EBV) の遺伝子発現を制御する宿主因子の探索では、95 種類のキナーゼ阻害剤小分子ライブラリーから複数のCyclin-dependent kinase (CDK) 阻害剤を同定しました。ウイルスタンパク質BDLF4 は宿主CDK2 によりリン酸化され、EBV 遺伝子発現の時間的な制御をしていることを明らかにしました( Sato Y et al.,J Virol 2019 )。実際に、alsterpaullone 2-Cyanoethyl およびalsterpaullone は、 in vitro で抗EBV 活性があるとされるガンシクロビル(ganciclovir; GCV) よりも低濃度でEBV 感染性粒子産生を抑制しました( 特願 2017-250093 ・佐藤, 渡辺, 木村・抗ウイルス薬・名古屋大学・2017 年12 月26 日 )。
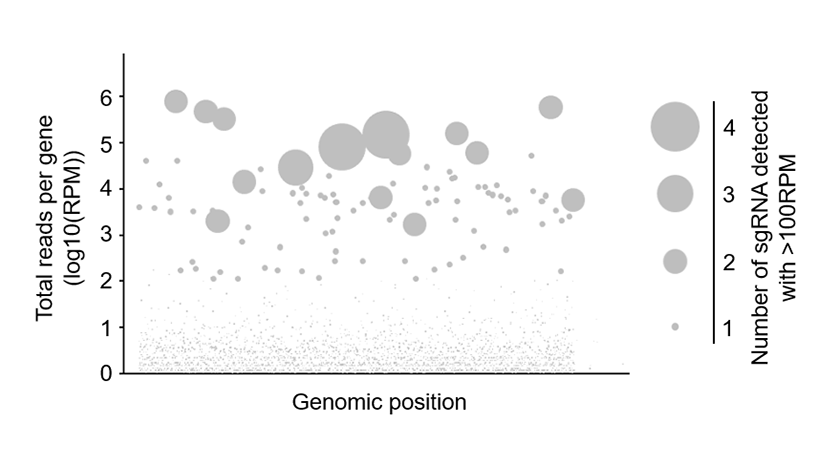
また、ヒト単純ヘルペスウイルスは2 つの血清型(HSV-1 とHSV-2 )が存在し、ヒトに脳炎、口唇ヘルペス、性器ヘルペス、皮膚疾患、眼疾患など多彩な疾患を引き起こす臨床的に重要なウイルスです。HSV 感染症にはアシクロビルなどの抗ヘルペスウイルス薬が存在するにもかかわらず、未だ臨床上の問題が多く存在するのはHSV 感染の病態が十分に解明されていないことも原因の一つであり、これに迫るCRISPR スクリーニングを実施しています。HSV 感染に抵抗性を示す細胞群を次世代シーケンサーで解析し、責任遺伝子を同定すると、いくつかの遺伝子が高度に濃縮されていることが明らかとなりました(図)。
私たちが構築している遺伝子欠損細胞ライブラリーは、CRISPR/Cas9 システムを用いたもので、約19,000 のヒト遺伝子をカバーしています。感染すると細胞死を引き起こすウイルスや、感染が成立すると蛍光タンパク質を発現する改変ウイルスなどを用いることで、ウイルス感染抵抗性を示す変異細胞を選択することができるため、様々なウイルス種に対して、感染に必要な宿主因子の同定が可能と考えています。
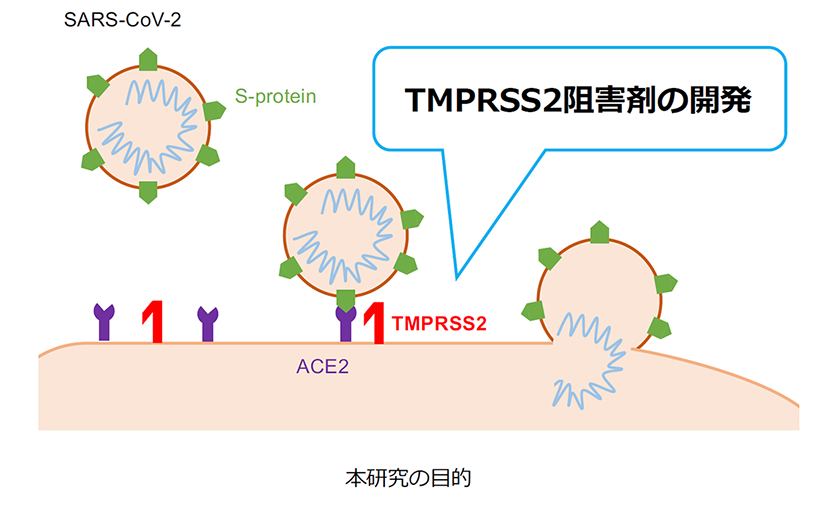
新型コロナウイルスの細胞内侵入に関わるTMPRSS2を阻害する分子の開発
2019年12 月に中国 武漢市で患者が確認された新型コロナウイルス(SARS-CoV-2 )による感染症(COVID-19 )は、短期間で世界中に拡散した。COVID-19 は公衆衛生上の問題に留まらず、その影響は経済・文化など、私たちの生活様式を一変させるまでに至った。現時点(2020 年12 月)でも感染を制御できず、感染者は増加の一途を辿る。
SARS-CoV-2はエンベロープに存在するSpike タンパク質(S タンパク質)が、細胞膜に存在するACE2 受容体に結合し、細胞内へ侵入し感染する。S タンパク質はFurin と想定される宿主プロテアーゼによりS1 とS2 に切断される。S1 は受容体であるACE2 受容体に結合し、S2 が細胞表面のセリンプロテアーゼTMPRSS2 によって、さらに切断されることで、膜融合が進行する(Hoffman et al ., Cell , 2020 )。この膜融合は、急性膵炎治療薬であるセリンプロテアーゼ阻害剤のカモスタットやナファモスタットにより阻害されることが報告され(Hoffman et al ., Cell , 2020; Yamamoto et al ., Viruses , 2020 )、臨床試験も始まっている。
共同研究者の藤本和宏博士(名古屋大学ITbM )がナファモスタットとTMPRSS2 との結合をドッキングシミュレーションにより評価したところ、ナファモスタットはTMPRSS2 の活性部位に強く結合することが予測された。さらに、ドッキングシミュレーションと共同研究者の佐藤綾人博士(名古屋大学ITbM )による分子設計を繰り返すことで、ナファモスタットの官能基を適切に置換した誘導体がTMPRSS2 に対してさらに強く結合することが予測された。計算結果をもとに、改良型ナファモスタットの合成に共同研究者の大松亨介博士(名古屋大学ITbM )が成功し、その抗ウイルス効果を検討した(一部は、藤田医科大学村田貴之教授との共同研究)。
改良型ナファモスタットは、新型コロナウイルス(SARS-CoV-2 )および旧型コロナウイルス感染(HCoV-229E およびHCoV-OC43 )に伴う細胞変性効果をナファモスタットに比べて、より低濃度で抑制した(強い抗ウイルス効果を示した)。現在、本研究結果の論文を執筆中である。今後は改良型ナファモスタットがより強い抗ウイルス効果を示した分子メカニズムについて詳細に解析をし、更なる改良を試みる予定である。
新興・再興RNAウイルスの細胞内侵入メカニズムの分子機構解明
毎年のように流行するインフルエンザウイルスは、時に世界中にパンデミックを引き起こします。A 型インフルエンザウイルスが細胞に感染し、細胞の内部へ侵入していく過程の分子機構の詳細は未だ明らかとなっていません。我々はウイルスの細胞内への侵入時に機能している宿主タンパク質を同定し、その分子機能の解明に取り組んでいます。
これまでにエンドサイトーシスによって細胞内に取り込まれたウイルスが、自身に含まれるユビキチン鎖を利用し、ストレス応答因子と考えられる宿主ヒストン脱アセチル化酵素ファミリーの一つであるHDAC6 を呼び寄せ、ゲノムRNA をエンドソームから細胞質内に放出すること(脱殻)を明らかにしてきました( Banerjee, Miyake et al., Science 2014 ) 。さらに、この宿主因子であるHDAC6 の酵素活性ドメインの分子構造を世界で初めて明らかにしました( Miyake et al., Nat Chem Biol 2016 ) 。最近、核輸送に関わる宿主因子のsiRNA によるスクリーニングから新たにトランスポーチン1(TNPO1) を同定し、TNPO1 がインフルエンザウイルスの殻を構成しているM1 タンパク質と相互作用することで、ウイルスゲノムRNA を細胞質内に分散させていることも明らかにしました( Miyake et al., Nat Microbiol 2019 ) 。これらの結果はウイルスが宿主タンパク質の機能を巧妙に利用することで細胞内へ侵入していること示しています。
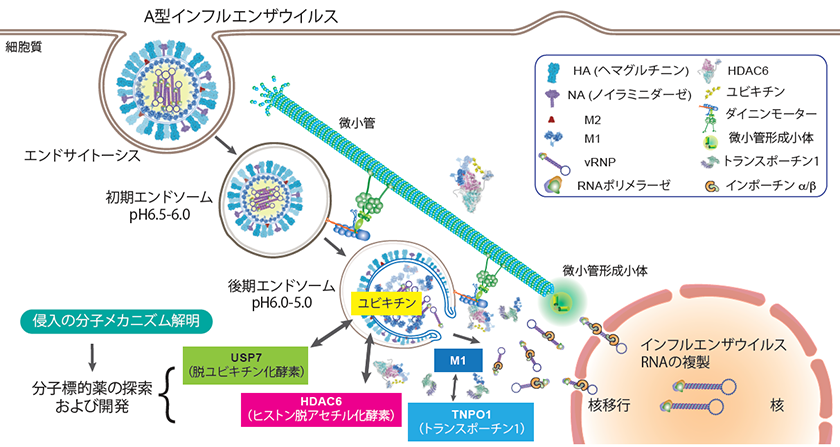
これまでの結果を踏まえ、現在、ウイルスのユビキチンシグナルがどのようにHDAC6 を呼び寄せるのか、その詳細を分子生物学的に解析しています。インフルエンザウイルスの細胞内侵入における宿主因子の分子機能を明らかにすることで、宿主タンパク質を標的とした新規抗ウイルス薬の探索および開発を目指しています。
本研究は、英国ブリストル大学の山内洋平博士(https://www.yamauchilab.com) およびスイスFriedrich Miescher Institute for Biomedical Research (FMI) のPatrick Matthias博士(https://www.fmi.ch/research-groups/groupleader.html?group=21) らと国際共同研究を展開しており、新興RNA ウイルスである新型コロナウイルス(SARS-CoV-2) の細胞内侵入にも共通のメカニズムがあるのか、現在、検証しているところです。
BIBLIOGRAPHY
2026
- Sato Y, Okuno Y, Murata T, Kimura H. Epstein–Barr virus-associated T/NK-cell neoplasms. J Med Virol, in press
- Kimura H, Cohen JI. Chronic Active Epstein–Barr Virus Disease: Molecular Pathogenesis, Evolving Concepts, and Emerging Therapies. Blood, in press
- Umeda M, Yoshimura K, Sato Y, Miyake Y, Kimura H Endosomal maturation leads to nucleocapsid conformation change in seasonal coronaviruses. Nagoya J Med Sci, in press
2025
- Bartlett A, Krejdovsky C, Yang G, Barry AP, Oduor C, Bailey JA, Moormann AM, Sato Y, Luftig MA. bioRxiv [Preprint]. 2025 Dec 19:2025.12.19.695354. doi: 10.64898/2025.12.19.695354. PMID: 41446165
- Sato Y, Okuno Y, Murata T, Kimura H. Defective But Tumorigenic: The Evolutionary and Functional Roles of Mutated Oncoviruses. FEMS Microbiol Rev. 2025 Jan 14:49:fuaf048. doi: 10.1093/femsre/fuaf048. PMID: 41004261
- Park H, Nakamura N, Miyamoto S, Sato Y, Kim KS, Kitagawa K, Kobashi Y, Tani Y, Shimazu Y, Zhao T, Nishikawa Y, Omata F, Kawashima M, Abe T, Saito Y, Nonaka S, Takita M, Yamamoto C, Morioka H, Kato K, Sagou K, Yagi T, Kawamura T, Sugiyama A, Nakayama A, Kaneko Y, Shibata RY, Aihara K, Kodama T, Kamiyama A, Tamura T, Fukuhara T, Shibuya K, Suzuki T, Iwami S, Tsubokura M. Longitudinal antibody titers measured after COVID-19 mRNA vaccination can identify individuals at risk for subsequent infection. Sci Transl Med. 2025 Sep 17;17(816):eadv4214. doi: 10.1126/scitranslmed.adv4214. Epub 2025 Sep 17. PMID: 40961221 プレスリリース/解説 ※本HP内の一番下に掲載中です。
- Aleksic B, Arthur A, Kasai-Prince M, Chretien B, Bustos-Villalobos I, Plewa C, Kasuya H, Page AJ, Zannettino ACW, Kimura H. The Nagoya University and the University of Adelaide Joint PhD Degree Program in Medicine - A Program of Opportunity. Adv Med Educ Pract. 2025 Sep 6;16:1635-1640. doi: 10.2147/AMEP.S526211. eCollection 2025.PMID: 40949886
- Kimura H, Chan JKC, Ng S-B, Sangueza JM, Tan SY. Severe mosquito bite allergy: WHO Classification of Tumours 5th ed., Vol.12, Skin Tumours. Who Classification of Tumours Editorial Board eds, WHO Press, Lyon, p430-431, 2025
- Kimura H, Chan JKC, Plaza JA, Sangueza JM. Hydroa vacciniforme lymphoproliferative disorder: WHO Classification of Tumours 5th ed., Vol.12, Skin Tumours. Who Classification of Tumours Editorial Board eds, WHO Press, Lyon, p432-433, 2025
- Khine HT, Sato Y, Hamada M, Umeda M, Iizuka A, Son S, Arai H, Kojima Y, Watanabe T, Naruse A, Goto K, Ohshima K, Akutsu Y, Nakaguro M, Satou A, Kataoka H, Ito Y, Sawada A, Kato S, Kawada JI, Murata T, Okuno Y, Kimura H. Association of Epstein–Barr viral genomic alterations to human pathologies. Blood. 2025 Sep 25;146(13):1533-1545. doi: 10.1182/blood.2024028055. PMID: 40569273 プレスリリース/解説 ※本HP内の一番下に掲載中です。
- Yabushita T, Yamashita D, Imai Y, Kimura H, Ishikawa T. Elderly-onset Hydroa Vacciniforme Lymphoproliferative Disorder. Int Med. 2025 Jul 24. doi: 10.2169/internalmedicine.5574-25. Online ahead of print. PMID: 40707220
- Sato Y, Hatanaka Y, Sato Y, Matsumoto K, Osana S, Nagatomi R, Nishizawa S. Viral Membrane-Targeting Amphipathic Helical Peptide-Based Fluorogenic Probes for the Analysis of Infectious Titers of Enveloped Viruses. Anal Chem. 2025 Mar 18;97(10):5480-5487. doi: 10.1021/acs.analchem.4c04852. Epub 2025 Jan 22. PMID: 39840494 プレスリリース/解説 ※本HP内の一番下に掲載中です。
- Kojima Y, Hamada M, Naruse A, Goto K, Khine HT, Arai H, Akutsu Y, Satou A, Nakaguro M, Kato S, Kodera Y, Yatabe Y, Torii Y, Kawada JI, Murata T, Kimura H, Takiguchi S, Inagaki H, Kataoka H, Okuno Y. The landscape of 142 Epstein-Barr viral whole genomes in gastric cancer. J Gastroenterol. 2025 Jan;60(1):55-65. doi: 10.1007/s00535-024-02170-3. Epub 2024 Nov 21. PMID: 39572460
2024
- Adachi Y, Terakura S, Osaki M, Okuno Y, Sato Y, Sagou K, Takeuchi Y, Yokota H, Imai K, Steinberger P, Leitner J, Hanajiri R, Murata M, Kiyoi H. Cullin-5 deficiency promotes chimeric antigen receptor T cell effector functions potentially via the modulation of JAK/STAT signaling pathway. Nat Commun. 2024 Dec 10;15(1):10376. doi: 10.1038/s41467-024-54794-x. PMID: 39658572 プレスリリース/解説 ※本HP内の一番下に掲載中です。
- Kimura H, Araujo I, Kato S, Ng S-B. Severe mosquito bite allergy: WHO Classification of Tumours Haematolymphoid tumours. Who Classification of Tumours Editorial Board eds. 5th ed, WHO Press, Lyon, p772-773, 2024
- Kimura H, Plaza JA, Araujo I, Rao HL, Chan JKC, Sangueza JM, Gru A. Hydroa vacciniforme lymphoproliferative disorder: WHO Classification of Tumours Haematolymphoid tumours. Who Classification of Tumours Editorial Board eds. 5th ed, WHO Press, Lyon, p774-776, 2024
- Araujo I, Kimura H, Liu WP, Sangueza OP. Systemic chronic active EBV disease: WHO Classification of Tumours Haematolymphoid tumours. Who Classification of Tumours Editorial Board eds. 5th ed, WHO Press, Lyon, p777-778, 2024
- Fujikawa Y, Kato K, Unno K, Narita S, Okuno Y, Sato Y, Takefuji M, Murohara T. Dynamic upregulation of retinoic acid signal in the early postnatal murine heart promotes cardiomyocyte cell cycle exit and maturation. Sci Rep. 2024 Aug 30;14(1):20222. doi: 10.1038/s41598-024-70918-1. PMID: 39215116
- Corrigendum: Inagaki T, Sato Y, Ito J, Takaki M, Okuno Y, Yaguchi M, Masud HMAA, Watanabe T, Sato K, Iwami S, Murata T, Kimura H. Direct evidence of abortive lytic infection-mediated establishment of Epstein-Barr virus latency during B-cell infection. Front Microbiol. 2024 May 23;15:1426311. doi: 10.3389/fmicb.2024.1426311. eCollection 2024. PMID: 38846570
- Nakamura N, Kobashi Y, Kim KS, Park H, Tani Y, Shimazu Y, Zhao T, Nishikawa Y, Omata F, Kawashima M, Yoshida M, Abe T, Saito Y, Senoo Y, Nonaka S, Takita M, Yamamoto C, Kawamura T, Sugiyama A, Nakayama A, Kaneko Y, Jeong YD, Tatematsu D, Akao M, Sato Y, Iwanami S, Fujita Y, Wakui M, Aihara K, Kodama T, Shibuya K, Iwami S, Tsubokura M. Modeling and predicting individual variation in COVID-19 vaccine-elicited antibody response in the general population. PLOS Digit Health. 2024 May 3;3(5):e0000497. doi: 10.1371/journal.pdig.0000497. eCollection 2024 May. PMID: 38701055
- Suzuki T, Sato Y, Okuno Y, Torii Y, Fukuda Y, Haruta K, Yamaguchi M, Kawamura Y, Hama A, Narita A, Muramatsu H, Yoshikawa T, Takahashi Y, Kimura H, Ito Y, Kawada JI. Single-cell transcriptomic analysis of Epstein-Barr virus-associated hemophagocytic lymphohistiocytosis. J Clin Immunol. 2024 Apr 20;44(4):103. doi: 10.1007/s10875-024-01701-0. PMID: 38642164
- Sagou K, Sato Y, Okuno Y, Watanabe T, Inagaki T, Motooka Y, Toyokuni S, Murata T, Kiyoi H, Kimura H. Epstein-Barr virus lytic gene BNRF1 promotes B-cell lymphomagenesis via IFI27 upregulation. PLoS Pathog. 2024 Feb 1;20(2):e1011954. doi: 10.1371/journal.ppat.1011954. eCollection 2024 Feb. PMID: 38300891 プレスリリース/解説 ※本HP内の一番下に掲載中です。
- Miyake Y, Hara Y, Umeda M, Banerjee I. Influenza A virus: Cellular entry. Subcell Biochem. 2023;106:387-401. doi: 10.1007/978-3-031-40086-5_14. PMID: 38159235
- Kimura H, Murata T. Understanding the Role of EBV Infection in Lymphomagenesis; Precision Cancer Therapies vol 2. O’Connor OA ed, Wiley-Blackwell, p235-45, 2024
2023
- Fukaura R, Terashima-Murase C, Tanahashi K, Sato Y, Kawase M, Kato K, Akiyama M. Generalized Verrucosis on a Background of 3C Syndrome Treated With Subcutaneous IgG Supplementation. JAMA Dermatol. 2023 Dec 1;159(12):1397-1399. doi: 10.1001/jamadermatol.2023.3801. PMID: 37851466
- Kawada JI, Ito Y, Ohshima K, Yamada M, Kataoka S, Muramatsu H, awada A, Wada T, Imadome KI, Arai A, Iwatsuki K, Ohga S, Kimura H. Updated guidelines for chronic active Epstein-Barr virus disease. Int J Hematol. 2023 Nov;118(5):568-576. doi: 10.1007/s12185-023-03660-5. Epub 2023 Sep 20. PMID: 37728704
- Taga S, Suga H, Nakano T, Kuwahara A, Inoshita N, Kodani Y, Nagasaki H, Sato Y, Tsumura Y, Sakakibara M, Soen M, Miwata T, Ozaki H, Kano M, Watari K, Ikeda A, Yamanaka M, Takahashi Y, Kitamoto S, Kawaguchi Y, Miyata T, Kobayashi T, Sugiyama M, Onoue T, Yasuda Y, Hagiwara D, Iwama S, Tomigahara Y, Kimura T, Arima H. Generation and purification of ACTH-secreting hPSC-derived pituitary cells for effective transplantation. Stem Cell Reports. 2023 Aug 8;18(8):1657-1671. doi: 10.1016/j.stemcr.2023.05.002. Epub 2023 Jun 8. PMID: 37295423
- Sugimoto A, Watanabe T, Matsuoka K, Okuno Y, Yanagi Y, Narita Y, Mabuchi S, Nobusue H, Sugihara E, Hirayama M, Ide T, Onouchi T, Sato Y, Kanda T, Saya H, Iwatani Y, Kimura H, Murata T. Growth Transformation of B cells by Epstein-Barr Virus Requires IMPDH2 Induction and Nucleolar Hypertrophy. Microbiol Spectr. 2023 Aug 17;11(4):e0044023. doi: 10.1128/spectrum.00440-23. Epub 2023 Jul 6. PMID: 37409959
- Uddin MK, Watanabe T, Arata M, Sato Y, Kimura H, Murata T. Epstein-Barr virus BBLF1 mediates secretory vesicle transport to facilitate mature virion release. J Virol. 2023 May 17:e0043723. doi: 10.1128/jvi.00437-23. Epub 2023 May 17. PMID: 37195206
- Hirai Y, Asada H, Hamada T, Kawada JI, Kimura H, Arai A, Ohshima K, Ohga S, Iwatsuki K. Diagnostic and disease severity determination criteria for hydroa vacciniforme lymphoproliferative disorders and severe mosquito bite allergy. J Dermatol. 2023 Jul;50(7):e198-e205. doi: 10.1111/1346-8138.16842. Epub 2023 May 30. PMID: 37249004.
- Sawa M, Murase C, Yamada N, Fukaura R, Tetsuka N, Sato Y, Takeichi T, Akiyama M. Giant condyloma of Buschke-Löwenstein in a Netherton syndrome patient, successfully treated with cryotherapy and intravenous immunoglobulin. J Dermatol. 2023 Apr 5. doi: 10.1111/1346-8138.16798. Online ahead of print. PMID: 37017444
- Nakaya Y, Koh H, Harada N, Okamura H, Misugi T, Suekane T, Tachibana D, Kimura H, Hino M, Nakamae H. Salvage HLA-haploidentical hematopoietic cell transplantation with post-transplant cyclophosphamide for graft failure in a patient with chronic active Epstein-Barr virus infection. Exp Clin Transplant. 2023 Feb;21(2):184-188. doi: 10.6002/ect.2022.0322. PMID: 36919727
- Murata T, Iwahori S, Okuno Y, Nishitsuji H, Yanagi Y, Watashi K, Wakita T, Kimura H, Shimotohno K. N6-methyladenosine modification of hepatitis B virus RNA in the coding region of HBx. Int J Mol Sci. 2023 Jan 23;24(3):2265. doi: 10.3390/ijms24032265. PMID: 36768585
- Kimura H. The 100th anniversary of the Nagoya Journal of Medical Science: a message from the Dean. Nagoya J. Med. Sci. 85. 5–6, 2023 doi:10.18999/nagjms.85.1.5. PMID: 36923615
2022
- Ding W, Wang C, Narita Y, Wang H, Leong MML, Huang A, Liao Y, Liu X, Okuno Y, Kimura H, Gewurz B, Teng M, Jin S, Sato Y, Zhao B. The Epstein-Barr Virus Enhancer Interaction Landscapes in Virus-Associated Cancer Cell Lines. J Virol. 2022 Sep 12:e0073922. doi: 10.1128/jvi.00739-22. Online ahead of print. PMID: 36094314
- Hara Y, Watanabe T, Yoshida M, Masud HMAA, Kato H, Kondo T, Suzuki R, Kurose S, Uddin MK, Arata M, Miyagi S, Yanagi Y, Sato Y, Kimura H, Murata T. Comprehensive Analyses of Intraviral Epstein-Barr Virus Protein-Protein Interactions Hint Central Role of BLRF2 in the Tegument Network. J Virol. 2022 Jul 27;96(14):e0051822. doi: 10.1128/jvi.00518-22. Epub 2022 Jul 11. PMID: 35862711
- Kimura H, de Leval L, Cai Q, Kim WS. EBV-associated NK and T-cell lymphoid neoplasms. Curr Opin Oncol. 2022 Sep 1;34(5):422-431. doi: 10.1097/CCO.0000000000000889. Epub 2022 Jul 27. PMID: 35900729
- Alaggio R, Amador C, Anagnostopoulos I, Attygalle AD, Araujo IBO, Berti E, Bhagat G, Borges AM, Boyer D, Calaminici M, Chadburn A, Chan JKC, Cheuk W, Chng WJ, Choi JK, Chuang SS, Coupland SE, Czader M, Dave SS, )de Jong D, Du MQ, Elenitoba-Johnson KS, Ferry J, Geyer J, Gratzinger D, Guitart J, Gujral S, Harris M, Harrison CJ, Hartmann S, Hochhaus A, Jansen PM, Karube K, Kempf W, Khoury J, Kimura H, Klapper W, Kovach AE, Kumar S, Lazar AJ, Lazzi S, Leoncini L, Leung N, Leventaki V, Li XQ, Lim MS, Liu WP, Louissaint A Jr, Marcogliese A, Medeiros LJ, Michal M, Miranda RN, Mitteldorf C, Montes-Moreno S, Morice W, Nardi V, Naresh KN, Natkunam Y, Ng SB, Oschlies I, Ott G, Parrens M, Pulitzer M, Rajkumar SV, Rawstron AC, Rech K, Rosenwald A, Said J, Sarkozy C, Sayed S, Saygin C, Schuh A, Sewell W, Siebert R, Sohani AR, Tooze R, Traverse-Glehen A, Vega F, Vergier B, Wechalekar AD, Wood B, Xerri L, Xiao W. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia. 2022 Jul;36(7):1720-1748. doi: 10.1038/s41375-022-01620-2. Epub 2022 Jun 22. PMID: 35732829
- Suzuki T, Sato Y, Okuno Y, Goshima F, Mikami T, Umeda M, Murata T, Miyake Y, Watanabe T, Watashi K, Wakita T, Kitagawa H, Kimura H. Genome-wide CRISPR screen for HSV-1 host factors reveals PAPSS1 contributes to heparan sulfate synthesis. Commun Biol. 2022 Jul 19;5(1):694. doi: 10.1038/s42003-022-03581-9. PMID: 35854076 プレスリリース/解説
- Narita S, Unno K, Kato K, Okuno Y, Sato Y, Tsumura Y, Fujikawa Y, Shimizu Y, Hayashida R, Kondo K, Shibata R, Murohara T. Direct reprogramming of adult adipose-derived regenerative cells toward cardiomyocytes using six transcriptional factors. iScience. 2022 Jun 24;25(7):104651. doi: 10.1016/j.isci.2022.104651. eCollection 2022 Jul 15. PMID: 35811849
- Sato Y, Yaguchi M, Okuno Y, Ishimaru H, Sagou K, Ozaki S, Suzuki T, Inagaki T, Umeda M, Watanabe T, Fujimuro M, Murata T, Kimura H. Epstein-Barr virus tegument protein BGLF2 in exosomes released from virus-producing cells facilitates de novo infection. Cell Commun Signal. 2022 Jun 21;20(1):95. doi: 10.1186/s12964-022-00902-7. PMID: 35729616
- Yanagi Y, Watanabe T, Hara Y, Sato Y, Miyake Y, Kimura H, Murata T. EBV exploits RNA m6A modification for cell survival and efficient progeny virus production in lytic cycle. Front Microbiol. 2022 Jun 15;13:870816. doi: 10.3389/fmicb.2022.870816. eCollection 2022. PMID: 35783391
- Nishikubo M, Hiramoto N, Yamashita D, Imoto H, Sato Y, Okuno Y, Haga H, Nannya Y, Ogawa S, Kimura H, Ishikawa T. Elderly-onset systemic Epstein Barr virus-positive T cell lymphoma of childhood: a case report. Pathol Int. 2022 Jul;72(7):376-378. doi: 10.1111/pin.13231. Epub 2022 May 24. PMID: 35611496.
- Kondo S, Okuno Y, Murata T, Dochi H, Wakisaka N, Mizokami H, Moriyama-Kita M, Kobayashi E, Kano, M Komori T, Hirai N, Ueno T, Nakanishi Y, Endo K, Sugimoto H, Kimura H, Yoshizaki T. EBV genome variations enhance clinicopathological features of nasopharyngeal carcinoma in a non-endemic region. Cancer Sci. 2022 Jul;113(7):2446-2456. doi: 10.1111/cas.15381. Epub 2022 May 24. PMID: 35485636
- Wang L, Moreira EA, Kempf G, Miyake Y, Oliveira Esteves BI, Fahmi A, Schaefer JV, Dreier B, Yamauchi Y, Alves MP, Plückthun A, Matthias P. Disrupting the HDAC6-ubiquitin interaction impairs infection by influenza and Zika virus and cellular stress pathways. Cell Rep. 2022 Apr 26;39(4):110736. doi: 10.1016/j.celrep.2022.110736. PMID: 35476995
- Yanagi Y, Hara Y, Mabuchi S, Watanabe T, Sato Y, Kimura H, Murata T. PD-L1 Upregulation by Lytic Induction of Epstein-Barr virus. Virology 2022 2022 Mar;568:31-40. doi: 10.1016/j.virol.2022.01.006. PMID: 35093708
- Fujimoto KJ, Hobbs DCF, Umeda M, Nagata A, Yamaguchi R, Sato Y, Sato S, Ohmatsu K, Ooi T, Yanai T, Kimura H, Murata T. In silico Analysis and Synthesis of Nafamostat Derivatives and Evaluation of Their Anti-SARS-CoV-2 Activity. Viruses 2022 Feb 14;14(2):389. doi: 10.3390/v14020389. PMID: 35215982
2021
- Murata T, Sugimoto A, Inagaki T, Watanabe T, Sato Y, Kimura H. Molecular Basis of Epstein-Barr Virus Latency Establishment and Lytic Reactivation. Viruses 2021 Nov 23;13(12):2344. doi: 10.3390/v13122344. PMID: 34960613
- Miyagi S, Watanabe T, Hara Y, Arata M, Uddin MMK, Mantoku K, Sago K, Yusuke Yanagi Y, Suzuki T, Masud HMAA , Kawada JI, Nakamura S, Miyake Y, Sato Y, Murata T, Kimura H. A STING inhibitor suppresses EBV-induced B cell transformation and lymphomagenesis. Cancer Sci 2021 Oct 5. doi: 10.1111/cas.15152. Online ahead of print. PMID: 34609775.
- Oka K, Morioka H, Eguchi M, Sato Y, Tetsuka N, Iguchi M, Kanematsu T, Fukano H, Hoshino Y, Kiyoi H, Yagi T. Bursitis, Bacteremia, and Disseminated Infection of Mycobacteroides (Mycobacterium) abscessus subsp. massiliense. Intern Med. 2021 Sep 15;60(18):3041-3045. doi: 10.2169/internalmedicine.6189-20. Epub 2021 Mar 29. PMID: 33775997
- Kimura H, Okuno Y, Sato Y, Watanabe T, Murata T. Deletion of Viral microRNAs in the Oncogenesis of Epstein-Barr Virus-Associated Lymphoma. Front Microbiol. 2021 Jul 8;12:667968. doi: 10.3389/fmicb.2021.667968. eCollection 2021. PMID: 34305835
- Yanagi Y, Okuno Y, Narita Y, Masud HMA, Watanabe T, Sato Y, Kanda T, Kimura H, Murata T. RNAseq analysis identifies involvement of EBNA2 in PD-L1 induction during Epstein-Barr virus infection of primary B cells. Virology. 2021 Feb 21;557:44-54. doi: 10.1016/j.virol.2021.02.004. Online ahead of print. PMID: 33639481
- Mabuchi S, Hijioka F, Watanabe T, Yanagi Y, Okuno Y, Masud HMA, Sato Y, Murata T, Kimura H. Role of Epstein-Barr virus C promoter deletion found in diffuse large B cell lymphoma. Cancers (Basel). 2021 Feb 1;13(3):561. doi: 10.3390/cancers13030561. PMID: 33535665
- Inagaki T, Sato Y, Ito, Takaki M, Okuno Y, Yaguchi M, Masud HMA, Watanabe T, Sato K, Iwami S, Murata T, Kimura H. Direct evidence of abortive lytic infection-mediated establishment of Epstein-Barr virus latency during B-cell infection. Front Microbiol., 2021 Jan 21;11:575255. doi: 10.3389/fmicb.2020.575255. eCollection 2020. PMID: 33613459
2020
- Takano G, Esaki S, Goshima F, Enomoto A, Hatano Y, Ozaki H, Watanabe T, Sato Y, Kawakita D, Murakami S, Murata T, Nishiyama Y, Iwasaki S, Kimura H. Oncolytic activity of naturally attenuated herpes-simplex virus HF10 against an immunocompetent model of oral carcinoma. Molecular Therapy – Oncolytics, 2020 Dec 19;20:220-227. doi: 10.1016/j.omto.2020.12.007. eCollection 2021 Mar 26. PMID: 33665360
- Sato Y, Iguchi M, Kato Y, Morioka H, Hirabayashi A, Tetsuka N, Tomita Y, Kato D, Yamada K, Kimura H, Yagi T. Number of concomitant drugs with thrombocytopenic adverse effect and the extent of resolution of inflammatory response are risk factors for thrombocytopenia in patients treated with Linezolid for more than 14 days. Nagoya J Med Sci 2020 Aug;82(3):407-414. doi: 10.18999/nagjms.82.3.407. PMID: 33132425
- Esaki E, Goshima F, Ozaki H, Takano G, Hatano Y, Kawakita D, Ijichi K, Watanabe T, Sato Y, Murata T, Iwata H, Shibamoto Y, Murakami S, Nishiyama Y, Kimura H. Oncolytic activity of HF10 in head and neck squamous cell carcinomas. Cancer Gene Ther 2020 Aug;27(7-8):585-598. doi: 10.1038/s41417-019-0129-3. PMID: 31477804
- Yonese I, Sakashita C, Imadome KI, Kobayashi T, Yamamoto M, Sawada A, Ito Y, Fukuhara N, Hirose A, Takeda Y, Makita M, Endo T, Kimura SI, Ishimura M, Miura O, Ohga S, Kimura H, Fujiwara S, Arai A. Nationwide survey of systemic chronic active EBV infection in Japan in accordance with the new WHO classification. Blood Adv. 2020 Jul 14;4(13):2918-2926. doi: 10.1182/bloodadvances.2020001451. PMID: 32598475
- Shibata A, Ishiguro Y, Makita S, Yamaga Y, Kimura H, Akiyama M. A systemic form chronic active Epstein-Barr virus infection diagnosed from erythema nodosum-like skin lesions. Eur J Dermatol. 2020 Jun 1;30(3):314-316. doi: 10.1684/ejd.2020.3781. PMID: 32666933
- Murata T, Okuno Y, Sato Y, Watanabe T, Kimura H. Oncogenesis of CAEBV Revealed: Intragenic Deletions in the Viral Genome and Leaky Expression of Lytic Genes\\\". Rev Med Virol. 2020 Mar;30(2):e2095. doi: 10.1002/rmv.2095. PMID: 31845495
- Cohen JI, Iwatsuki K, Ko YH, Kimura H, Manoli I, Ohshima K, Pittaluga S, Quintanilla-Fend L, Jaffe ES. Epstein-Barr virus NK and T cell lymphoproliferative disease: report of a 2018 international meeting. Lymphoma Leuk 2020 Apr;61(4):808-819. doi: 10.1080/10428194.2019.1699080. PMID: 31833428
- Watanabe T, Sato Y, Masud HMA, Takayama M, Matsuda H, Hara Y, Yanagi Y, Yoshida M, Goshima F, Murata T, Kimura H. Antitumor activity of CDK inhibitor alsterpaullone in Epstein-Barr virus-associated lymphoproliferative disorders. Cancer Sci 2020 Jan;111(1):279-287. doi: 10.1111/cas.14241. PMID: 31743514
2019
- Iemura T, Kondo T, Hishizawa M, Yamashita K, Kimura H, Takaori-Kondo A. NK-cell post-transplant lymphoproliferative disease with chronic active Epstein-Barr virus infection-like clinical findings. Int J Infect Dis. 2019 Nov;88:31-33. doi: 10.1016/j.ijid.2019.07.039. Epub 2019 Aug 6. PMID: 31398454
- Fujiwara S, Kimura H. Editorial: Epstein-Barr virus-associated T/NK-cell lymphoproliferative diseases. Frontiers Pediatr. 2019 Jul 10;7:285. doi: 10.3389/fped.2019.00285. PMID: 31355168
- Kawada JI, Kamiya Y, Sawada A, Iwatsuki K, Izutsu K, Torii Y, Kimura H, Ito Y. Viral DNA loads in various blood components of patients with Epstein–Barr virus-positive-T/NK cell lymphoproliferative diseases. J Infect Dis. 2019 Sep 13;220(8):1307-1311. doi: 10.1093/infdis/jiz315. PMID: 31240305
- Masud HMA, Watanabe T, Sato Y, Goshima F, Kimura H, Murata T. The BOLF1 Gene is Necessary for Effective Epstein-Barr Viral Infectivity. Virology. 2019 May;531:114-125. doi: 10.1016/j.virol.2019.02.015. PMID: 30856483
- Miyake Y, Keusch JJ, Decamps L, Ho-Xuan H, Iketani S, Gut H, Kutay U, Helenius A, Yamauchi Y. Influenza virus uses transportin 1 for vRNP debundling during cell entry. Nat Microbiol. 2019 Apr;4(4):578-586. doi: 10.1038/s41564-018-0332-2 PMID: 30692667
- Sato Y, Watanabe T, Suzuki C, Abe Y, Masud HMA, Inagaki T, Yoshida M, Suzuki T, Goshima F, Adachi J, Tomonaga T, Murata T, Kimura H. S-like phase CDKs stabilize the Epstein-Barr virus BDLF4 protein to temporally control late gene transcription. J Virol. 2019 Apr 3;93(8). pii: e01707-18. doi: 10.1128/JVI.01707-18. PMID: 30700607
- Yanagi Y, Masud HMA, Watanabe T, Sato Y, Goshima F, Kimura H, Murata T. Initial Characterization of the Epstein-Barr Virus BSRF1 Gene Product. Viruses. 2019 Mar 21;11(3). pii: E285. doi: 10.3390/v11030285. PMID: 30901892
- Okuno Y, Murata Y, Sato Y, Muramatsu H, YIto Y, Watanabe T, Okuno T, Murakami N, Yoshida K, Sawada A, Inoue M, Kawa K, Seto M, Ohshima K, Shiraishi Y, Chiba K, Tanaka H, Miyano S, Narita Y, Yoshida M, Goshima F, Kawada JI, Nishida T, Kiyoi H, Kato S, Nakamura S, Morishima S, Yoshikawa T, Fujiwara S, Shimizu N, Isobe Y, Noguchi M, Kikuta1 A, Iwatsuki K, Takahashi Y, Kojima S, Ogawa S, Kimura H. Defective Epstein-Barr virus (EBV) in chronic active EBV infection and EBV-related hematological malignancy. Nat Microbiol. 2019 Mar;4(3):404-413. doi: 10.1038/s41564-018-0334-0. PMID: 30664667
- Kimura H, Kwong YL. EBV Viral Loads in Diagnosis, Monitoring, and Response Assessment. Frontiers Oncol. 2019 Feb 12;9:62. doi: 10.3389/fonc.2019.00062. PMID: 30809508
- Kimura H, Fujiwara S. Overview of EBV-associated T/NK-cell lymphoproliferative diseases. Frontiers Pediatr. 2019 Jan 4;6:417. doi: 10.3389/fped.2018.00417. PMID: 30662890
2018
- Ichikawa T, Okuno Y, Sato Y, Goshima F, Yoshiyama H, Kanda T, Kimura H, Murata T. Regulation of EBV Lifecycle and Cell Proliferation by Histone H3K27 Methyltransferase, EZH2, in Akata Cells. mSphere. 2018 Nov 28;3(6). pii: e00478-18. doi: 10.1128/mSphere.00478-18. PMID: 3048715
- Kimura H. JAK inhibitors for refractory lymphoma. Oncotarget 2018, Vol. 9, (No. 68), pp: 32883-32884 doi: 10.18632/oncotarget.26054
- Murata T. Encyclopedia of EBV-Encoded Lytic Genes: An Update. Adv Exp Med Biol. 2018;1045:395-412. doi: 10.1007/978-981-10-7230-7_18. PMID: 29896677
- Watanabe D, Goshima F. Oncolytic Virotherapy by HSV. Adv Exp Med Biol. 2018;1045:63-84. doi: 10.1007/978-981-10-7230-7_4. PMID: 29896663
- Kimura H. EBV in T-/NK-Cell Tumorigenesis. Adv Exp Med Biol. 2018;1045:459-475. doi: 10.1007/978-981-10-7230-7_21. PMID: 29896680
- Konishi N, Narita Y, Hijioka F, Masud HMAA, Sato Y, Kimura H, Murata M. BGLF2 Increases Infectivity of Epstein-Barr virus by Activating AP-1 upon de novo Infection. mSphere 2018 Apr 25;3(2). pii: e00138-18. doi: 10.1128/mSphere.00138-18. PMID: 29695622
- Miyake Y, Matthias P, Yamauchi Y. Purification of Unanchored Polyubiquitin Chains from Influenza Virions. Methods Mol Biol. 2018;1836:329-342. doi: 10.1007/978-1-4939-8678-1_16. PMID: 30151581
- Matsuzawa T, Nakamura Y, Ogawa Y, Ishimaru K, Goshima F, Shimada S, Nakao A, Kawamura T. Differential Day-Night Outcome to HSV-2 Cutaneous Infection. J Invest Dermatol. 2018 Jan;138(1):233-236. doi: 10.1016/j.jid.2017.07.838. PMID: 28842321
- Kawamoto K, Miyoshi H, Suzuki T, Kozai Y, Kato K, Miyahara M, Yujiri T, Oishi N, Choi I, Fujimaki K, Muta T, Kume M, Moriguchi S, Tamura S, Kato T, Tagawa H, Makiyama J, Kanisawa Y, Sasaki Y, Kurita D, Yamada K, Shimono J, Sone H, Takizawa J, Seto M, Kimura H, Ohshima K. A distinct subtype of Epstein Barr virus positive T/NK-cell lymphoproliferative disorder: Adult patients with chronic active Epstein Barr virus infection-like features. Haematologica. 2018 Jun;103(6):1018-1028. doi: 10.3324/haematol.2017.174177. PMID: 29242302
- Kawada JI, Ando S, Torii Y, Ito Y, Kimura H. Antitumor effects of duvelisib on Epstein-Barr virus-associated lymphoma cells. Cancer Med 2018 Apr;7(4):1275-1284. doi: 10.1002/cam4. PMID: 29522278
2017
- Kimura H, Cohen JI. Chronic Active Epstein-Barr Virus Disease. Front Immunol 8:1867, 2017 doi: 10.3389/fimmu.2017.01867
- Yoshida M, Murata T, Ashio K, Narita Y, Watanabe T, Masud HMAA, Sato Y, Goshima F, Kimura H. Characterization of a Suppressive Cis-acting Element in the Epstein-Barr virus LMP1 Promoter. Front Microbiol 8: 2302, 2017
- Masud HMA, Watanabe T, Yoshida M, Sato Y, Goshima F, Kimura H, Murata T. Epstein-Barr Virus BKRF4 Gene Product Is Required for Efficient Progeny Production. J Virol doi: 10.1128/JVI.00975-17. [Epub ahead of print]
- Quintanilla-Martinez L, Ko YH, Kimura H, Jaffe ES. EBV-positive T-cell and NK-cell lymphoproliferative diseases of childhood: WHO Classification of Tumours of Haematopoietic and Lymphoid Tissues. Swerdlow SH, Campo E, Harris NL, Jaffe ES, Pileri SA, Stein H, Thiele J eds. Revised 4th ed, IARC Press, Lyon, p355-62, 2017
- Tanaka R, Goshima F, Esaki S, Sato Y, Murata T, Nishiyama Y, Watanabe D, Kimura H. The efficacy of combination therapy with oncolytic herpes simplex virus HF10 and dacarbazine in a mouse melanoma model. Am J Cancer Res 7:1693-1703, 2017
- Yoshida M, Watanabe T, Narita Y, Sato Y, Goshima F, Kimura H, Murata T. The Epstein-Barr Virus BRRF1 Gene is Dispensable for Viral Replication in HEK293 cells and Transformation. Sci Rep 7:6044, 2017
- Sato Y, Ochiai S, Murata T, Kanda T, Goshima F, Kimura H. Elimination of LMP1-expressing cells from a monolayer of gastric cancer AGS cells. Oncotarget 8:39345-39355, 2017
- Washio K, Oka T, Abdalkader L, Muraoka M, Shimada A, Oda M, Sato H, Takata K, Kagami Y, Shimizu N, Seto M, Nakamura S, Kimura H, Yoshino T, Tsukahara H. Gene expression analysis of hypersensitivity to mosquito bite, chronic active EBV infection and NK/T-lymphoma/leukemia. Leuk Lymphoma 58: 2683-2694, 2017
- Watanabe T, Sakaida K, Yoshida M, Masud HMA, Sato Y, Goshima F, Kimura H, Murata T. The C-terminus of Epstein-Barr virus BRRF2 is required for its proper localization and efficient virus production. Front Microbiol 8: 125, 2017
- Torii Y, Kawada JI, Murata T, Yoshiyama H, Kimura H, Ito Y. Epstein-Barr virus infection-induced inflammasome activation in human monocytes. PLoS One 12(4):e0175053, 2017
2016
- Murata T, Noda C, Narita Y, Watanabe T, Yoshida M, Ashio K, Sato Y, Goshima F, Kanda T, Yoshiyama H, Tsurumi T, Kimura H. Induction of Epstein-Barr Virus Oncoprotein Latent Membrane Protein 1 (LMP1) by Transcription Factors Activating Protein 2 (AP-2) and Early B Cell Factor (EBF). J Virol 90:3873-89, 2016
- Ando S, Kawada JI, Watanabe T, Suzuki M, Sato Y, Torii Y, Asai M, Goshima F, Murata T, Shimizu N, Ito Y, Kimura H. Tofacitinib induces G1 cell-cycle arrest and inhibits tumor growth in Epstein-Barr virus-associated T and natural killer cell lymphoma cells. Oncotarget 7:76793-76805, 2016
- Kawano Y, Kawada JI, Kamiya Y, Suzuki M, Torii Y, Kimura H, Ito Y. Analysis of circulating human and viral microRNAs in patients with congenital cytomegalovirus infection. J Perinatol 36: 1101-1105, 2016
- Aoki R, Kawamura T, Goshima F, Ogawa Y, Nakae S, Moriishi K, Nakao A, Shimada S. The Alarmin IL-33 Derived from HSV-2-Infected Keratinocytes Triggers Mast Cell-Mediated Antiviral Innate Immunity. J Invest Dermatol 136(6):1290-2, 2016.
- Kawamura Y, Miura H, Matsumoto Y, Uchida H, Kudo K, Hata T, Ito Y, Kimura H, Yoshikawa T. A case of Epstein-Barr virus–associated hemophagocytic lymphohistiocytosis with severe cardiac complications. BMC Pediatrics 16:172, 2016
- Ikumi K, Ando T, Katano H, Katsuno M, Sakai Y, Yoshida M, Saida T, Kimura H, Sobue G. HSV-2-related hemophagocytic lymphohistiocytosis in a fingolimod-treated MS patient. Neurol Neuroimmunol Neuroinflamm 3(4):e247, 2016
- Shimomura M, Morishita H, Meguro T, Seto S, Kimura M, Hamazaki M, Hashimoto A, Sugiyama Y, Kimura H. A case of CAEBV showing features of granulomatosis with polyangiitis. Pediatr Int 58:639-42, 2016
- Ito Y, Suzuki M, Kawada J, Kimura H. Diagnostic values for the viral load in peripheral blood mononuclear cells of patients with chronic active Epstein-Barr virus disease. J Infect Chemother 22:268-271, 2016
2015
- Watanabe T, Narita Y, Yoshida M, Sato Y, Goshima F, Kimura H, Murata T. Epstein-Barr virus BDLF4 gene is required for efficient expression of viral late lytic genes. J Virol 89(19):10120-4
- Narita Y, Sugimoto A, Kawashima D, Watanabe T, Kanda T, Kimura H, Tsurumi T, Murata T. A herpesvirus specific motif of Epstein-Barr virus DNA polymerase is required for the efficient lytic genome synthesis. Sci Rep 5:11767, 2015
- Watanabe T, Tsuruoka M, Narita Y, Katsuya R, Goshima F, Kimura H, Murata T. The Epstein-Barr virus BRRF2 gene product is involved in viral progeny production. Virology 484:33-40, 2015
- Watanabe T, Fuse K, Takano T, Narita Y, Goshima F, Kimura H, Murata T. Roles of Epstein-Barr virus BGLF3.5 Gene and Two Upstream Open Reading Frames in Lytic Viral Replication in HEK293 Cells. Virology 483: 44–53, 2015
- Suzuki M, Takeda T, Nakagawa H, Iwata S, Watanabe T, Siddiquey MN, Goshima F, Murata T, Kawada JI, Ito Y, Kojima S, Kimura H. The heat shock protein 90 inhibitor BIIB021 suppresses the growth of T and natural killer cell lymphomas.Front Microbiol 6:280, 2015
- Nagata K, Nakayama Y, Higaki K, Ochi M, Kanai K, Matsushita M, Kuwamoto S, Kato M, Murakami I, Iwasaki T, Nanba E, Kimura H, Hayashi K. Reactivation of persistent Epstein—Barr virus (EBV) causes secretion of thyrotropin receptor antibodies (TRAbs) in EBVinfected B lymphocytes with TRAbs on their surface. Autoimmunity 11:1-8, 2015
- Morishima S, Nakamura S, Yamamoto K, Miyauchi H, Kagami Y, Kinoshita T, Onoda H, Yatabe Y, Ito M, Miyamura K, Nagai H, Moritani S, Sugiura I, Tsushita K, Mihara H, Ohbayashi K, Iba S, Emi N, Okamoto M, Iwata S, Kimura H, Kuzushima K, Morishima Y. Increased T-cell responses to EBV with high viral load in patients with EBV-positive diffuse large B-cell lymphoma.Leukemia & Lymphoma 56:1072-8, 2015
- Coleman CB, Wohlford EM, Smith NA, King CA, Ritchie JA, Baresel PC, Kimura H, Rochford R. Epstein-Barr virus Type 2 latently infects T-cells inducing an atypical activation characterized by expression of lymphotactic cytokines. J Virol 89:2301-12, 2015
- Kawada J, Torii Y, Kawano Y, Suzuki M, Kamiya Y, Kotani T, Kikkawa F, Kimura H, Ito Y. Viral load in children with congenital cytomegalovirus infection identified on newborn hearing screening. J Clin Virol 65:41-5, 2015
- Kawano Y, Suzuki M, Kawada JI, Kimura H, Kamei H, Ohnishi Y, Ono Y, Uchida H, Ogura Y, Ito Y. Effectiveness and safety of immunization with live-attenuated and inactivated vaccines for pediatric liver transplantation recipients. Vaccine 33:1440-5, 2015
2014
- Kanazawa T, Hiramatsu Y, Iwata S, Siddiquey MN, Sato Y, Suzuki M, Ito Y, Goshima F, Murata T, Kimura H. Anti-CCR4 monoclonal antibody mogamulizumab for the treatment of EBV-associated T- and NK-cell lymphoproliferative diseases. Clin Cancer Res 20:5075-84, 2014
- Kawada JI, Ito Y, Iwata S, Suzuki M, Kawano Y, Kanazawa T, Siddiquey MN, Kimura H. mTOR inhibitors induce cell cycle arrest and inhibit tumor growth in Epstein-Barr virus-associated T and natural killer cell lymphoma cells. Clin Cancer Res 20:5412-22, 2014
- Murata T, Sato Y, Kimura H. Modes of infection and oncogenesis by the Epstein-Barr virus. Rev Med Virol 24: 242–253, 2014
- Murata T. Regulation of Epstein-Barr virus reactivation from latency. Microbiol Immunol 58(6):307-17, 2014
- Fujiwara S, Kimura H, Imadome KI, Arai A, Kodama E, Morio T, Shimizu N, Wakiguchi H. Current Studies on Chronic Active Epstein-Barr virus Infection in Japan. Pediatr Int 56, 159–166, 2014
- Ito T, Kawazu H, Murata T, Iwata S, Arakawa S, Sato Y, Kuzushima K, Goshima F, Kimura H. Role of latent membrane protein 1 (LMP1) in chronic active Epstein-Barr virus infection (CAEBV)-derived T/NK cell proliferation. Cancer Med 3: 787-795, 2014
- Siddiquey MN, Nakagawa H, Iwata S, Kanazawa T, Suzuki M, Imadome KI, Fujiwara S, Goshima F, Murata T, Kimura H. Anti-tumor effects of suberoylanilide hydroxamic acid on Epstein-Barr virus-associated T- and natural killer- cell lymphoma. Cancer Sci 105:713-722, 2014
- Murata T, Tsurumi T. Switching of EBV cycles between latent and lytic states. Rev Med Virol 24:142-53, 2014
- Kimura H, Karube K, Ito Y, Hirano K, Suzuki M, Iwata S, Seto M. Rare occurrence of JAK3 mutations in NK cell neoplasms in Japan. Leukemia & Lymphoma 55:962-3, 2014
- Goshima F, Esaki S, Luo C, Kamakura M, Kimura H, Nishiyama Y. Oncolytic viral therapy with a combination of HF10, a herpes simplex virus type 1 variant, and granulocyte–macrophage colony-stimulating factor for murine ovarian cancer. Int J Cancer 134:2865-77, 2014
- Nagata K, Higaki K, Nakayama Y, Miyauchi H, Kiritani Y, Kanai K, Matsushita M, Iwasaki T, Sugihara H, Kuwamoto S, Kato M, Murakami I, Nanba E, Kimura H, Hayashi K. Presence of Epstein-Barr virus-infected B lymphocytes with thyrotropin receptor antibodies on their surface in Graves' disease patients and in healthy individuals. Autoimmunity 47:193-200, 2014
2013
- Goshima F, Esaki S, Luo C, Kamakura M, Kimura H, Nishiyama Y.Oncolytic viral therapy with a combination of HF10, a herpes simplex virus type 1 variant, and granulocyte–macrophage colony-stimulating factor for murine ovarian cancer. Int J Cancer in press
- Kimura H, Karube K, Ito Y, Hirano K, Suzuki M, Iwata S, Seto M. Rare occurrence of JAK3 mutations in NK cell neoplasms in Japan. Leukemia & Lymphoma in press
- Kato S, Miyata T, Takata K, Shimada S, Ito Y, Tomita A, Elsayed AA, Takahashi E, Asano N, Kinoshita T, Kimura H, Nakamura S. Epstein-Barr virus-positive cytotoxic T-cell lymphoma followed by chronic active Epstein-Barr virus infection-associated T/NK-cell lymphoproliferative disorder: a case report. Hum Pathol in press
- Hayashi K, Ishigami M, Ishizu Y, Kuzuya T, Honda T, Itoh A, Hirooka Y, Ishikawa T, Nakano I, Ito Y, Kimura H, Katano Y, Goto H. A pediatric case of hepatitis B virus subgenotype A2 in Japan. Clin J Gastroenterol in press
- Kimura H, Kawda J, Ito Y. Epstein-Barr virus-associated lymphoid malignancies: the expanding spectrum of hematopoietic neoplasms. Nagoya J Med Sci 75: 169-79, 2013
- Ito Y, Suzuki R, Torii Y, Kawa K, Kikuta A, Kojima S, Kimura H. HLA-A*26 and HLA-B*52 are associated with a risk of developing EBV-associated T/NK lymphoproliferative disease. Blood e-Letter ID: bloodjournal_el; 8085, 2013
- Suzuki M, Torii Y, Kawada J, Kimura H, Kamei H, Onishi Y, Kaneko K, Ando H, Kiuchi T, Ito Y. Immunogenicity of inactivated seasonal influenza vaccine in adult and pediatric liver transplant recipients over two seasons. Microbiol Immunol 57:715-22.2013
- Kawano Y, Iwata S, Kawada J, Gotoh K, Suzuki M, Torii Y, Kojima S, Kimura H, Ito Y.Plasma viral MicroRNA profiles reveal potential biomarkers for chronic active Epstein-Barr virus infection.J Infect Dis 208: 771-9, 2013
- Sugimoto A, Sato Y, Kanda T, Murata T, Narita Y, Kawashima D, Kimura H, Tsurumi T.Different Distributions of Epstein-Barr virus early and late gene transcripts within viral replication compartments.J Virol 87: 6693-9, 2013
- Ito Y, Kimura H, Torii Y, Hayakawa M, Tanaka T, Tajiri H, Yoto Y, Tanaka-Taya K, Kanegane H, Nariai A, Sakata H, Tsutsumi H, Oda M, Yokota S, Morishima T, Moriuchi H. Risk factors for poor outcome in congenital cytomegalovirus infection and neonatal herpes on the basis of a nationwide survey in Japan.Pediatr Int 55, 566–571, 2013
- Trii Y, Kimura H, Ito Y, Hayakawa M, Tanaka T, Tajiri H, Yoto Y, Tanaka-Taya K, Kanegane H, Nariai A, Sakata H, Tsutsumi H, Oda M, Yokota S, Morishima T, Moriuchi H.Clinico-epidemiological states of mother-to-child infections: a nationwide survey in Japan. Pediatr Infect Dis J 32:699-701, 2013
- Murata T, Iwata S, Siddiquey NA, Kanazawa T, Goshima F, Kimura H, Tsurumi T.Heat shock protein 90 inhibitors repress latent membrane protein 1 (LMP1) expression and proliferation of Epstein-Barr virus-positive natural killer cell lymphoma.PLoS One 8:e63566, 2013
- Narita Y, Murata T, Ryo A, Kawashima D, Sugimoto A, Kanda T, Kimura H, Tsurumi T.Pin1 interacts with the Epstein-Barr virus DNA polymerase catalytic subunit and regulates viral DNA replication.J Virol 87:2120-7, 2013
- Esaki S, Goshima F, Kimura H, Murakami S, Nishiyama Y.Enhanced antitumoral activitiy of oncolytic herpes simplex virus with gemcitabine using colorectal tumor models.Int J Cancer 132:1592-601, 2013
- Isobe Y, Hamano Y, Yoshinori Ito Y, Kimura H, Tsukada N, Sugimoto K, Komatsu N. A monoclonal expansion of Epstein–Barr virus-infected natural killer cells after allogeneic peripheral blood stem cell transplantation.J Clin Virol 56:150-2, 2013
- Kawada J, Ito Y, Torii Y, Kimura H, Iwata N.Remission of Juvenile Idiopathic Arthritis with Primary Epstein-Barr Virus Infection. Rheumatol 52:956-8 2013
- Ohta R, Imai M, Kawada J, Kimura H, Ito Y.Interleukin-17A-producing T lymphocytes in chronic active Epstein-Barr virus infection.Microbiol Immunol 57:139-44, 2013
- Hiraiwa-Sofue A, Ito Y, Ohta R, Kimura H, Okumura A.Human herpesvirus 6-associated encephalopathy in a child with Dravet syndrome. Neuropediatrics 44:155-8, 2013
- Torii Y, Kimura H, Hayashi K, Suzuki M, Kawada J, Kojima S, Katano Y, Goto H, Ito Y.Causes of vertical transmission of hepatitis B virus under the at-risk prevention strategy in Japan.Microbiol Immunol 57:118-21, 2013
- Ito Y, Kawamura Y, Iwata S, Kawada J, Yoshikawa T, Kimura H. Demonstration of type II latency in T lymphocytes of Epstein-Barr Virus -associated hemophagocytic lymphohistiocytosis. Pediatr Blood Cancer 60: 326-328, 2013
2012
- Kimura H, Ito Y, Kawabe S, Gotoh K, Takahashi Y, Kojima S, Naoe T, Esaki S, Kikuta A, Sawada A, Kawa K, Ohshima K, Nakamura S. Epstein-Barr virus (EBV)-associated T/NK lymphoproliferative diseases in non-immunocompromised hosts: prospective analysis of 108 cases. Blood 119:673-86, 2012
- Ito Y, Kimura H, Maeda Y, Hashimoto C, Ishida F, Izutsu K, Sueoka E, Isobe Y, Takizawa J, Hasegawa Y, Kobayashi H, Okamura S, Kobayashi H, Yamaguchi M, Suzumiya J, Hyo R, Nakamura S, Kawa K, Oshimi K, Suzuki R. Pretreatment EBV-DNA copy number is predictive of response and toxicities to SMILE chemotherapy for extranodal NK/T-cell lymphoma, nasal type. Clin Cancer Res 18: 4183-4190, 2012
- Li Z, Yamauchi Y, Kamakura M, Murayama T, Goshima F, Kimura H, Nishiyama Y. Herpes simplex virus requires PARP activity for efficient replication and induces ERK-dependent phosphorylation and ICP0-dependent nuclear localization of tankyrase 1. J Virol 86: 492-503, 2012
- Ko Y-H, Kim H-J, Oh Y-H, Park G, Lee S-S, Huh J, Kim C-W, Kim I, Ng S-B, Tan S-Y, Chuang S-S, Nakamura N, Yoshino T, Nakamura S, Kimura H, Ohshima K. EBV-associated T and NK cell lymphoproliferative disorders: Consensus report of the 4th Asian Hematopathology Workshop. J Hematopathol 5:319–324, 2012
- Muto Y, Goshima F, Ushijima Y, Kimura H, Nishiyama Y. Generation and characterization of UL21-null herpes simplex virus type 1. Front Microbiol 3:394, 2012
- Esaki S, Yamano K, Kiguchi J, Katsumi S, Keceli S, Okamoto H, Goshima F, Kimura H, Nishiyama Y, Murakami S. Diabetic mice show an aggravated course of herpes-simplex-virus-induced facial nerve paralysis. Otol Neurotol 33:1452-7, 2012
- Sahin TT, Kasuya H, Nomura N, Shikano T, Yamamura K, Gewen T, Kanzaki A, Fujii T, Sugae T, Imai T, Nomoto S, Takeda S, Sugimoto H, Kikumori T, Kodera Y, Nishiyama Y , Nakao A. Impact of novel oncolytic virus HF10 on cellular components of the tumor microenviroment in patients with recurrent breast cancer. Cancer Gene Therapy 19:229-37,2012
- Higashimoto Y, Ohta A, Nishiyama Y , Ihira M, Sugata K, Asano Y, Peterson DL, Ablashi DV, Lusso P, Yoshikawa T. Development of a human herpesvirus 6 species-specific immunoblotting assay. Journal of Clinical Microbiology 50:1245-51,2012
- Kawabe S, Ito Y, Gotoh K, Kojima S, Matsumoto K, Kinoshita T, Iwata S, Nishiyama Y, Kimura H. Application of flow cytometric in situ hybridization assay to Epstein–Barr virus-associated T/NK lymphoproliferative diseases. Cancer Sci 103: 1481-8, 2012
- Yasuda K, Sugiura K, Ishikawa R, Kihira M, Negishi Y, Iwayama H, Ito K, Kimura H, Kosugi I, Akiyama M. Perinatal cytomegalovirus -associated bullae in an immunocompetent infant. Arch Dermatol 148: 770-2, 2012
- Luo C, Goshima F, Kamakura M, Mutoh Y, Iwata S, Kimura H, Nishiyama Y. Immunization with a highly attenuated replication -competent herpes simplex virus type 1 mutant, HF10, protects mice from genital disease caused by herpes simplex virus type 2. Front Microbiol 3: 158, 2012
- Isobe Y, Aritaka N, Setoguchi Y, Ito Y, Kimura H, Hamano Y, Sugimoto K, Komatsu N. T/NK-cell type chronic active Epstein-Barr virus (EBV) disease in adults: an underlying condition for EBV-associated T/NK-cell lymphoma. J Clin Pathol 65: 278-82, 2012
- Hirai Y, Yamamoto T, Kimura H, Ito Y, Tsuji K, Miyake T, Morizane S, Suzuki D, Fujii K, Iwatsuki K. Hydroa vacciniforme is associated with increased numbers of Epstein-Barr virus-infected T-cells. J Invest Dermatol 132:1401-8, 2012
- Iwata S, Saito T, Ito Y, Kamakura M, Gotoh K, Kawada J, Nishiyama Y, Kimura H. Antitumor activities of valproic acid on Epstein-Barr virus-associated T and natural killer lymphoma cells. Cancer Sci 103:375-8, 2012
- Kawada J, Iwata N, Kitagawa Y, Kimura H, Ito Y. Prospective monitoring of Epstein-Barr virus and other herpesviruses in patients with juvenile idiopathic arthritis treated with methotrexate and tocilizumab. Mod Rheumatol 22: 565-70, 2012
プレスリリース記事の詳細は次をご覧ください
研究業績
2025年
3「新型コロナワクチンの継続的な接種を優先すべきはだれか?~抗体応答不良の集団特定で接種戦略を最適化、感染拡大・重症化抑制へ~」
7「ありふれたウイルスががんを引き起こす機構を解明!」
9「エンベロープウイルス粒子を蛍光検出する 分子プローブを開発~ウイルス感染力を迅速、簡便に計測する技術を目指して ~」
2024年
1「従来のCAR-T細胞よりも増殖が良好なCAR-T細胞を開発! 〜CAR-T細胞療法の効果増強を期待〜」
9「発がんウイルス(EBウイルス)に感染した細胞の増殖が促進され、腫瘍が形成されるメカニズムを発見」

