研究グループ紹介
最近の神経科学の急速な発展に伴い、遺伝性神経・筋疾患における分子遺伝学的、分子生物学的研究、あるいは認知症および筋萎縮性側索硬化症やパーキンソン病をはじめとした神経難病の研究と治療法の開発は神経内科学の研究において益々重要な分野となっています。
名古屋大学神経内科の特徴として、分子生物学的基礎研究をベースに、日本で弱いとされているコホートを用いた広域型臨床研究、基礎的研究から臨床へ成果を還元する橋渡し研究に力を入れていることであり、基礎研究、臨床研究、橋渡し研究のいずれも日本のみならず、世界の最先端の研究を行っています。
名古屋大学神経内科では、研究方法・研究分野により系統的にグループが構成されており、各グループがそれぞれ独創的かつ特色をもって活発に臨床および基礎研究を進めています。
ALS研究グループ
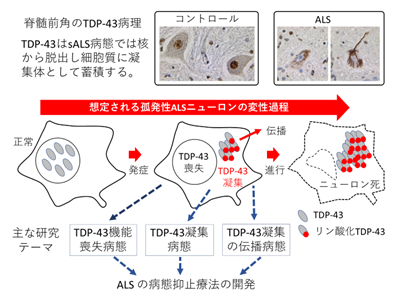
特にこの疾患の9割以上を占める孤発性ALSについては、病態のメカニズムに未解明の点が多く、治療法開発が難航しています。孤発性ALSの変性神経細胞では、RNA結合タンパク質であるTDP-43が本来存在する核から消失し細胞内で封入体を形成することが特徴ですが、その原因は分かっていません。当研究グループは神経細胞におけるTDP-43の機能喪失病態を細胞や動物モデルを用いて解析しています。また、ALS病態においてTDP-43が凝集に至る病態や、TDP-43凝集が細胞間を伝播する病態を解析し、ALSに対する病態抑止療法の開発を目指しています。
SBMA・SMA研究グループ
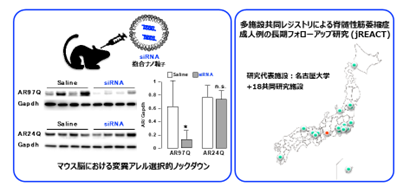
当グループでは運動ニューロン疾患、中でも球脊髄性筋萎縮症(SBMA)、脊髄性筋萎縮症(SMA)の病態解明と、治療法の創出につながる研究に取り組んでいます。ポリグルタミン病の一つでもあるSBMAについては早期病態・外的因子関連病態の解析、オルガノイド研究、個体細胞レベルでの研究とともに、RNA・タンパク質標的治療の開発を行なっています。またAI創薬研究、広く応用可能なポリグルタミン病の治療シーズや中枢神経のドラッグデリバリーシステムのプラットフォーム開発も進めています。SMAに関しては、患者由来細胞、トランスジェニックマウスを用いて発症起点となる病態の検証を行うとともに、一方で患者レジストリ・コホート研究を立ち上げ、疾患重症度や薬効判定のバイオマーカーの開発や、疾患修飾因子の解明にも取り組んでいます。
さらに網羅的遺伝学的解析、培養細胞・動物実験、患者検体の解析を組み合わせ、孤発性も含め神経変性疾患の病態研究も行なっています。本学の他研究科、他大学との共同研究や、企業との産学連携を強化させ、より多面的な研究アプローチを通じて、社会への還元を目指す研究活動を目標としています。
レビー小体病グループ
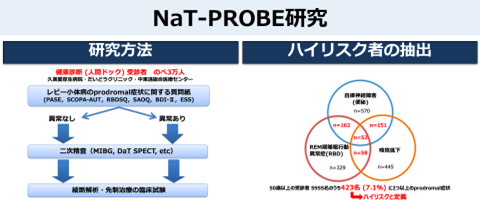
我々はこれまで、健康診断受診者を対象としたレビー小体病のprodromal症状に関する調査研究とレジストリ構築を進めてきました。その結果、50歳以上の健診受診者のうち約7%が2つ以上のprodromal症状を有するハイリスク者に該当し、さらにその約3割の方が神経症状を有しないもののDaT
SPECTもしくはMIBGの異常を呈することを明らかにしました。この結果は、自覚症状のない50歳以上の健診受診者のうち約2-3%でレビー小体病の病態変化が始まっていることを示唆しており、これらの集団がレビー小体病の先制治療のターゲットになると考えています。
一方、パーキンソン病およびレビー小体型認知症の運動症状に対する既承認薬として日常診療で使用されているゾニサミドは、基礎研究などにおいて神経保護作用を示すことが報告されており、prodromal期における神経変性に対する疾患修飾効果が期待されます。そこで我々は、「レビー小体病ハイリスク者に対するゾニサミドの有効性・安全性に関わる探索的臨床試験(NaT-PROBEi)」と題した研究を2021年2月から開始しました。本試験では、2つ以上のprodromal症状と画像異常を有するハイリスク者30例を、二重盲検下でゾニサミド100mg群とプラセボ群の2群に割り付け、96週間にわたって試験薬を投与し、ドパミンニューロンの変性マーカーであるDaT
SPECTのSBR値を主要評価項目として、有効性と安全性を検証します。
末梢神経グループ
末梢神経グループの研究テーマは神経生検および剖検による末梢神経検体の組織病理学的検討、名古屋大学医学部附属病院・関連病院、さらに全国調査によりえられた臨床データに基づいた、自然歴、予後などの検討、さらにこれらの結果に基づいた新規治療法の開発などです。個別の研究テーマは、(1)慢性炎症性脱髄性多発ニューロパチー(CIDP)、(2)ギラン・バレー症候群、(3)アミロイドニューロパチー、(4)血管炎性ニューロパチー(5)サルコイドーシスに伴うニューロパチーなどの臨床病理学的検討や動物モデルの解析です。また、これらの研究と並行して、当教室では多くの臨床医のニーズに答えるべく末梢神経疾患の病理診断の質的向上を目指しています。腓腹神経生検の御依頼や生検標本作製は、当院のみならず関連病院・施設のほか最近では全国からのご依頼も増加傾向にあり、年間100〜140例の組織標本・レポート作成しています。
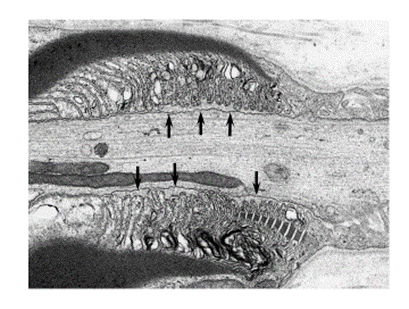
筋グループ
筋グループは、名大病院および関連病院からの依頼により年間100件程度の筋生検を施行しております。直接筋グループが、筋生検術を施行し、各種検索を行い、筋生検結果としてご報告しています。また、鈴鹿病院で多くの筋疾患の患者さんの診療にも携わっております。筋疾患について、多くの先生方から御相談をいただくことも多く、最先端の臨床情報をご提供できるように努めています。
最近、筋疾患の新規遺伝子の発見、デュシャンヌ型筋ジストロフィーに対するエクソンスキップ療法など、筋疾患の発展は目を見張るものがあります。現在筋グループは、①筋疾患の網羅的エクソーム解析、②封入体筋炎、GVHD筋炎の臨床病理学的検討、③封入体筋炎のメタボローム解析、④鈴鹿病院と連携して、筋疾患の医療用ロボットスーツ (HAL ®) によるリハビリテーションの効果解析、筋強直性ジストロフィーのメタボローム解析等の様々な研究が進行中です。
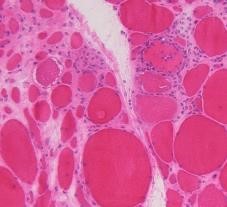
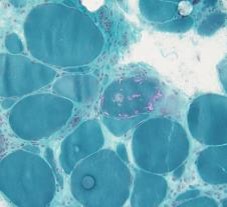
運動異常症・DBS/FUSグループ
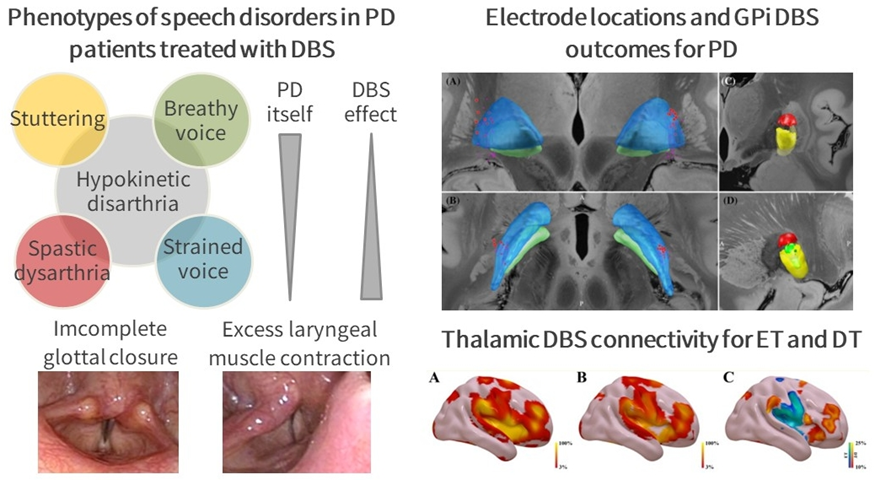
このグループでは,パーキンソン病,本態性振戦,ジストニアなどを中心する運動異常症の患者さんの中でも,特に既存の薬物療法で十分なコントロールを得ることが難しい患者さんを対象とした外科的治療を行っています.名古屋大学では,運動異常症を専門とする脳神経内科医と機能的脳神経外科を専門とする脳神経外科医,さらには言語聴覚士がチームを形成し,脳深部刺激療法(DBS)および集束超音波療法(FUS)の術前の適応評価から術後の治療を共同で行う体制を確立しています.研究面ではこれまでに,DBS術後の運動症状・QOL改善効果のみならず,最も頻度の高い刺激誘発性合併症である発話障害にフォーカスを当て,発話障害の複数の表現型(Tsuboi
et al., JNNP 2015),喉頭機能異常(Tsuboi et al., J Neural Transm 2015),発話リズムの障害(Tsuboi
et al., J Neurol Sci 2019),音響学的特性(Tanaka et al., J Neurol 2015; Tanaka
et al., J Parkinsons Dis 2016; Tanaka et al., J Parkinsons Dis 2020),縦断観察研究に基づく治療ストラテジーの提案(Tsuboi
et al., J Neural Transm 2017)を報告しています.さらに,現在は近年使用可能となったFUSを用いて,パーキンソン病・本態性振戦・ジストニア性振戦などの疾患における振戦の病態基盤の解明および治療成績の向上を目指した研究も進めています.
神経生理グループ
神経生理グループでは、神経伝導検査、針筋電図検査の施行と脳波などの判読を行っています。年間、針筋電図を医師が約300件施行し、さらに1000件前後の末梢神経伝導検査、500件前後の脳波判読を行っています。関連病院医師の電気生理検査の研修も受け入れており、検査を通して非常に多くの症例を学ぶ機会があります。さらに、当グループでは自律神経障害の検査ならびに研究も行っており、起立性低血圧の診断に重要なヘッドアップティルト試験は年間100件近くに及びます。当教室における自律神経研究は全国的にも古くから有名で、約25年前に神経変性疾患におけるMIBG心筋シンチグラフィーの異常を初めて報告していますが、そのほかにも数多くの自律神経障害に関する報告を行っています。近年では、ウェラブルデヴァイスを用いたパーキンソン病の心拍変動の研究や、自律神経機能と画像との関連ついての研究、てんかんの診断に関する研究なども行っており、臨床に役立つ知識を幅広く学ぶことができます。

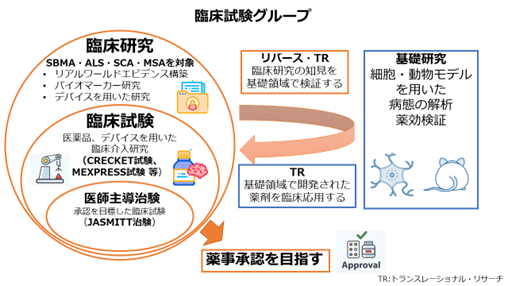
臨床試験グループ
1.球脊髄性筋萎縮症患者の臨床研究
1-①リュープロレリン酢酸塩の臨床開発
名古屋大学神経内科では、遺伝性の神経筋疾患である球脊髄性筋萎縮症(SBMA)について臨床・基礎の両面から研究をすすめています。基礎的研究においては、SBMAの動物モデルにLH-RHアゴニスト(リュープロレリン酢酸塩:リュープリンÒ)を投与すると、本疾患の原因タンパク質である変異アンドロゲン受容体の核内蓄積を阻害し、神経変性が抑制できることが示されました。さらに、この成果を臨床応用する(TR; translational research)ために、数々の自主臨床研究、医師主導治験を実施してきました。それらの結果に基づき、2017年8月25日、リュープロレリン酢酸塩がSBMAの治療薬としての薬事承認を受けることができました。今後は、リュープリンÒの実臨床下での有効性・安全性を検討するため、新たな患者レジストリを構築し、評価を継続しています。
1-②メキシレチン塩酸塩の臨床開発
SBMA患者の多くは、寒冷暴露によって運動麻痺や巧緻運動障害の悪化を呈し、ADLを強く障害されることが経験的に知られていますが、その病態生理は解明されていません。予備的検討において、SBMA患者では健常人に比して、寒冷下で有意に筋力の低下や遠位潜時の延長がみられることを見出しました。このことはSBMAの神経筋障害にイオンチャンネルの機能異常に伴う脱分極の遷延が関与していることを示しており、脱分極の遷延を阻害する薬剤を投与することにより運動症状の改善に寄与することが期待されます。MEXPRESS試験は、上記の研究結果に基づき、SBMA患者に対するメキシレチン塩酸塩経口摂取の有効性及び安全性を検討する多施設共同ランダム化二重盲検クロスオーバー比較試験であり、SBMA患者20症例および健常人20例を対象として、メキシレチン塩酸塩300㎎/日を経口投与し、遠位潜時に与える影響や運動機能に対する有効性及び安全性について評価を行いました。本試験の結果を基に、現在新たな臨床試験を計画中です。
2. 筋萎縮性側索硬化症の臨床研究について
筋萎縮性側索硬化症(ALS)患者から得られるバイオサンプルの解析を中心に、ALSの進行に関連するバイオマーカーや発症前に変化するバイオマーカーの研究を実施しています。
具体的には、患者の血液のメタボローム解析や神経由来エクソソーム中のmiRNAの網羅的な解析を行い、ALSの進行速度を予測できるバイオマーカーを探索し、それらを基礎研究において検証を行う、リバースTR(rTR)の手法を用いて研究を進めています。
発症前のバイオマーカーについては血清CK値が発症前に上昇することを臨床データと統計モデルを用いて推測しています。
また、最近では、尿中のTitinがALSの予後と関連することを明らかにしています。
運動ニューロン疾患の精査のために入院された患者さんを中心に、研究協力のご説明をさせていただいており、今後も継続的に患者さんにご協力いただきながら研究を進めていきます。
3. 脊髄小脳変性症の臨床研究について
遺伝性脊髄小脳変性症に加え、多系統萎縮症患者の臨床研究も積極的に行っています。脊髄小脳変性症については近年病態修飾療法の開発が進んでおり、重症度を適切に反映するバイオマーカーの重要性が増しています。臨床試験グループでは、独自の機器を用いた運動失調の診察や患者血清を用いて、より感度の高いバイオマーカー開発を目標に研究を継続しています。