病態神経科学分野
KEYWORDS
- 筋萎縮性側索硬化症
- アルツハイマー病
- 神経変性疾患
- 神経細胞
- ミクログリア
- アストロサイト
- 神経炎症
- SOD1
- TDP-43
HEAD

LAB MEMBER
| 構成員名 | 役職 | 研究者総覧 |
|---|---|---|
| 小峯 起 | 講師 | 研究者総覧 |
| 遠藤 史人 | 特任講師 | 研究者総覧 |
| 川出 野絵 | 特任助教 | 研究者総覧 |
| 真野 叶子 | 特任助教 | 研究者総覧 |
| 堀内 麻衣 | 特任助教 | 研究者総覧 |
| 前川 華澄 | 特任助教 | 研究者総覧 |
CONTACT
| mnd◎riem.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | 独自ホームページ |
OUTLINE
多くの神経変性疾患では原因遺伝子の同定が進んできた一方で、当研究室がターゲットとする筋萎縮性側索硬化症(ALS)やアルツハイマー病(AD)ではほとんどの患者が孤発性 (非遺伝性)に発症し、「なぜ神経細胞が変性するのか」そして「どのように疾患が進行していくのか」といった病態の本質的な分子機構はいまだ明らかになっていません。
これまで私たちは、ALSの運動神経変性は神経細胞内の異常だけでなく、周囲の非神経細胞(グリア細胞)によって積極的に制御される「非細胞自律性」と呼ばれる神経変性メカニズムを明らかにしました。この知見を踏まえ、神経変性疾患の原因となる脳内環境の破綻について、神経細胞”内”および神経細胞”外”の両面からアプローチすることでそのメカニズムを解明し、得られた理解を新たな治療戦略の開発へとつなげることを当研究室のミッションとしています。
ALS研究においては、RNA結合タンパク質TDP-43をはじめとする病因タンパク質異常やミトコンドリアなどのオルガネラ機能障害が運動神経の変性をどのように引き起こし、さらにミクログリアやアストロサイトといったグリア細胞を介してどのように疾患進行を加速させるのかを明らかにしようとしています。
また、AD研究では、アミロイドβ (Aβ)やタウといった病因タンパク質蓄積に応答したグリア細胞が引き起こす神経炎症や脳内環境変化に着目し、発症・病態進行に関わる分子・細胞基盤の解明、および、疾患治療につながる神経炎症制御分子の同定を目指しています。
これらの研究を通じて、疾患モデルマウスや iPS 細胞を含む in vitro 系を用い、神経細胞内の分子異常から脳内環境の破綻、最終的な神経変性に至る一連の過程を統合的に理解し、神経変性疾患に対する新たな治療介入法の開発を目標としています。
RESEARCH PROJECTS
1. 神経炎症・ミクログリアの活性制御を標的としたALS・ADの病態解明
中枢神経系の自然免疫細胞であるミクログリアは、炎症関連分子や神経保護因子の放出によって神経細胞の周囲環境を変容させる「神経炎症」を誘導し、ALSやADといった神経変性疾患の病態形成に深く関与することが知られています。また、神経変性疾患に共通するミクログリアの活性化状態として Disease-associated microglia(DAM)という概念が提唱されていますが、その機能的意義や疾患共通性の程度などについては未解明な部分が多く残されています。私たちはALS・AD病態におけるミクログリアの活性化状態と神経炎症の役割を体系的に解明することを目指し、網羅的遺伝子発現解析や空間トランスクリプトミクス、ヒト死後脳を用いた統合オミクス解析を進めています。さらに、これらの研究から得られた知見を基盤として、ミクログリア機能および神経炎症を制御することで疾患進行を抑制可能な鍵分子の同定につなげることを目標としています(Sobue et al. Acta Neuropathol Commune, 2021; Wang et al. J Neuroinflamm, 2024; Sobue et al. Cell Death Dis, 2024)。
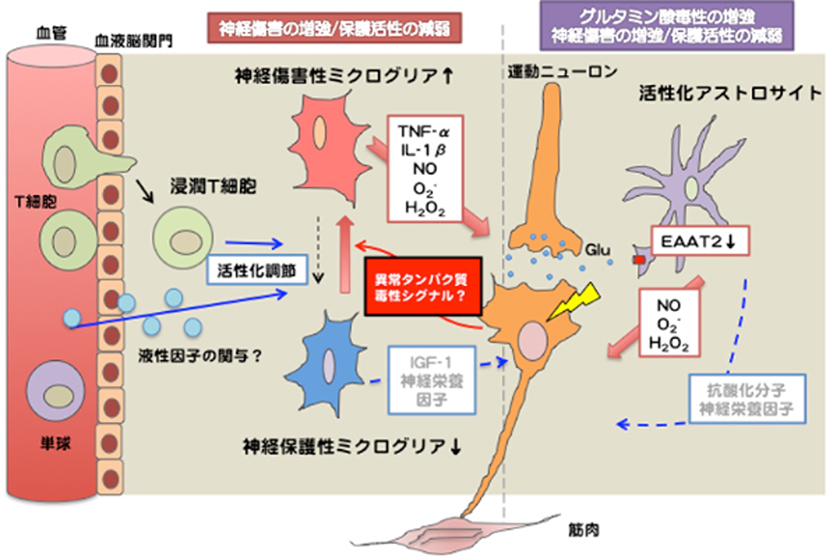
2. AD・ALSのアストロサイトにおける分子病態の解明
アストロサイトは神経細胞に栄養因子を供給するのみならず, シナプス活動の調節など多岐にわたる機能をもつグリア細胞です. 私たちはアストロサイト由来の多機能性サイトカインTGF-β1が病態悪化因子であることを明らかにしました(Endo et al. Cell Rep 2015)。 さらに、ALSやADのアストロサイト病態を解明するため、BioID法(近接依存性ビオチン標識法)を活用したモデルマウスのアストロサイトにおけるタンパク質異常の網羅的同定を行い、新たな視点での病態解明を目指しています。
3. オリゴデンドロサイト・脳白質病態に着目した神経変性機序の解明
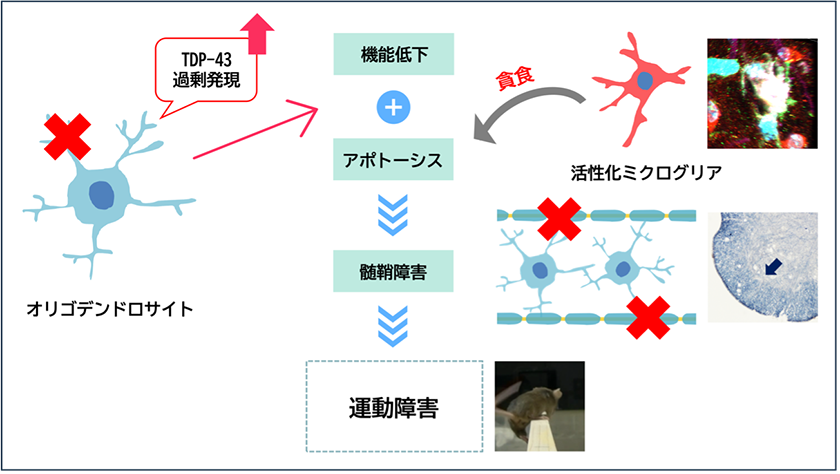
ALSの病因タンパク質であるTDP-43は運動神経以外に、髄鞘形成に関わるグリア細胞であるオリゴデンドロサイトにも異常蓄積することが知られています。遺伝性ALS由来の変異TDP-43をオリゴデンドロサイトに過剰発現するモデルマウスを作成したところ、運動機能障害を引き起こし、髄鞘の障害やオリゴデンドロサイトの細胞死がみられました(Horiuchi et al. Acta Neuropathol Commune 2024:図)。また、ADの早期病変として大脳白質の変化が注目されています。そこで、ADにおいても白質の主要なグリア細胞であるオリゴデンドロサイトの異常や脂質代謝に注目した病態解析をすすめています。
4. TDP-43の異常によるALS発症メカニズムの解明
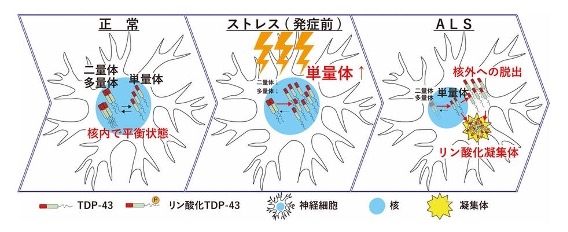
ALSの大部分を占める孤発性ALSや認知症の一種である前頭側頭葉変性症(FTLD)の病巣にTDP-43が蓄積し、TDP-43病理と呼ばれています。 TDP-43の機能やその異常が運動神経にどのような変調をもたらすのかを明らかにすることは、ALSの病態解明の本丸であると考え、解析を進めています. これまでに変異TDP-43は野生型よりも細胞内で異常に安定化すること(Watanabe et al. J Biol Chem 2013)やTDP-43が核内スプライソソーム因子の成熟の場であるGemを破綻させること(Tsuiji et al. EMBO Mol Med 2013)、TDP-43の単量体化がTDP-43病理形成の鍵であること(Oiwa et al. Sci Adv, 2023:図)を見出しました. 現在、これらTDP-43の異常を引き起こすメカニズムの解明を目指し、iPS細胞モデルや疾患モデルマウスを用いた実験を行っています。
5. オルガネラ異常による運動神経変性機序の解明
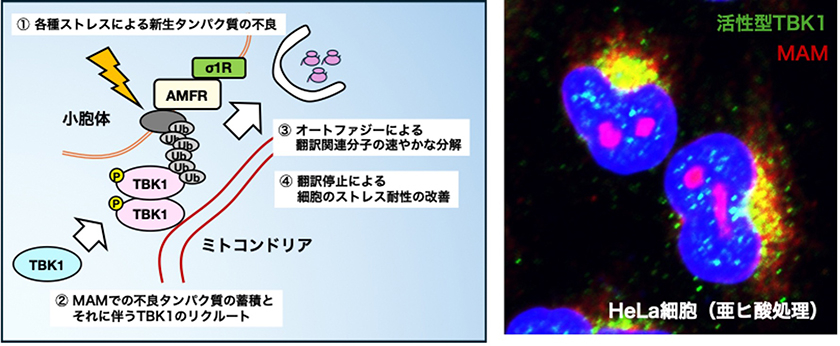
私たちはこれまでに、 異なる2つの家族性ALSモデルマウスにおいて運動神経における小胞体・ミトコンドリア膜間領域(MAM)の崩壊が両者に共通した病態であることを明らかにしました(Watanabe et al. EMBO Mol Med 2016, Watanabe & Horiuchi et al. Neurobiol Dis 2023)。さらに、MAMの破綻がALS原因遺伝子産物であるTBK1の機能を阻害し、異常化したタンパク質に対して細胞を脆弱化させることを報告しました(Watanabe et al. PNAS 2023、図)。 現在、MAMを維持・破綻させる分子メカニズムの解明を目指し、更なる研究を行っています。
BIBLIOGRAPHY
2025
- Watanabe S, Yamanaka K: Mitochondria and Endoplasmic Reticulum Contact Site as a Regulator of Proteostatic Stress Responses in Neurodegenerative Diseases. Bioessays 4: e70016, 2025.
- Maekawa K, Sobue A, Komine O, Saito Y, Murayama S, Saido TC, Saito T, Yamanaka K: Long-term systemic androgen deprivation partially modulates neuroinflammation in male AppNL-G-F/NL-G-F mice. Scientific Reports 15: 14702, 2025.
2024
- Horiuchi M, Watanabe S, Komine O, Takahashi E, Kaneko K, Itohara S, Shimada M, Ogi T, Yamanaka K: ALS-linked mutant TDP-43 in oligodendrocytes induces oligodendrocyte damage and exacerbates motor dysfunction in mice. Acta Neuropathologica Communications 12: 184, 2024.
- Sobue A, Komine O, Endo F, Kakimi C, Miyoshi Y, Kawade N, Watanabe S, Saito Y, Murayama S, Saido SC, Saito T, Yamanaka K: Microglial cannabinoid receptor type II stimulation improves cognitive impairment and neuroinflammation in Alzheimer’s disease mice by controlling astrocyte activation. Cell Death & Diseaae 15: 858, 2024.
- Watanabe S, Amporndanai K, Awais R, Latham C, Awais M, O'Neill PM, Yamanaka K, Hasnain S: Ebselen analogues delay disease onset and its course in fALS by on-target SOD-1 engagement. Scientific Reports 14, 12118, 2024.
- Wang T, Sobue A, Watanabe S, Komine O, Saido TC, Saito T, Yamanaka K: Dimethyl fumarate improves cognitive impairment and neuroinflammation in mice with Alzheimer’s disease. Journal of Neuroinflammation 21(1), 55, 2024.
- Komine O, Ohnuma S, Hinohara K, Hara Y, Shimada M, Akashi T, Watanabe S, Sobue A, Kawade N, Ogi T, Yamanaka K: Genetic background variation impacts microglial heterogeneity and disease progression in amyotrophic lateral sclerosis model mice. iScience 27(2), 108872, 2024.
2023
- Watanabe S, Murata Y, Oka Y, Oiwa K, Horiuchi M, Iguchi Y, Komine O, Sobue A, Katsuno M, Ogi T, Yamanaka K: Mitochondria-associated membrane collapse impairs TBK1-mediated proteostatic stress response in ALS. Proceedings of the National Academy of Sciences of the United States of America 120(47): e2315347120, 2023.
- Oiwa K, Watanabe S, Onodera K, Iguchi Y, Kinoshita Y, KOmine O, Sobue A, Okada Y, Katsuno M, Yamanaka K: Monomerization of TDP-43 is a key determinant for inducing TDP-43 pathology in amyotrophic lateral sclerosis. Science Advances 9(31): eadf6895, 2023.
- Kawade N, Yamanaka K: Novel insights into brain lipid metabolism in Alzheimer's disease: Oligodendrocytes and white matter abnormalities. FEBS Open Bio 14(2): 194-216, 2023.
- Hashimoto K, Watanabe S, Akutu M, Mukai N, Kamishina H, Furukawa Y, Yamanaka K: Intrinsic structural vulnerability in the hydrophobic core induces species-specific aggregation of canine SOD1 with degenerative myelopathy–linked E40K mutation. Journal of Biological Chemistry 299(6): 104798, 2023.
- Sobue A, Komine O, Yamanaka K: Neuroinflammation in Alzheimer’s disease: microglial signature and their relevance to disease. Inflammation & Regeneration 43: 26, 2023.
- Maekawa K, Yamanaka K: Role of sex hormones in neuroinflammation in Alzheimer's disease. Clinical & Experimental Neuroimmunology 4: 16 1045647, 2023.
- Watanabe S, Horiuchi M, Murata Y, Komine O, Kawade N, Sobue A, Yamanaka K: Sigma-1 receptor maintains ATAD3A as a monomer to inhibit mitochondrial fragmentation at the mitochondria-associated membrane in amyotrophic lateral sclerosis. Neurobiology of Disease 2: 179 106031, 2023.
2022
- Yamashita H, Komine O, Fujimori-Tonou, N, Yamanaka K: Comprehensive expression analysis with cell-type-specific transcriptome in ALS-linked mutant SOD1 mice: Revisiting the active role of glial cells in disease. Frontiers in Cellular Neuroscience 4: 16 1045647, 2022.
2021
- Sakai S, Watanabe S, Komine O, Sobue A, and Yamanaka K: Novel reporters of mitochondria-associated membranes (MAM), MAMtrackers, demonstrate MAM disruption as a common pathological feature in amyotrophic lateral sclerosis. FASEB Journal e21688, 2021.
- Sobue A, Komine O, Hara Y, Endo F, Mizoguchi H, Watanabe S, Murayama S, Saito T, Saido T, Sahara N, Higuchi M, Ogi T and Yamanaka K: Microglial gene signature reveals loss of homeostatic microglia associated with neurodegeneration of Alzheimer’s disease. Acta Neuropathologica Communications 9: 1, 2021.
2020
- Watanabe S, Inami H, Oiwa K, Murata Y, Sakai S, Komine O, Sobue A, Iguchi Y, Katsuno M, Yamanaka K: Aggresome formation and liquid–liquid phase separation independently induce cytoplasmic aggregation of TAR DNA-binding protein 43. Cell Death & Disease 11: 909, 2020.
- Amporndanai K, Rogers M, Watanabe S, Yamanaka K, O’Neill P. M., Hasnain S. S.: Novel Selenium-based compounds with therapeutic potential for SOD1-linked Amyotrophic Lateral Sclerosis. EBioMedicine 59: 102980, 2020.
- Watanabe S, Oiwa K, Murata Y, Komine O, Sobue A, Endo F, Takahashi E and Yamanaka K: ALS-linked TDP-43M337V knock-in mice exhibit splicing deregulation without neurodegeneration. Molecular Brain 13: 8, 2020.
2019
- Nishino K, Watanabe S, Shijie J, Murata Y, Oiwa K, Komine O, Endo F, Tsuiji H, Abe M, Sakimura K, Mishra A, Yamanaka K: Mice deficient in the C-terminal domain of TAR DNA-binding protein 43 develop age-dependent motor dysfunction associated with impaired Notch1-Akt signaling pathway. Acta Neuropathologica Communications 7(1): 118, 2019.
- Trias E, Barbeito L, Yamanaka K: Phenotypic heterogeneity of astrocytes in motor neuron disease. Clinical Experimantal Neurology 9(4): 225-234, 2018.
2018
- Komine O, Yamashita H, Fujimori-Tonou N, Koike M, Jin S, Moriwaki Y, Endo F, Watanabe S, Uematsu S, Akira S, Uchiyama Y, Takahashi R, Misawa H, Yamanaka K: Innate immune adaptor TRIF deficiency accelerates disease progression of ALS mice with accumulation of aberrantly activated astrocytes. Cell Death & Differentiation 25: 2130-2146, 2018.
2017
- Watanabe S, Komine O, Fumito E, Wakasugi K, Yamanaka K: Intracerebroventricular administration of Cystatin C ameliorates disease in SOD1-linked amyotrophic lateral sclerosis mice. Journal of Neurochemistry 145(1): 80-89, 2017.
- Yamanaka K, Komine O: The multi-dimensional roles of astrocytes in ALS. Neuroscience Research 126: 31-38, 2018.
- Tsuiji H, Inoue I, Takeuchi M, Furuya A, Yamakage Y, Watanabe S, Koike M, Hattori M, Yamanaka K: TDP-43 accelerates age-dependent degeneration of interneurons. Scientific Reports 7: 14972, 2017.
2016
- Endo F, Komine O, Yamanaka K: Neuroinflammation in motor neuron disease. Clinical and Experimental Neuroimmunology 7: 126-138, 2016.
- Watanabe S, Ilieva H, Tamada H, Nomura H, Komine O, Endo F, Jin S, Mancias P, Kiyama H, Yamanaka K: Mitochondria-associated membrane collapse is a common pathomechanism in SIGMAR1- and SOD1-linked ALS. EMBO Molecular Medicine 8(12): 1421-1437, 2016.
- Lasiene J, Komine O, Fujimori-Tonou N, Powers B, Endo F, Watanabe S, Shijie J, Ravits J, Horner P, Misawa H, Yamanaka K: Neuregulin 1 confers neuroprotection in SOD1-linked amyotrophic lateral sclerosis mice via restoration of C-boutons of spinal motor neurons. Acta Neuropathologica Communications 4: 15, 2016
- Chhangani D, Endo F, Amanullah A, Upadhyay A, Watanabe S, Mishra R, Yamanaka K, Mishra A: Mahogunin ring finger 1 confers cytoprotection against mutant SOD1 aggresomes and is defective in an ALS mouse model. Neurobiology of Disease 86: 16, 2015.
2015
- Komine O & Yamanaka K: Neuroinflammation in motor neuron disease. Nagoya Journal of Medical Science 77: 537, 2015.
- Endo F & Yamanaka K: Astrocytic TGF-β1: detrimental factor in ALS. Oncogene 6: 15728, 2015.
- Endo F, Komine O, Fujimori-Tonou N, Katsuno M, Jin S, Watanabe S, Sobue G, Dezawa M, Wyss-Coray T, Yamanaka K: Astrocyte-derived TGF-β1 accelerates disease progression in ALS mice by interfering with the neuroprotective functions of microglia and T cells. Cell Reports 11: 592, 2015.
- Heneka MT, Carson MJ, Khoury JE, Landreth GE, Brosseron F, Feinstein DL, Jacobs AH, Wyss-Coray T, Vitorica J, Ransohoff RM, Herrup K, Frautschy SA, Finsen B, Brown GC, Verkhratsky A, Yamanaka K, Koistinaho J, Latz E, Halle A, Petzold GC, Town T, Morgan D, Shinohara ML, Perry VH, Holmes C, Bazan NG, Brooks DJ, Hunot S, Joseph B, Deigendesch N, Garaschuk O, Boddeke E, Dinarello CA, Breitner JC, Cole GM, Golenbock DT, Kummer MP: Neuroinflammation in Alzheimer’s disease. Lancet Neurology 14: 388, 2015.
2014
- Watanabe S, Hayakawa T, Wakasugi K, Yamanaka K: Cystatin C protects neuronal cells against mutant copper-zinc superoxide dismutase-mediated toxicity. Cell Death & Disease, 5: e1497, 2014.
- Watanabe S, Ageta-Ishihara N, Nagatsu S, Takao K, Komine O, Endo F, Miyakawa T, Misawa H, Takahashi R, Kinoshita M, Yamanaka K: SIRT1 overexpression ameliorates a mouse model of SOD1-linked amyotrophic lateral sclerosis via HSF1/HSP70i chaperone system. Molecular Brain 7: 62, 2014.
- Austin JA, Wright GS, Watanabe S, Grossmann JG, Antonyuk SV, Yamanaka K, Hasnain SS: Disease causing mutants of TDP-43 nucleic acid binding domains are resistant to aggregation and have increased stability and half-life. Proceedings of the Natural Academy of Sciences, USA 111: 4309-4314, 2014.
- Nomura T, Watanabe S, Kaneko K, Yamanaka K, Nukina N, Furukawa Y: Intranuclear Aggregation of Mutant FUS/TLS as a Molecular Pathomechanism of Amyotrophic Lateral Sclerosis. The Journal of Biological Chemistry, 289: 1192-1202, 2014.
2013
- Furukawa Y, Kaneko K, Watanabe S, Yamanaka K, Nukina N: Intracellular seeded aggregation of mutant Cu,Zn-superoxide dismutase associated with amyotrophic lateral sclerosis. FEBS Letters 587: 2500-2505, 2013.
- Iguchi Y, Katsuno M, Niwa J, Takagi S, Ishigaki S, Ikenaka K, Kawai K, Watanabe H, Yamanaka K, Takahashi R, Misawa H, Sasaki S, Tanaka F, Sobue G: Loss of TDP-43 causes age-dependent progressive motor neuron degeneration. Brain, 136: 1371-1382, 2013.
- Toichi K, Yamanaka K, Furukawa Y: Disulfide scrambling describes the oligomer formation of superoxide dismutase (SOD1) proteins in the familial form of amyotrophic lateral sclerosis. The Journal of Biological Chemistry, 288: 4970-4980, 2013.
- Tsuiji H, Iguchi Y, Furuya A, Kataoka A, Hatsuta H, Atsuta N, Tanaka F, Hashizume Y, Akatsu H, Murayama S, Sobue G, Yamanaka K: Spliceosome integrity is defective in the motor neuron diseases ALS and SMA. EMBO Molecular Medicine, 5: 221-234, 2013.
- Watanabe S, Kaneko K, Yamanaka K: Accelerated disease onset with stabilized familial amyotrophic lateral sclerosis (ALS)-linked TDP-43 mutations. The Journal of Biological Chemistry, 288: 3641-3654, 2013.
2012
- Mishra A, Maheshwari M, Chhangani D, Fujimori-Tonou N, Endo, F, Joshi AP, Jana NR, Yamanaka K. E6-AP association promotes SOD1 aggresomes degradation and suppresses toxicity. Neurobiology of Aging, 34: 1310.e11-23, 2012.
2011
- Lasiene J, Yamanaka K: Glial cells in Amyotrophic Lateral Sclerosis. Neurology Research International 2011: 718987, 2011.
2008
- Yamanaka K, Boillee S, Roberts EA, Garcia ML, McAlonis-Downes M, Mikse OR, Cleveland DW, Goldstein LSB: Mutant SOD1 in cell types other than motor neurons and oligodendrocytes accelerates onset of disease in ALS mice. Proceedings of the Natural Academy of Sciences, USA, 105: 7594-7599, 2008.
- Yamanaka K, Chun SJ, Boillee S, Fujimori-Tonou N, Yamashita H, Gutmann DH, Takahashi R, Misawa H, Cleveland DW: Astrocytes as determinants of disease progression in inherited amyotrophic lateral sclerosis. Nature Neuroscience, 11: 251-253, 2008.
2006
- Boillee S, Yamanaka K, Lobsiger CS, Copeland NG, Jenkins NA, Kassiotis G, Kollias G, Cleveland DW: Onset and Progression in Inherited ALS determined by Motor Neurons and Microglia. Science, 312: 1389-1392, 2006.
MESSAGE
当研究室では大学院生(修士課程・博士課程)を募集しています。また、学部学生や研究生など、様々なかたちで研究活動に参加することが可能です。研究内容に興味を持たれた方は、随時mnd◎riem.nagoya-u.ac.jpまで御連絡下さい。(送信の際は◎を@に変更してください)

