標的探索・治療学
KEYWORDS
- がん
- シグナル伝達
- EV
- 脂質ラフト
HEAD

小根山 千歳
連携教授
CONTACT
| coneyama◎aichi-cc.jp(送信の際は◎を@に変更してください) |
OUTLINE
当講座では、がんを「細胞恒常性維持メカニズムの破綻」として捉え、その分子機構を解明しています。正常細胞は、分化・増殖・運動などを厳密に制御する多層的な仕組みにより恒常性を維持しています。しかし、遺伝子変異やエピジェネティックな異常の蓄積、さらには環境変化によって、シグナル伝達分子の機能異常が生じると、無秩序な増殖や浸潤・転移が引き起こされます。がん治療を困難にしている要因の一つは、その原因が多様かつ複合的であることです。私たちは、がん形質に直接関与する細胞恒常性の分子機構に着目し、その破綻を解明するとともに、薬剤などでその機構に働きかけることで、がん形質を抑制し、がん細胞を正常細胞に近い状態へ導く可能性を探求しています。
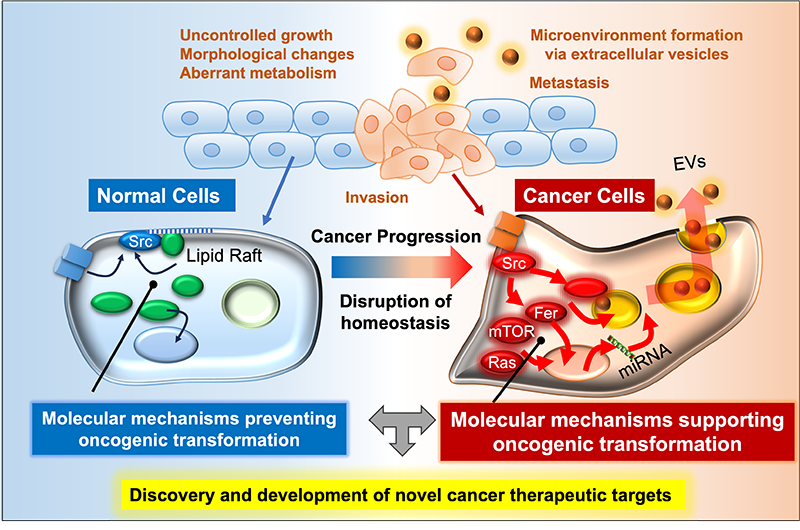
特に、最初に同定されたがん遺伝子産物であり、細胞膜直下に局在するシグナル分子Srcを起点として、恒常性破綻のメカニズムに基づく新たな分子標的を探索し、診断・治療シーズへと結実させることで、がんの先進医療に貢献することを目指しています。
RESEARCH PROJECTS
1. がんにおける細胞外小胞分泌機構の解明とイメージング技術の開発
がん組織は、がん細胞と周囲の細胞から構成され、両者の細胞間コミュニケーションはがんの悪性化や恒常性維持に深く関与しています。近年、直径約100nmの膜小胞であるエクソソームを介した情報伝達が注目され、エクソソーム内包分子の役割や診断応用に関する研究が進んでいます。しかし、がんにおいてエクソソームの「量」や「質」がどのように制御されるのか、その分子機構は未解明です。
私たちは、エクソソーム研究を加速するため、エクソソームマーカー(CD9、CD63、CD81)と高輝度発光タンパク質NanoLucを融合した細胞系を構築しました(Sci Rep, 2018)。この細胞では、培養液中の発光量とエクソソーム数が比例し、分泌量を効率的に定量できます。さらに、この細胞をマウスに移植し、生理的条件下でエクソソーム動態を長期間追跡できるex vivoシステムを開発しました。加えて、BRETによる赤色発光を利用した非侵襲的in vivoイメージングにも成功しました(Sci Rep, 2020; Methods Mol Biol, 2022)。
この実験系を用いて、エクソソーム分泌を制御する分子機構を解明しました。具体的には、エンドソーム膜上のSrcチロシンキナーゼがESCRT関連タンパク質Alixと相互作用し、腔内小胞(ILV)形成を促進することで分泌が亢進することを明らかにしました(Sci Rep, 2019)。さらに、Srcファミリーキナーゼ間で分泌促進作用に差があり、それが脂質ラフトへの親和性と関連していることを見出しました。また、膜融合に関与するSNAREタンパク質がSrcの局在と分泌に影響することも示しました(Biol Pharm Bull, 2022)。加えて、MEK/ERK経路の活性化がエクソソーム分泌増加と相関することを発見しました。MEK活性化により、リソソーム関連遺伝子群の発現が低下し、エンドソーム分解が抑制されることで分泌が亢進します。MEK阻害によりこの過程を抑制すると、がん形質も顕著に抑制されました(Cancer Sci, 2022)。
これらの成果は、がん細胞由来エクソソームの機能解明や、エクソソームを標的とした新規治療法開発に向けた基盤となると考えています (Fig 2)。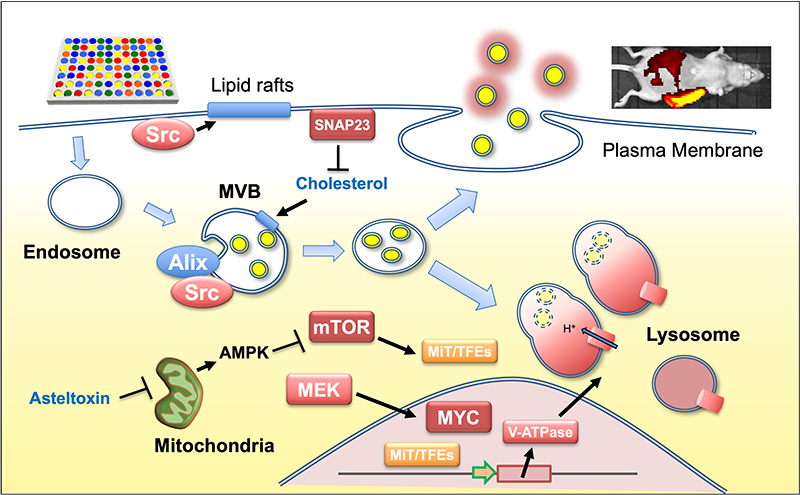
2. 脂質ラフトを介したシグナル制御と多量体型チロシンキナーゼを標的とするがん治療
細胞の生存・増殖を調整するシグナル分子は、発現や活性が精密に制御され、細胞恒常性維持に不可欠です。がん原遺伝子産物c-Srcは代表的なチロシンキナーゼであり、多くのヒトがんで発現・活性の亢進が認められます。しかし、Srcは遺伝子変異を伴わない場合が多く、その制御破綻の分子機構は不明でした。
私たちは、Srcの制御における細胞膜ミクロドメイン脂質ラフトの重要性を明らかにし、コレステロールや脂質代謝酵素のがん形質への関与を報告しました(Mol Cell, 2008; Mol Cell Biol, 2009)。ラフトはシグナル分子を膜上で空間的に制御し、細胞接着斑から発信されるがんシグナルを遮断する機能を担っていました。さらに、ラフト依存的ながんシグナルに関与する分子を探索し、FerキナーゼがSrcシグナル経路の鍵分子であることを同定しました(Oncogene, 2016)。Ferはv-SrcやEGFR活性化による形質転換にも必須であり、Src高発現がん細胞の腫瘍形成や浸潤にも重要です。Ferは大腸・肺・膵臓・乳腺・腎臓など多くのがんで高発現し、正常細胞ではノックダウンしても増殖にほとんど影響しないため、選択的治療標的として有望と考えられます。
さらに、Ferに結合する化合物をスクリーニングし、正常細胞への毒性が低く、がん細胞の増殖を強力に抑制するリード化合物を取得しました。これらは従来の非選択的チロシンキナーゼ阻害剤 (TKI)とは異なる作用機序を持つ新しいタイプの選択的阻害剤であり、高い特異性が期待されます。
本研究は、Src–Fer軸という新しいがんシグナル経路を明らかにし、多量体型チロシンキナーゼを標的とした新規治療戦略につながると考えています (Fig 3)。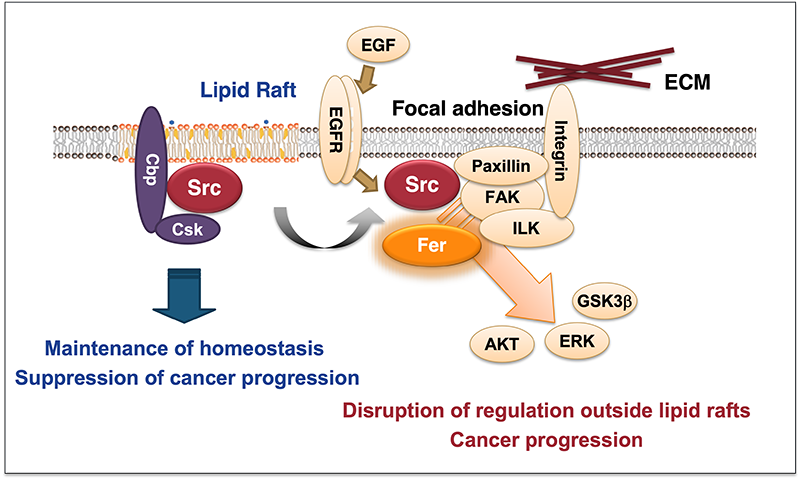
3. マイクロRNAによるがんシグナル制御の解明
現在、microRNA(miRNA)による遺伝子の発現制御が細胞の恒常性維持に果たす役割が次々に明らかとなっています。1つのmiRNAは複数の標的遺伝子の発現を制御し、またそれぞれの遺伝子は複数のmiRNAによる制御を受けています。我々はシグナル異常によるがん形質と密接に関連するmiRNAを探索し(Oncogene, 2011)、その標的遺伝子を明らかにしてきました (J Biochem, 2015; Review)。その結果様々なシグナル分子の発現がmiRNAによる制御を受けており、従来研究されてきたシグナル分子同士の直接的な相互作用の背後に、miRNAを介したシグナルネットワークが存在していることが明らかとなりました。例えば、Srcがんシグナルによって制御されるmiR-99a及びmiR-424/503が、それぞれmTOR複合体2の構成因子であるmTORとRictorを制御していることを見出しました (Oncogene, 2011; Oncogene, 2012; PLoS One, 2013)。またSrc自身もmiR-137やmiR-129-3pによって制御されていることがわかりました (Genes Cells, 2018; Cancer Sci, 2020)。
miRNAを切り口に新たなシグナル分子間の関連性を見出すことは、薬剤耐性を獲得したがんに対する新しい治療戦略につながる可能性があります(Fig.4)。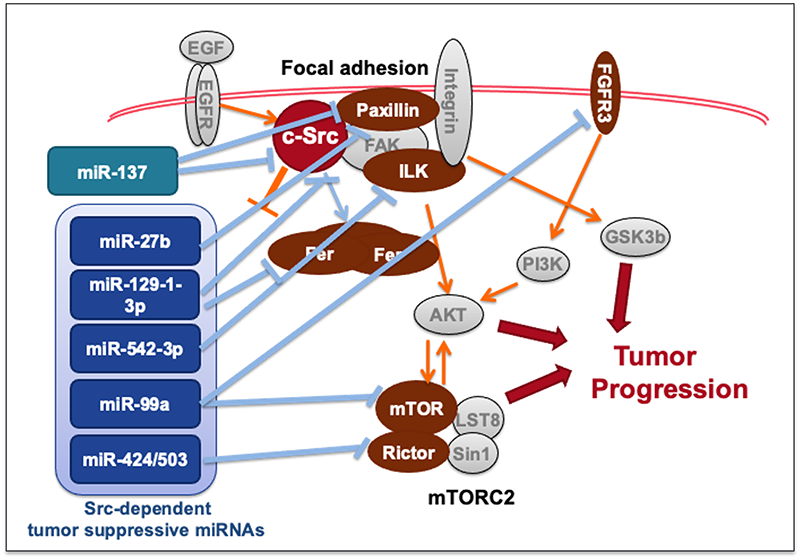
BIBLIOGRAPHY
2024
- Kunitake K, Mizuno T, Hattori K, Oneyama C, Kamiya M, Ota S, Urano Y, Kojima R. Barcoding of small extracellular vesicles with CRISPR-gRNA enables comprehensive, subpopulation-specific analysis of their biogenesis/release regulators. Nat Commun. 15(1), 9777 (2024)
2022
- Mitani F, Lin J, Sakamoto T, Uehara R, Hikita T, Yoshida T, Setiawan A, Arai M, Oneyama C. Asteltoxin inhibits extracellular vesicle production through AMPK/mTOR-mediated activation of lysosome function. Scientific Reports, 12(1), 6674 (2022)
- Hikita T, Uehara R, Itoh RE, Mitani F, Miyata M, Yoshida T, Yamaguchi R, Oneyama C. MEK/ERK-mediated oncogenic signals promote secretion of extracellular vesicles by controlling lysosome function. Cancer Sci, 113(4), 1264-1276 (2022)
- Mitani F, Hayasaka R, Hirayama A, Oneyama C. SNAP23-mediated perturbation of cholesterol-enriched membrane microdomain promotes extracellular vesicle production in Src-activated cancer cells. Biol Pharm Bull, 45(10), 1572-1580 (2022)
- Hikita T, Oneyama C. Quantification and imaging of exosomes via luciferase-fused exosome marker proteins: ExoLuc system. Methods Mol Biol, 2524, 281-290 (2022)
- Morioka S, Nakanishi H, Yamamoto T, Hasegawa J, Tokuda E, Hikita T, Sakihara T, Zhang Y, Oneyama C, Yamazaki M, Suzuki A, Sasaki J, Sasaki T. A novel comprehensive method for measuring the regioisomers of phosphoinositides. Nat Commun, 13(1),83 (2022)
2021
- Nishimura T, Oyama T, Hu HT, Fujioka T, Hanawa-Suetsugu K, Ikeda K, Yamada S, Kawana H, Saigusa D, Ikeda H, Kurata R, Oono-Yakura K, Kitamata M, Kida K, Hikita T, Mizutani K, Yasuhara K, Mimori-Kiyosue Y, Oneyama C, Kurimoto K, Hosokawa Y, Aoki J, Takai Y, Arita M, Suetsugu S. Filopodium-derived vesicles produced by MIM enhance the migration of recipient cells. Dev Cell, 56(6), 842-859 (2021)
2020
- Okuzaki D, Yamauchi T, Mitani F, Miyata M, Ninomiya Y, Watanabe R, Akamatsu H, Oneyama C.: c-Src promotes tumor progression via downregulation of miR-129-1-3p. Cancer Science, 111(2): 418-428 (2020)
- Hikita T, Miyata M, Watanabe R, Oneyama C. In vivo imaging of long-term accumulation of cancer-derived exosomes using a BRET-based reporter. Scientific Reports, 10(1):16616 (2020)
2019
- Hikita T, Kuwahara A, Watanabe R, Miyata M, Oneyama C. Src in endosomal membranes promotes exosome secretion and tumor progression. Scientific Reports, 9(1):3265 (2019)
MESSAGE
一緒に研究して頂ける大学院生を募集しております。日々の一つ一つの実験が新しい発見への一歩になることを一緒に体験して、その喜びを分かち合うことができればと思います。
ご興味のある方はぜひお問い合わせください。

