先端がん標的治療学
KEYWORDS
- 分子標的治療
- KRAS
- 耐性機序
- BRAF
- 新規治療開発
- ctDNA
HEAD

衣斐 寛倫
連携教授
CONTACT
| med◎t.mail.nagoya-u.ac.jp(送信の際は◎を@に変更してください) | |
| HP | 先端がん標的治療学 独自ホームページ |
OUTLINE
当分野は、がんの約40%に存在するKRAS、BRAF遺伝子に異常を有するがんに対する治療開発を行っています。BRAF阻害薬については、研究室が主導した研究をもとに、現在BRAF変異を持つ患者さんに対し、BRAF阻害薬と抗EGFR抗体薬の併用療法がおこなわれています。また、様々なBRAF異常に対し、治療方針を決める際の参考データとしても利用されています。KRAS遺伝子異常を有するがんに対しては、近年阻害薬の開発が急速に進んでいることから、特に、薬剤の耐性機序の解明と、耐性を克服するような新規治療法の提唱に力を入れています。
RESEARCH PROJECTS
i) KRAS阻害薬の耐性機序解明と新規治療開発
KRAS遺伝子は、肺がん(5%)、大腸がん(40%)、膵がん(80%以上)において、高頻度に認められる異常で、がん細胞の生存・増殖に強くかかわっている。発見から40年にわたり有効な薬剤が存在せず、創薬不可能(undruggable)とされてきたが、2022年日本でもKRASを標的とした薬剤が承認され、現在急速に研究が進んでいる。本研究室では、KRAS阻害薬の効果が上皮間葉移行状態(epithelial to mesenchymal transition: EMT)に関連していること、EMTを起こしたKRAS変異腫瘍では、KRASに対する依存性が低下することでKRAS阻害薬に非感受性を示すことを示した(CCR 2020)。さらに、腫瘍細胞は、KRAS阻害薬暴露後、24時間以内に上皮系の性質維持に関連する膜タンパク質の局在変化を誘導し、その結果YAPシグナルを活性化することを明らかにした。YAPシグナルの活性化の結果、RASスーパーファミリータンパクのひとつであるMRASの発現が誘導され、その結果、KRASを抑制してもMRASによりMAPKの活性が維持されることを明らかにした(Nature Cancer 2023)。また、KRAS阻害薬の投与は、腫瘍細胞のCD47(マクロファージによる貪食を阻害するdon’t eat meシグナルと呼ばれる)の発現を誘導し、KRAS阻害薬と免疫チェックポイント阻害薬の不応性にも関与することを明らかにしている(Cell Reports Medicine 2025)。
ii) BRAF変異腫瘍に対する個別化治療の開発
BRAF遺伝子変異は、全固形がんの約8%で認められるドライバー遺伝子異常であり、メラノーマでは約50%、甲状腺がんでは30~70%、大腸がんでは10%、肺がんでは1%の割合で認められる。その多くは600番目のアミノ酸であるバリン(BRAF V600)に発生するが、遺伝子パネル検査を含む次世代シーケンサーの発展に伴い、V600以外の変異(BRAF non-V600)が、大腸がんではBRAF変異の1/3程度、肺がんでは半数程度を占めることが明らかになってきた。
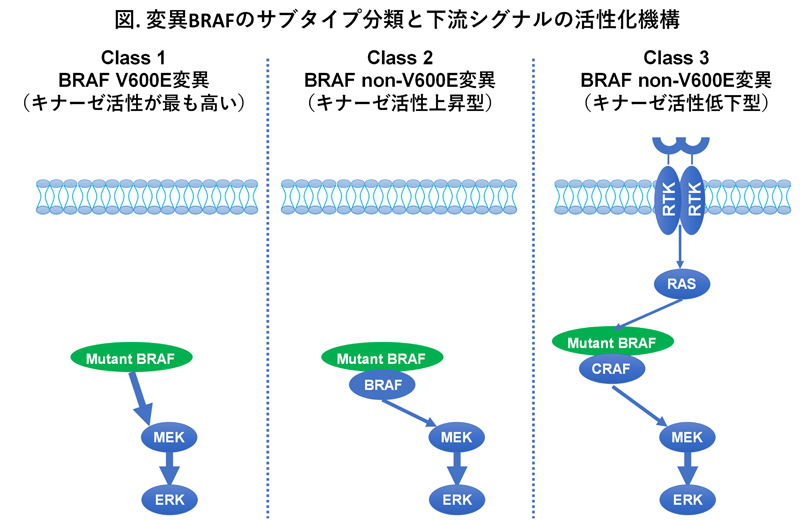
BRAF変異は、変異BRAFタンパクのキナーゼ活性により、3つのタブタイプに分類される。Class 1はBRAF V600変異であり、BRAF V600変異タンパクのキナーゼ活性は野生型BRAFより500倍程度上昇し、単量体の変異BRAFが直接下流シグナルを活性化する。一方、non-V600変異については、部位によりBRAFキナーゼ活性が数倍~50倍程度上昇するもの(Class 2)に加え、活性がむしろ低下するもの(Class 3)が存在する。Class 2変異BRAFは、野生型BRAFと二量体を形成し下流シグナルを活性化する。Class 3変異BRAFは、キナーゼ活性自体は低下しているが、野生型BRAFまたはCRAFと二量体を形成し、二量体が受容体(RTK)-RASにより活性化されることで下流シグナルを活性化する(図)。
BIBLIOGRAPHY
2025
- Hirade K, Tanaka N, Kajino T, Adachi Y, Kimura R, Kasuya H, Kisoda S, Tan TK, Hayakawa S, Sato T, Yanase S, Kitaura Y, Yamamoto T, Nishioka Y, Muto O, Muraoka D, Fujishita T, Kasuga N, Watanabe K, Sakata Y, Aoki M, Matsushita H, Sanda T, Iida S, Tsuchiya K, Yamaguchi R, Ebi H. Inhibiting KRAS with CD47 and immune checkpoint overcomes intrinsic resistance to combined KRAS and immune checkpoint inhibitor therapy. Cell Rep Med. 6:102317, 2025
2023
- Adachi Y, Kimura R, Hirade K, Yanase S, Nishioka Y, Kasuga N, Yamaguchi R, Ebi H. Scribble mis-localization induces adaptive resistance to KRAS G12C inhibitors through feedback activation of MAPK signaling mediated by YAP-induced MRAS. Nat Cancer. 4:829-843, 2023.
2020
- Adachi Y, Ito K, Hayashi Y, Kimura R, Tan TZ, Yamaguchi R, Ebi H. Epithelial-to-Mesenchymal Transition is a Cause of Both Intrinsic and Acquired Resistance to KRAS G12C Inhibitor in KRAS G12C-Mutant Non-Small Cell Lung Cancer. Clin Cancer Res. 26:5962-5973, 2020.
2019
- Yaeger R, Kotani D, Mondaca S, Parikh, AR, Bando H, Van Seventer EE, Taniguchi H, Zhao H, Thant CN, de Stanchina E, Rosen N, Corcoran RB, Yoshino T, Yao Z, Ebi H. Response to Anti-EGFR Therapy in Patients with BRAF non-V600-Mutant Metastatic Colorectal Cancer. Clin Cancer Res 2019.
MESSAGE
KRAS阻害薬は、がん治療の中でも大きなトピックのひとつとなっています。当研究室は、世界各国のRAS研究者と交流、共同研究の実績があり、新規の治療開発や薬剤の作用メカニズムに興味のある方の参加をお待ちしております。

