桐生寿美子

- 桐生寿美子 Sumiko Kiryu-Seo
- 准教授
- 生まれは名古屋ですが、広島、高松、大阪、旭川に住んでいました。一番長く住んだのは大阪です。ネイティブ大阪人からすれば標準語にきこえる(らしい)程度の大阪弁をしゃべります。
研究テーマ
神経損傷や神経変性疾患によって引き起こされる神経細胞死•軸索変性を回避するための答えを見つけたいと考えています。この研究の発端は、神経再生可能な末梢神経を用いて神経再生•修復に関わる分子群のプロファイリングを行い神経再生現象というパズルのピースを集めその大枠を明らかにしようとしたことにあります (Kiryu et al., J Neurosci, 1995; Morita et al., J Neurosci, 1996)。現在では大規模遺伝子スクリーニングやデータサイエンスの発達に伴いさらに詳細な情報が得られるようになっています。これと並行し分子レベルでの機能、個別の細胞のゆらぎ、細胞間・分子間相互作用に至るまで統合的に理解し、生命活動の様々な局面で必要となる神経再生メカニズムを明らかにしたいと考えています。
(1)損傷運動ニューロンの再生・変性のメカニズム
軸索損傷を受けた運動ニューロンはALSなど神経変性疾患に罹患した運動ニューロンと多くのメカニズムを共有しています(Kiryu-Seo et al., J Neurosci, 2005; Kiryu-Seo et al., EMBO J, 2006)。私たちは運動神経損傷というシンプルな実験モデルを利用して、運動ニューロン再生・変性のメカニズムに迫りたいと考えています。
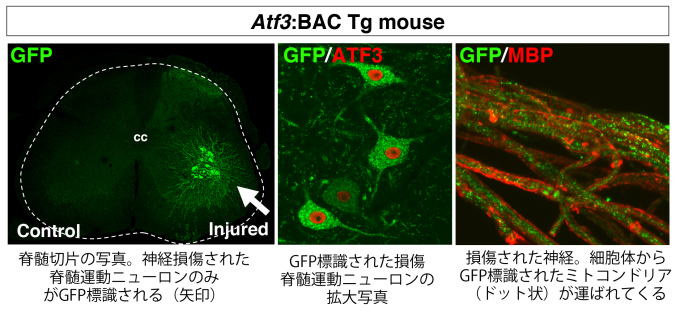
ストレス応答転写因子ATF3は神経再生プログラムを稼働させるキーとなる分子であることがわかっています(Nakagomi et al., J Neurosci, 2003)。ATF3は分化成熟した運動ニューロンを幼若な状態へリプログラムするのではないかと考えられます。私たちは神経損傷に鋭敏に応答して発現誘導されるATF3の転写制御機構を利用し、損傷を受けた神経細胞のみを狙ってcreリコンビナーゼを発現し、かつ、ミトコンドリアをGFP標識するユニークなマウス(Atf3:BAC Tg)を作製しました(図)(Kiryu-Seo et al., Sci Rep, 2016)。このマウスを用いることで再生あるいは疾患関連遺伝子を損傷ニューロン特異的にノックアウトすることが可能になります。また、このマウスは損傷ニューロンの細胞体、軸索、樹状突起のミトコンドリアのみをGFP標識できます。多くの神経変性疾患で発症以前からミトコンドリア動態が変化するなど、ミトコンドリアは細胞内状態を鋭敏に反映する良い指標と考えられています(Kiryu-Seo et al., J Neurosci, 2010)。ところがミトコンドリアはほぼ全ての細胞が持っているオルガネラであるためin vivoでは特定細胞のミトコンドリアのみを可視化することは難しいのですが、これが可能になるのもこのマウスの特徴です。
グリア細胞をはじめとした多様な細胞が関わる神経再生・変性現象を理解するためにはin vivoでの研究が必要です。このマウスを強力なツールとして利用し、運動神経変性疾患と共通した運動ニューロン再生・変性のメカニズムの全貌解明を目指したいと考えています。
(2)神経依存性に組織修復を促すメカニズム
末梢組織・臓器のホメオスタシスは神経により調節されることが明らかになってきています。損傷を受けた後これら組織を修復・再構築する際にも、神経から損傷組織に向けて何らかの制御機構が働くと考えられています。しかし、その分子メカニズムは未だほとんどわかっていません。私達はDINE (Damage induced neuronal endopeptidase)という神経損傷に対して感度良く発現応答する分子に注目し新しいメカニズムを解明しようとしています。 DINEは神経再生関連分子として私達が単離・同定し命名した分子です(Kiryu-Seo et al., PNAS, 2000)。末梢や中枢神経損傷に鋭敏に発現応答する特徴を持っています。膜一回貫通型メタロプロテアーゼでペプチドを基質とすると考えられ、アルツハイマー病の原因分子であるアミロイドβの分解酵素ネプリライシンとファミリーを形成しています。DINE同定以来その機能や意義が全く不明で五里霧中でしたが(Kato et al., J Neurosci, 2002; Kiryu-Seo et al., JBC, 2008)、訳のわからない分子にも関わらず一緒に研究を進めてくれた大学院生達の奮闘により、DINEが発生過程の胎児運動ニューロンの軸索分岐を制御すること(Nagata et al., J Neurosci, 2010; Matsumoto et al., J Neurosci, 2016)、神経原性のヒト先天性関節拘縮症の原因遺伝子であること(Nagata et al., Acta Neuropathol, 2016)、中枢神経である視神経再生に関わること(Kaneko et al., CDDis, 2017)など非常に重要な生理的意義が次第に明らかになってきました。運動神経変性疾患でのDINEの意義についての研究は現在も進行中です。 最近では、皮膚をはじめとした組織や臓器の損傷時にもDINEが重要な働きをすることがわかってきました。組織が損傷を受けるとそこに豊富に分布している感覚神経も同時に損傷を受けます。損傷組織内では免疫細胞や幹細胞などから構成される複雑な細胞集団が組織修復に向けて動き出します。損傷神経ではDINEが発現誘導され、損傷神経末端に集まってきたDINEが自身の切断した分子をメディエーターとしてシグナルを発信しこれら細胞集団をオーガナイズし組織の再生・修復を促すのではないかと考えています。この新たなメカニズムを細胞・分子レベルで解明することが再生医療への貢献につながると期待しています。
好きな言葉・座右の銘
Simple is the best.
シンプルな結果でありながらこの分野を大きく発展させる研究を行えるよう、鋭意努力したいと思っています。
趣味
読書、マッサージ
特技
基本的に暢気だからでしょうか。自分では結構忙しいと思っている時でも暇そうに見える事。
